名校
1 . 下图为元素周期表的一部分。请回答下列问题:
(1)C的最简单氢化物的分子式为____________ ;
(2)N的简单氢化物溶于水,所得溶液显____________ (填“酸性”或“碱性”);
(3)F和Cl的非金属性强弱:F____________ Cl(填“>”或“<”);
(4)Cl的氢化物的水溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为_____________ 。
C | N | F | |
Cl |
(2)N的简单氢化物溶于水,所得溶液显
(3)F和Cl的非金属性强弱:F
(4)Cl的氢化物的水溶液与
 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 乙醇和乙酸是生活中常见的有机化合物。请根据题意填空:
(1)乙酸的工业制法: ,该反应的类和属于
,该反应的类和属于____________ (填“取代”或“加成”)反应;
(2)乙醇在加热、催化剂(Cu或Ag)的条件下,能被空气中的氧气氧化为 ,产物
,产物 的官能团名称是
的官能团名称是____________ (填“羟基”或“醛基”);
(3)乙醇、乙酸和小苏打( )是生活中常见的物质,其中能与小苏打反应的物质是
)是生活中常见的物质,其中能与小苏打反应的物质是____________ (填“乙醇”或“乙酸”)。
(1)乙酸的工业制法:
 ,该反应的类和属于
,该反应的类和属于(2)乙醇在加热、催化剂(Cu或Ag)的条件下,能被空气中的氧气氧化为
 ,产物
,产物 的官能团名称是
的官能团名称是(3)乙醇、乙酸和小苏打(
 )是生活中常见的物质,其中能与小苏打反应的物质是
)是生活中常见的物质,其中能与小苏打反应的物质是
您最近一年使用:0次
名校
解题方法
3 . 非金属元素与人类生活、生产密切相关。根据题意填空:
(1)“84”消毒液常用于公共场所、室内环境的消杀,其有效成分是____________ (填“NaCl”或“NaClO”);
(2)酸雨有很大的危害,能直接损伤农作物、破坏森林和草原。导致酸雨形成的物质有____________ (填“ ”或“NO2”);
”或“NO2”);
(3)为实现“2030年前碳达峰”的目标,我国大力推广硅太阳能电池,组成硅太阳能电池的主要成分是(填“Si”或“ ”)
”)____________ 。
(1)“84”消毒液常用于公共场所、室内环境的消杀,其有效成分是
(2)酸雨有很大的危害,能直接损伤农作物、破坏森林和草原。导致酸雨形成的物质有
 ”或“NO2”);
”或“NO2”);(3)为实现“2030年前碳达峰”的目标,我国大力推广硅太阳能电池,组成硅太阳能电池的主要成分是(填“Si”或“
 ”)
”)
您最近一年使用:0次
名校
解题方法
4 . 金属元素在生产、生活中扮演着重要角色。请根据题意填空:
(1)钠有多种化合物,医疗上常用作抗酸药的是____________ (填“NaOH”或“ ”);
”);
(2)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是____________ (填“FeO”或“ ”);
”);
(3)铝热反应原理常用于金属的冶炼,制取金属钒的反应原理为 ,该反应的氧化剂是
,该反应的氧化剂是____________ 。
(1)钠有多种化合物,医疗上常用作抗酸药的是
 ”);
”);(2)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是
 ”);
”);(3)铝热反应原理常用于金属的冶炼,制取金属钒的反应原理为
 ,该反应的氧化剂是
,该反应的氧化剂是
您最近一年使用:0次
名校
5 . 海水是人类的资源宝库。回答下列问题:
(1)仪器C的名称是_______ 。
(2)装置B中进水口应为_______ (填“a”或“b”)。
Ⅱ.空气吹出法是海水提溴的常用方法。其中一种工艺流程为
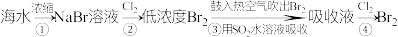
(3)在步骤③中发生反应: ,反应中
,反应中 是
是_______ (填“氧化”或“还原”)剂。
(4)在步骤③中,每吸收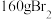 ,理论上需要通入
,理论上需要通入_______ (标准状况下)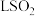 。
。
(5)步骤④发生的反应类型是_______ (填“置换”或“复分解”)反应。
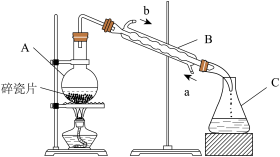
(1)仪器C的名称是
(2)装置B中进水口应为
Ⅱ.空气吹出法是海水提溴的常用方法。其中一种工艺流程为
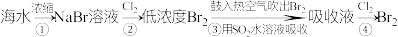
(3)在步骤③中发生反应:
 ,反应中
,反应中 是
是(4)在步骤③中,每吸收
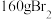 ,理论上需要通入
,理论上需要通入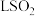 。
。(5)步骤④发生的反应类型是
您最近一年使用:0次
7日内更新
|
122次组卷
|
2卷引用:湖南省普通高中2023-2024学年高一下学期学业水平合格性考试模拟化学试卷四
6 . 化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列转化制得。
(1)X的分子式是_______ 。
(2)Y中含氧官能团的名称是羟基和_______ 。
(3)Y→Z反应的反应类型是_______ 。
(4)乙醛与 反应的化学方程式是
反应的化学方程式是_______ 。

(1)X的分子式是
(2)Y中含氧官能团的名称是羟基和
(3)Y→Z反应的反应类型是
(4)乙醛与
 反应的化学方程式是
反应的化学方程式是
您最近一年使用:0次
7 . 回答下列问题:
(1)① 的电子式是
的电子式是_______ ;②乙炔的结构简式是_______ 。
(2)将红色鲜花放入盛有干燥氯气的集气瓶中,可观察到的现象是_______ 。
(3) 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是_______ 。
(1)①
 的电子式是
的电子式是(2)将红色鲜花放入盛有干燥氯气的集气瓶中,可观察到的现象是
(3)
 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是
您最近一年使用:0次
解题方法
8 . 电子工业常用覆铜板为基础材料制作印刷电路板。现取一定质量的覆铜板,用油性笔画上设计好的图案,浸入盛有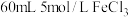 ,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻
,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻 。请计算:
。请计算:
(1) 的物质的量是
的物质的量是_______ mol。
(2)反应过程中,转移电子总数为_______  。
。
(3)为使使用后的“腐蚀液”中金属阳离子完全沉淀,至少需要加入物质的量浓度为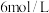 的
的 溶液
溶液_______ mL。
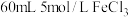 ,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻
,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻 。请计算:
。请计算:(1)
 的物质的量是
的物质的量是(2)反应过程中,转移电子总数为
 。
。(3)为使使用后的“腐蚀液”中金属阳离子完全沉淀,至少需要加入物质的量浓度为
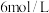 的
的 溶液
溶液
您最近一年使用:0次
9 . 硒(Se)是动物和人体所必需的微量元素,硒单质是一种重要的工业原料。
(1)Se与S同一主族,Se在元素周期表的位置为:第4周期,___________ 。
(2)工业制备Se常用的原料含有硒化铜(CuSe),其中硒元素的化合价为___________ 。
(3)非金属性Br强于Se,用原子结构解释:Se和Br位于周期表中同一周期,原子核外电子层数相同,___________ ,___________ ,得电子能力Br大于Se.
(4)依据元素周期律,下列推断正确的是___________ (填字母)。
a.浓H2SeO4具有氧化性,可能有脱水性
b.热稳定性:H2S<H2Se<HCl
c.CuSe制备Se的过程会产生SeO2烟气,可用NaOH吸收
d.H2Se能与O2或Cl2反应生成Se单质
(1)Se与S同一主族,Se在元素周期表的位置为:第4周期,
(2)工业制备Se常用的原料含有硒化铜(CuSe),其中硒元素的化合价为
(3)非金属性Br强于Se,用原子结构解释:Se和Br位于周期表中同一周期,原子核外电子层数相同,
(4)依据元素周期律,下列推断正确的是
a.浓H2SeO4具有氧化性,可能有脱水性
b.热稳定性:H2S<H2Se<HCl
c.CuSe制备Se的过程会产生SeO2烟气,可用NaOH吸收
d.H2Se能与O2或Cl2反应生成Se单质
您最近一年使用:0次
解题方法
10 . 化学用语是化学专业语言,是学习化学的工具。请回答:
(1)H2S的电子式为___________ ;生产光导纤维的主要原料是为___________ 。
(2)向NaOH溶液中放入一小块铝片,发生的反应离子方程式为___________ 。
(3)在制备乙酸乙酯的实验中,其中浓硫酸的作用为①___________ ;②___________ 。
(1)H2S的电子式为
(2)向NaOH溶液中放入一小块铝片,发生的反应离子方程式为
(3)在制备乙酸乙酯的实验中,其中浓硫酸的作用为①
您最近一年使用:0次



