1 . 酸和醇反应是合成酯的一种重要方法,例如:
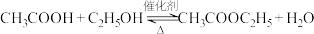
丙烯酸乙酯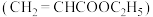 是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:

回答下列问题:
(1)乙烯和丙烯互称为__________ (填“同系物”或“同分异构体”)。
(2)乙醇分子中的官能团名称为___________ (填“羟基”或“羧基”)。
(3)有机物X的结构简式为__________ 。
(4)丙烯酸乙酯有两种官能团,它能发生的化学反应类型为______ (填标号)。
a.加成反应 b.水解反应 c.置换反应
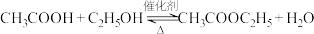
丙烯酸乙酯
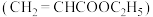 是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
是一种食品用合成香料。以石油化工产品乙烯、丙烯等为原料合成该化合物的路线如下:
回答下列问题:
(1)乙烯和丙烯互称为
(2)乙醇分子中的官能团名称为
(3)有机物X的结构简式为
(4)丙烯酸乙酯有两种官能团,它能发生的化学反应类型为
a.加成反应 b.水解反应 c.置换反应
您最近一年使用:0次
2 . 四氧化三铁(Fe3O4)俗称磁性氧化铁,在工业上应用广泛,可作催化剂、磁记录材料等。Fe3O4的一种制备方法如下:
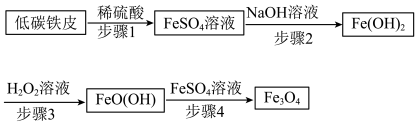
(1)低碳铁皮与稀硫酸反应时,会形成许多微小原电池。
①形成原电池时,Fe作___________ 。
A.正极 B.负极
②反应过程中,溶液的pH___________ 。
A.变大 B.变小 C.不变
(2)检验步骤1得到的FeSO4溶液中是否存在 ,可选用的试剂是___________。
,可选用的试剂是___________。
(3)实验室测定FeSO4溶液的浓度,常用K2Cr2O7标准溶液进行滴定。现称量2.940gK2Cr2O7(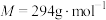 )固体,配制成
)固体,配制成 K2Cr2O7标准溶液。
K2Cr2O7标准溶液。
①称量时,需用到的仪器有___________ 。
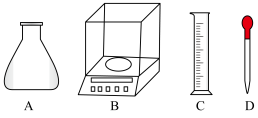
②根据计算,选用的容量瓶规格应为___________ 。
A.100mL B.250mL C.500mL D.1000mL
(4)步骤2用下图所示装置制备 。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
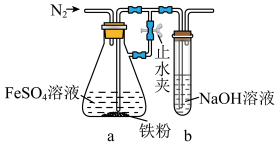
止水夹关闭前后,通入N2的作用分别为___________ 、___________ 。
(5)步骤3的反应原理为: 。反应中每消耗34gH2O2,转移的电子数为
。反应中每消耗34gH2O2,转移的电子数为___________ 。
(6)步骤4在不同时刻得到的Fe3O4粒径大小如下图所示。
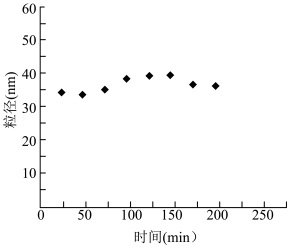
①实验过程中,Fe3O4不易形成沉淀,结合上图分析原因___________ 。
②写出一种可使Fe3O4较快形成沉淀的方法___________ 。

(1)低碳铁皮与稀硫酸反应时,会形成许多微小原电池。
①形成原电池时,Fe作
A.正极 B.负极
②反应过程中,溶液的pH
A.变大 B.变小 C.不变
(2)检验步骤1得到的FeSO4溶液中是否存在
 ,可选用的试剂是___________。
,可选用的试剂是___________。| A.KSCN溶液 | B.KMnO4溶液 | C.稀硝酸 | D.BaCl2溶液 |
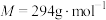 )固体,配制成
)固体,配制成 K2Cr2O7标准溶液。
K2Cr2O7标准溶液。①称量时,需用到的仪器有

②根据计算,选用的容量瓶规格应为
A.100mL B.250mL C.500mL D.1000mL
(4)步骤2用下图所示装置制备
 。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
。制备时,先打开止水夹,通入N2一段时间;再关闭止水夹,继续通入N2一段时间。
止水夹关闭前后,通入N2的作用分别为
(5)步骤3的反应原理为:
 。反应中每消耗34gH2O2,转移的电子数为
。反应中每消耗34gH2O2,转移的电子数为(6)步骤4在不同时刻得到的Fe3O4粒径大小如下图所示。

①实验过程中,Fe3O4不易形成沉淀,结合上图分析原因
②写出一种可使Fe3O4较快形成沉淀的方法
您最近一年使用:0次
3 . 乙醇有多种制备方法。
(1)用粮食制备乙醇的方法称为___________ 法,该法是我国目前生产乙醇的主要方法之一。
(2)乙烯水合法也是一种制备乙醇的方法,用该方法制备乙醇时,乙烯和水发生了___________ 反应(填反应类型)。乙烯主要来源于石油的___________ 。
A.分馏 B.裂化 C.裂解
(3)与上述两种制备乙醇的方法相比,以二氧化碳为碳源,催化氢化制乙醇的方法具有的优势有___________ 、___________ 、___________ 。(列举三点)
(1)用粮食制备乙醇的方法称为
(2)乙烯水合法也是一种制备乙醇的方法,用该方法制备乙醇时,乙烯和水发生了
A.分馏 B.裂化 C.裂解
(3)与上述两种制备乙醇的方法相比,以二氧化碳为碳源,催化氢化制乙醇的方法具有的优势有
您最近一年使用:0次
4 . 乙醇在生产、生活中应用广泛。
(1)乙醇俗称___________ 。
(2)列举乙醇在生活中的两种用途:___________ 、___________ 。
(1)乙醇俗称
(2)列举乙醇在生活中的两种用途:
您最近一年使用:0次
5 . 电解饱和食盐水也可以获得氢气。
(1)电解是将___________ 能转化为___________ 能的过程。
(2)运用绿色化学思想,设想一种用海水制取氢气的方法___________ 。
(1)电解是将
(2)运用绿色化学思想,设想一种用海水制取氢气的方法
您最近一年使用:0次
6 . 以煤炭为原料制备氢气是一种常用的方法,总反应为: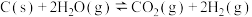 (正反应为吸热反应)
(正反应为吸热反应)
(1)上述反应中,反应物的总能量___________ 生成物的总能量。
A.大于 B.小于 C.等于
(2)下列措施中,能加快上述反应的反应速率的是___________。
(3)能说明上述反应一定达到化学平衡状态的是
(4)一定温度下,在2L密闭容器中加入足量的C(s)和3molH2O(g),反应至5min时,H2O(g)的物质的量变为1mol,0~5min内H2O(g)的平均反应速率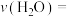
___________ 。
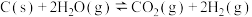 (正反应为吸热反应)
(正反应为吸热反应)(1)上述反应中,反应物的总能量
A.大于 B.小于 C.等于
(2)下列措施中,能加快上述反应的反应速率的是___________。
| A.将煤炭粉碎 | B.通入氦气 | C.降低温度 | D.加入催化剂 |
A. 保持不变 保持不变 | B.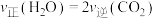 |
| C.物质的总质量不变 | D.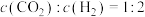 |
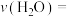
您最近一年使用:0次
7 . “84消毒液”是常见的消毒剂,其有效成分是NaClO。
(1)Cl2和NaOH制备NaClO的化学方程式为___________ 。
(2)如图是某品牌“84消毒液”的使用注意事项。
①注意事项4“易使有色衣物脱色”,是因为“84消毒液”具有___________ 。
A.碱性 B.强氧化性
②注意事项6“不可与酸性物质同时使用”,例如,若将“84消毒液”与“洁厕灵”(含盐酸)同时使用会生成黄绿色有毒气体。写出反应的离子方程式___________ 。
(1)Cl2和NaOH制备NaClO的化学方程式为
(2)如图是某品牌“84消毒液”的使用注意事项。
| 注意事项 1、外用消毒液,勿口服; 2、现用现配,使用时注意戴手套防护; 3、不适用于钢和铝制品的消毒; 4、易使有色衣物脱色; 5、避光、阴凉处保存; 6、不可与酸性物质同时使用。 |
A.碱性 B.强氧化性
②注意事项6“不可与酸性物质同时使用”,例如,若将“84消毒液”与“洁厕灵”(含盐酸)同时使用会生成黄绿色有毒气体。写出反应的离子方程式
您最近一年使用:0次
8 . 实验室提纯粗盐时,将粗盐溶于水后,先除去泥沙等难溶性杂质,再除去 、
、 、
、 等可溶性杂质。
等可溶性杂质。
(1)写出NaCl溶于水时的电离方程式___________ 。
(2)为了除去可溶性杂质,依次加入稍过量的BaCl2溶液、NaOH溶液和Na2CO3溶液,加热至70℃左右约2min,冷却后过滤,得到的沉淀有BaSO4、 、CaCO3和
、CaCO3和___________ 。
 、
、 、
、 等可溶性杂质。
等可溶性杂质。(1)写出NaCl溶于水时的电离方程式
(2)为了除去可溶性杂质,依次加入稍过量的BaCl2溶液、NaOH溶液和Na2CO3溶液,加热至70℃左右约2min,冷却后过滤,得到的沉淀有BaSO4、
 、CaCO3和
、CaCO3和
您最近一年使用:0次
9 . 如表是元素周期表的一部分,表中的每个编号代表一种短周期主族元素,请回答下列问题:
(1)元素②的原子结构示意图是______ 。
(2)比较元素原子半径大小:③______ ④(填“>”或“<”)。
(3)元素③位于元素周期表中第______ 周期VA族。
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式______ 。
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为______ 。
| 族 周期 | IA | 0 | ||||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ② | ③ | ④ | |||||||
| 3 | ⑤ | ⑥ | ||||||||
(2)比较元素原子半径大小:③
(3)元素③位于元素周期表中第
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为
您最近一年使用:0次
10 . 实验室需要配制100mL1.00mol/L的NaNO3溶液,扎西老师进行了如下操作:
(1)计算需要NaNO3固体的质量:______ 克。
(2)根据计算结果,用______ (填仪器名称)称量NaNO3固体。
(3)在烧杯中加入适量蒸馏水,将固体溶解;冷却至室温,将烧杯中的溶液转移至容量瓶时,玻璃棒的作用是______ ;用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液一并注入到容量瓶中。
(4)将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2cm时,改用______ (填仪器名称)滴加蒸馏水至液面与刻度线相切;盖好瓶塞,反复上下颠倒,摇匀。
(5)定容时,仰视液面,则所配溶液物质的量浓度______ (填“偏大”或“偏小”)。
(1)计算需要NaNO3固体的质量:
(2)根据计算结果,用
(3)在烧杯中加入适量蒸馏水,将固体溶解;冷却至室温,将烧杯中的溶液转移至容量瓶时,玻璃棒的作用是
(4)将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2cm时,改用
(5)定容时,仰视液面,则所配溶液物质的量浓度
您最近一年使用:0次



