解题方法
1 . 从物质类别和元素价态的视角认识氮及其化合物间的转化关系,以N2为起点,分别以 、
、 为终点,设计如下两种“向空气要氮肥”的转化方案。
为终点,设计如下两种“向空气要氮肥”的转化方案。
(1)X的电子式为_______ 。方案1-①步骤中利用了N2的_______ (填“氧化”或“还原”)性。写出方案1-②步骤中反应的离子方程式:_______ 。
(2)Y的化学式为_______ 。方案2中属于非氧化还原反应的步骤为_______ (填编号)。实验室将浓硝酸保存在棕色试剂瓶中,且需放置在阴凉处,其原因是_______ 。
(3)利用下图实验装置实现方案2中从NO到HNO3的转化。_______ 。
ii.然后打开弹簧夹,快速吸入10mL空气后夹上弹簧夹,观察到气体先由无色变红棕色,振荡后又逐渐变浅至无色。此过程中涉及反应的化学方程式有2NO+O2=2NO2及_______ 。若将注射器内NO充分转化为HNO3,需吸入_______ 后,再振荡。
(4)浓硝酸在工业生产中不选择 铜制容器盛装的理由,用化学方程式表示为_______ 。
(5)NO2污染环境,可用NH3将其催化转化为N2,每转化33.6L(已折算成标准状况的气体体积)NO2,理论上消耗NH3的物质的量为_______ mol。
 、
、 为终点,设计如下两种“向空气要氮肥”的转化方案。
为终点,设计如下两种“向空气要氮肥”的转化方案。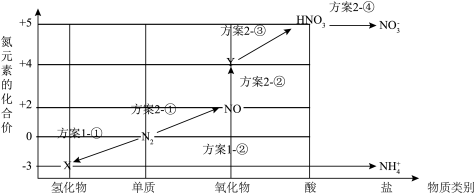
(1)X的电子式为
(2)Y的化学式为
(3)利用下图实验装置实现方案2中从NO到HNO3的转化。
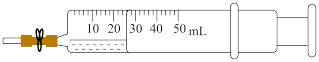
ii.然后打开弹簧夹,快速吸入10mL空气后夹上弹簧夹,观察到气体先由无色变红棕色,振荡后又逐渐变浅至无色。此过程中涉及反应的化学方程式有2NO+O2=2NO2及
(4)浓硝酸在工业生产中
(5)NO2污染环境,可用NH3将其催化转化为N2,每转化33.6L(已折算成标准状况的气体体积)NO2,理论上消耗NH3的物质的量为
您最近一年使用:0次
2 . 在2L的恒容密闭容器中充入1mol CO和2mol 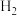 ,一定条件下发生反应:
,一定条件下发生反应: ,测得和
,测得和 的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
的物质的量变化如图1所示,反应过程中的能量变化如图2所示。___________  。平衡时
。平衡时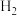 的转化率为
的转化率为___________ 。
(2)下列措施能增大反应速率的是___________(填字母)。
(3)下列描述中能说明上述反应达到平衡状态的是___________。
(4)该反应是___________ 反应(填“吸热”或“放热”),已知断开1mol CO(g)和2mol  中的化学键需要吸收的能量为1924kJ,则断开1mol
中的化学键需要吸收的能量为1924kJ,则断开1mol  中的化学键所需要吸收
中的化学键所需要吸收___________ kJ的能量。
(5)汽车尾气(含有烃类、CO、 、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式
、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式___________ 。
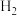 ,一定条件下发生反应:
,一定条件下发生反应: ,测得和
,测得和 的物质的量变化如图1所示,反应过程中的能量变化如图2所示。
的物质的量变化如图1所示,反应过程中的能量变化如图2所示。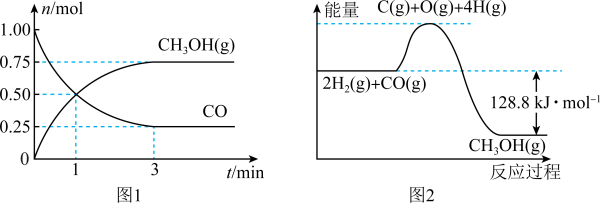
 。平衡时
。平衡时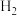 的转化率为
的转化率为(2)下列措施能增大反应速率的是___________(填字母)。
| A.升高温度 | B.降低压强 | C.减小 的浓度 的浓度 | D.加入合适的催化剂 |
(3)下列描述中能说明上述反应达到平衡状态的是___________。
A.CO、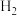 和 和 三种物质的浓度相等 三种物质的浓度相等 |
| B.混合气体的密度不随时间的变化而变化 |
| C.混合气体的总物质的量不随时间的变化而变化 |
D.单位时间内消耗2mol 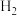 的同时生成1mol 的同时生成1mol  |
(4)该反应是
 中的化学键需要吸收的能量为1924kJ,则断开1mol
中的化学键需要吸收的能量为1924kJ,则断开1mol  中的化学键所需要吸收
中的化学键所需要吸收(5)汽车尾气(含有烃类、CO、
 、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式
、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式
您最近一年使用:0次
2024-07-12更新
|
98次组卷
|
2卷引用:2024年天津市普通高中学业水平合格性考试河东区化学模拟试卷
3 . 我国空间站“天和”核心舱太阳翼电池采用自主研发的砷化镓器件,能量转化效率大大提高。
已知:砷(As)与镓(Ga)同位于第四周期;Ga与Al同主族,As与P同主族。
(1)铝元素的原子结构示意图为___________ 。
(2)P在元素周期表中的位置是___________ 。
(3)P的非金属性弱于S的,用原子结构解释原因:P和S在同一周期,原子核外电子层数相同,___________ ,得电子能力P弱于S。
(4)下列关于Ga的推断正确的是___________ (填字母)。
a.最外层电子数为5
b.原子半径:
c.元素的金属性:
(5)氮的简单氢化物的电子式___________ , ,
, ,
, 的酸性由强到弱的关系是
的酸性由强到弱的关系是___________ 。
(6)三价砷有剧毒,五价砷毒性减弱。含 的污水可被次氯酸钠碱性溶液转化为
的污水可被次氯酸钠碱性溶液转化为 而降低毒性。该反应的离子方程式是
而降低毒性。该反应的离子方程式是___________ 。
已知:砷(As)与镓(Ga)同位于第四周期;Ga与Al同主族,As与P同主族。
(1)铝元素的原子结构示意图为
(2)P在元素周期表中的位置是
(3)P的非金属性弱于S的,用原子结构解释原因:P和S在同一周期,原子核外电子层数相同,
(4)下列关于Ga的推断正确的是
a.最外层电子数为5
b.原子半径:

c.元素的金属性:

(5)氮的简单氢化物的电子式
 ,
, ,
, 的酸性由强到弱的关系是
的酸性由强到弱的关系是(6)三价砷有剧毒,五价砷毒性减弱。含
 的污水可被次氯酸钠碱性溶液转化为
的污水可被次氯酸钠碱性溶液转化为 而降低毒性。该反应的离子方程式是
而降低毒性。该反应的离子方程式是
您最近一年使用:0次
2024-07-12更新
|
66次组卷
|
2卷引用:2024年天津市普通高中学业水平合格性考试河东区化学模拟试卷
解题方法
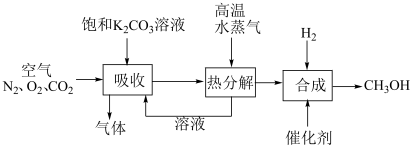
4 . CO2是一种温室气体。种吸收空气中的CO2并催化加氢合成CH3OH的流程如下:________ 。
(2)“吸收”“热分解”两步的目的是________ 。
(3)CH3OH的官能团是________ ;CH3OH分子中与碳原子形成共价键的原子的数目是________ 。
(2)“吸收”“热分解”两步的目的是
(3)CH3OH的官能团是
您最近一年使用:0次
5 . 回答下列问题:
(1)写出Ca(ClO)2的名称:_______ ;写出CO2的结构式:______ 。
(2)写出二氧化氮与水反应的化学方程式:___________ 。
(3)向氯化铝溶液中逐滴加入氢氧化钠溶液,观察到的现象为_______ 。
(1)写出Ca(ClO)2的名称:
(2)写出二氧化氮与水反应的化学方程式:
(3)向氯化铝溶液中逐滴加入氢氧化钠溶液,观察到的现象为
您最近一年使用:0次
解题方法
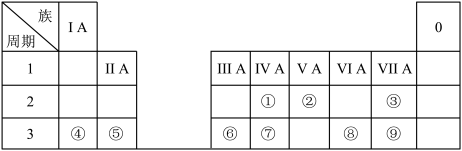
6 . 根据表中9种元素及由这些元素形成的单质和化合物,完成下列问题:_____ 。
(2)①②③非金属性最强的是_____ (填元素符号)。
(3)④的单质与水反应的离子方程式为_____ 。
(4)③和④的简单离子半径大小:③_____ (填“ ”或“
”或“ ”)④。
”)④。
(2)①②③非金属性最强的是
(3)④的单质与水反应的离子方程式为
(4)③和④的简单离子半径大小:③
 ”或“
”或“ ”)④。
”)④。
您最近一年使用:0次
7 . 化学电池的发明,改变了人们的生活方式。
(1)某原电池实验装置如图所示。___________ (填“正极”或“负极”)。
②Zn片上的电极反应为___________ 。
③能证明化学能转化为电能的实验现象是___________ 。
(2)微型锌银纽扣电池的装置如图所示。___________ (填字母)。
a.Zn发生氧化反应
b.Ag2O在正极发生反应
c.电池工作时,K+向Zn极移动
d.电池工作时,电子由Ag2O极经外电路流向Zn极
(1)某原电池实验装置如图所示。
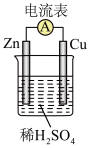
②Zn片上的电极反应为
③能证明化学能转化为电能的实验现象是
(2)微型锌银纽扣电池的装置如图所示。
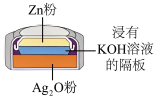
a.Zn发生氧化反应
b.Ag2O在正极发生反应
c.电池工作时,K+向Zn极移动
d.电池工作时,电子由Ag2O极经外电路流向Zn极
您最近一年使用:0次
8 . 化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列转化制得。
(1)X的分子式是_______ 。
(2)Y中含氧官能团的名称是羟基和_______ 。
(3)Y→Z反应的反应类型是_______ 。
(4)乙醛与 反应的化学方程式是
反应的化学方程式是_______ 。

(1)X的分子式是
(2)Y中含氧官能团的名称是羟基和
(3)Y→Z反应的反应类型是
(4)乙醛与
 反应的化学方程式是
反应的化学方程式是
您最近一年使用:0次
9 . 回答下列问题:
(1)① 的电子式是
的电子式是_______ ;②乙炔的结构简式是_______ 。
(2)将红色鲜花放入盛有干燥氯气的集气瓶中,可观察到的现象是_______ 。
(3) 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是_______ 。
(1)①
 的电子式是
的电子式是(2)将红色鲜花放入盛有干燥氯气的集气瓶中,可观察到的现象是
(3)
 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是
您最近一年使用:0次
解题方法
10 . 化学用语是化学专业语言,是学习化学的工具。请回答:
(1)H2S的电子式为___________ ;生产光导纤维的主要原料是为___________ 。
(2)向NaOH溶液中放入一小块铝片,发生的反应离子方程式为___________ 。
(3)在制备乙酸乙酯的实验中,其中浓硫酸的作用为①___________ ;②___________ 。
(1)H2S的电子式为
(2)向NaOH溶液中放入一小块铝片,发生的反应离子方程式为
(3)在制备乙酸乙酯的实验中,其中浓硫酸的作用为①
您最近一年使用:0次



