名校
解题方法
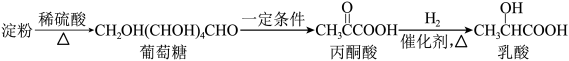
1 . 乳酸在生活中应用广泛,可通过多种途径制得。以淀粉为原料可经过如下转化制得乳酸:________ 。
(2)银氨溶液是实验室常见试剂,以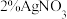 溶液和2%氨水为原料制取银氨溶液的方法是
溶液和2%氨水为原料制取银氨溶液的方法是________ 。
(3)设计检验淀粉与稀硫酸共热后所得水解液中是否含有葡萄糖的实验方案:________ 。
(4)1mol丙酮酸中所含 键的数目为
键的数目为________ 。
(5)乳酸可聚合成易降解的高分子材料,写出该高分子材料分子的结构简式:________ 。
(6)完善以 为原料的物质转化图
为原料的物质转化图______ (燃烧、与酸性 溶液、卤素单质反应除外,同一类型的反应只需写一种,所得有机产物均需写出)
溶液、卤素单质反应除外,同一类型的反应只需写一种,所得有机产物均需写出)
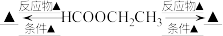
(2)银氨溶液是实验室常见试剂,以
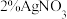 溶液和2%氨水为原料制取银氨溶液的方法是
溶液和2%氨水为原料制取银氨溶液的方法是(3)设计检验淀粉与稀硫酸共热后所得水解液中是否含有葡萄糖的实验方案:
(4)1mol丙酮酸中所含
 键的数目为
键的数目为(5)乳酸可聚合成易降解的高分子材料,写出该高分子材料分子的结构简式:
(6)完善以
 为原料的物质转化图
为原料的物质转化图 溶液、卤素单质反应除外,同一类型的反应只需写一种,所得有机产物均需写出)
溶液、卤素单质反应除外,同一类型的反应只需写一种,所得有机产物均需写出)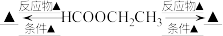
您最近一年使用:0次
昨日更新
|
10次组卷
|
2卷引用:江苏省南京市第九中学2023-2024学年高一下学期教学质量调研(二)化学试题
名校
解题方法
2 . 根据信息书写指定反应的方程式。
(1)请从下列试剂中选择合适的完成指定转化。
试剂: 溶液、稀硝酸、
溶液、稀硝酸、 溶液、
溶液、 溶液、
溶液、 溶液
溶液
① 的离子方程式:
的离子方程式:________ ;
②酸性条件下 (有强氧化性)
(有强氧化性)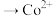 的离子方程式:
的离子方程式:________ 。
(2)工业上可利用氨水吸收 和
和 ,原理如下图所示。
,原理如下图所示。 被氨水吸收后生成含
被氨水吸收后生成含 和
和 溶液的离子方程式:
溶液的离子方程式:________ ;
② 被
被 吸收的离子方程式:
吸收的离子方程式:________ 。
(1)请从下列试剂中选择合适的完成指定转化。
试剂:
 溶液、稀硝酸、
溶液、稀硝酸、 溶液、
溶液、 溶液、
溶液、 溶液
溶液①
 的离子方程式:
的离子方程式:②酸性条件下
 (有强氧化性)
(有强氧化性)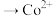 的离子方程式:
的离子方程式:(2)工业上可利用氨水吸收
 和
和 ,原理如下图所示。
,原理如下图所示。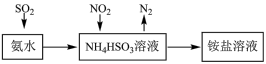
 被氨水吸收后生成含
被氨水吸收后生成含 和
和 溶液的离子方程式:
溶液的离子方程式:②
 被
被 吸收的离子方程式:
吸收的离子方程式:
您最近一年使用:0次
昨日更新
|
13次组卷
|
2卷引用:江苏省南京市第九中学2023-2024学年高一下学期教学质量调研(二)化学试题
3 . 在化学反应的研究和实际应用中,人们还要关注化学反应进行的快慢和程度,以提高生产效率。请回答下列问题。
(1)在一定温度下,2L体积不变密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正、逆反应速率大小
时刻,正、逆反应速率大小
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
②若 ,计算反应开始至
,计算反应开始至 时刻用
时刻用 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为_______  。
。
③如果升高温度,则
_______ (填“增大”“减小”或“不变”)。
(2)在 密闭容器内,800℃时仅发生反应
密闭容器内,800℃时仅发生反应 ,体系中开始仅含有
,体系中开始仅含有 和
和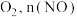 随时间的变化如下表所示:
随时间的变化如下表所示:
① 时,生成
时,生成 的物质的量为
的物质的量为_______  ,在第
,在第 时,
时, 的转化率为
的转化率为_______ 。
②已知图中曲线分别代表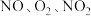 浓度变化曲线,则无关曲线为
浓度变化曲线,则无关曲线为_______ (填字母)。_______ (填字母)。
a.容器内压强不再变化 b.混合气体颜色不再改变
c.混合气体的平均相对分子质量不变 d.容器内密度保持不变
(1)在一定温度下,2L体积不变密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
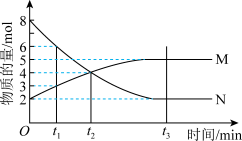
 时刻,正、逆反应速率大小
时刻,正、逆反应速率大小
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。②若
 ,计算反应开始至
,计算反应开始至 时刻用
时刻用 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为 。
。③如果升高温度,则

(2)在
 密闭容器内,800℃时仅发生反应
密闭容器内,800℃时仅发生反应 ,体系中开始仅含有
,体系中开始仅含有 和
和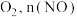 随时间的变化如下表所示:
随时间的变化如下表所示:时间 | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
 时,生成
时,生成 的物质的量为
的物质的量为 ,在第
,在第 时,
时, 的转化率为
的转化率为②已知图中曲线分别代表
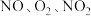 浓度变化曲线,则无关曲线为
浓度变化曲线,则无关曲线为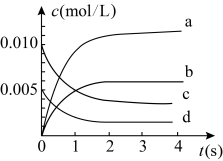
a.容器内压强不再变化 b.混合气体颜色不再改变
c.混合气体的平均相对分子质量不变 d.容器内密度保持不变
您最近一年使用:0次
名校
解题方法
4 . 化学电源广泛地应用于现代社会的生产和生活。请回答下列问题:
(1)原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是_______(填字母)。
(2)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图实验。_______ 。
②Zn棒是_______ 极,电流方向是从_______ 棒流向_______ 棒。
(3)若将两个金属棒用导线相连在一起,总质量为80.00g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为47.5g,则装置工作时锌片上的电极反应式为_______ ,工作时间内装置所产生氢气的体积为_______ L(标准状况)。
(1)原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是_______(填字母)。
A.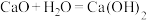 |
B. |
C. |
D. |
(2)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图实验。

②Zn棒是
(3)若将两个金属棒用导线相连在一起,总质量为80.00g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为47.5g,则装置工作时锌片上的电极反应式为
您最近一年使用:0次
名校
5 . 氧化还原反应原理在研究物质性质及物质转化等方面具有重要的价值。回答下列问题:
(1)按照不同的分类方法将下列化学反应进行分类。
a. ;b.
;b. ;c.
;c.
d. ;e.
;e.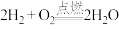 。
。
其中属于氧化还原反应,但不属于四大基本反应类型的是______ (填字母)。
(2)亚硝酸钠( )具有致癌作用,许多腌制食品中含
)具有致癌作用,许多腌制食品中含 。酸性
。酸性 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:
,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:______ 。
(3)新储氢材料—碳纳米管可利用电弧法合成,合成过程中会伴随大量的碳纳米颗粒杂质,这种碳纳米颗粒杂质可用氧化气化法提纯,反应方程式为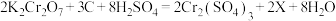

①该反应中,生成物X的化学式为______ 。
②该反应中,氧化剂为______ (填化学式),被氧化的元素为______ (填元素符号)。
③该反应中, 表现出
表现出______ (填字母)
A.酸性 B.还原性 C.氧化性
④该反应中,每生成3mol ,转移
,转移______ mol电子。
(1)按照不同的分类方法将下列化学反应进行分类。
a.
 ;b.
;b. ;c.
;c.
d.
 ;e.
;e.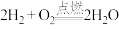 。
。其中属于氧化还原反应,但不属于四大基本反应类型的是
(2)亚硝酸钠(
 )具有致癌作用,许多腌制食品中含
)具有致癌作用,许多腌制食品中含 。酸性
。酸性 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:
,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:(3)新储氢材料—碳纳米管可利用电弧法合成,合成过程中会伴随大量的碳纳米颗粒杂质,这种碳纳米颗粒杂质可用氧化气化法提纯,反应方程式为
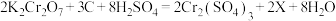

①该反应中,生成物X的化学式为
②该反应中,氧化剂为
③该反应中,
 表现出
表现出A.酸性 B.还原性 C.氧化性
④该反应中,每生成3mol
 ,转移
,转移
您最近一年使用:0次
6 . 完成下列问题。
(1)一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸中直接加入纯化后的甲醇(CH3OH),同时向一个电极通入空气。
①此电池的正极发生的电极反应为_______ 。
②电解液中H+向_____ 极移动。
(2)如图所示,该装置通电5 min后,电极5的质量增加2.16 g,回答下列问题:____ 极,A池阴极电极反应:______ ,C池阳极电极反应:_______ 。
②如果B槽中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为______ 。
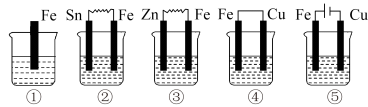
(3)下图各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由大到小的顺序为_____ 。______ 。
(1)一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸中直接加入纯化后的甲醇(CH3OH),同时向一个电极通入空气。
①此电池的正极发生的电极反应为
②电解液中H+向
(2)如图所示,该装置通电5 min后,电极5的质量增加2.16 g,回答下列问题:
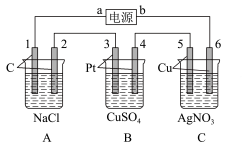
②如果B槽中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
(3)下图各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由大到小的顺序为
您最近一年使用:0次
7 . 爱护水资源,落实长江大保护。
(1)树立保护水体意识。下列做法正确的有___________ 。
A.节约用水 B.工业用水重复利用 C.洗衣污水集中处理
(2)掌握水的净化方法。日常生活中,我们常使用活性炭制作净水器滤芯,是利用活性炭的___________ 性,为降低水的硬度,我们常选择的方法是___________ 。
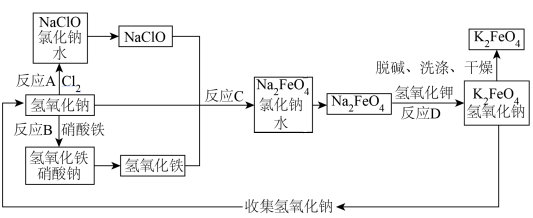
(3)学习净水材料制备。高铁酸钾(K2FeO4)是一种新型非氯高效水处理消毒剂,主要用于饮用水处理,制备高铁酸钾的一种模拟流程如图(部分反应条件未标出):___________ 。
②反应A、B、C、D中属于复分解反应的是___________ 。
③反应A的化学方程式是___________ 。
(1)树立保护水体意识。下列做法正确的有
A.节约用水 B.工业用水重复利用 C.洗衣污水集中处理
(2)掌握水的净化方法。日常生活中,我们常使用活性炭制作净水器滤芯,是利用活性炭的
(3)学习净水材料制备。高铁酸钾(K2FeO4)是一种新型非氯高效水处理消毒剂,主要用于饮用水处理,制备高铁酸钾的一种模拟流程如图(部分反应条件未标出):
②反应A、B、C、D中属于复分解反应的是
③反应A的化学方程式是
您最近一年使用:0次
解题方法
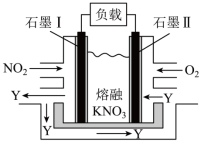
8 . NO2、O2和熔融KNO3可作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y。
(2)写出此燃料电池的负极电极反应式_______ ,从绿色化学角度评价此燃料电池的应用前景_______ 。
| A.石墨Ⅱ为阳极 |
| B.NO2在原电池中为氧化剂 |
| C.Y物质可循环使用 |
| D.电池总反应式为4NO2+O2=2N2O5 |
您最近一年使用:0次
9 . 缺电子化合物是指电子数不符合路易斯结构(路易斯结构是通过共用电子使原子价层电子数达到8,氢原子达到2所形成的稳定分子结构)要求的一类化合物,某科学小组依据 、
、 、
、 分子对此进行研究。
分子对此进行研究。
(1)写出B原子的价层电子轨道表示式_______ 。
(2) 中心原子的轨道杂化类型是
中心原子的轨道杂化类型是_______ ,其_______ (能/不能)提供孤对电子与Fe2+形成配位键。
(3)上述三种化合物中,是缺电子化合物的是_______ 。
(4)NH3分子极易溶于水,是说明理由_______ 。
 、
、 、
、 分子对此进行研究。
分子对此进行研究。(1)写出B原子的价层电子轨道表示式
(2)
 中心原子的轨道杂化类型是
中心原子的轨道杂化类型是(3)上述三种化合物中,是缺电子化合物的是
(4)NH3分子极易溶于水,是说明理由
您最近一年使用:0次
解题方法
10 . 在碳循环中,以 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。
_______ 0(填“>”、“<”或“=”)。从图像分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应,并说明理由______________ 。
 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。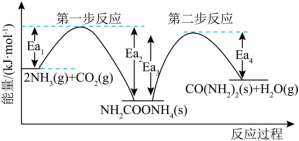

您最近一年使用:0次





