完成下列问题。
(1)一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸中直接加入纯化后的甲醇(CH3OH),同时向一个电极通入空气。
①此电池的正极发生的电极反应为_______ 。
②电解液中H+向_____ 极移动。
(2)如图所示,该装置通电5 min后,电极5的质量增加2.16 g,回答下列问题:____ 极,A池阴极电极反应:______ ,C池阳极电极反应:_______ 。
②如果B槽中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为______ 。
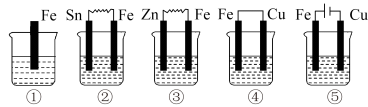
(3)下图各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由大到小的顺序为_____ 。______ 。
(1)一种甲醇燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸中直接加入纯化后的甲醇(CH3OH),同时向一个电极通入空气。
①此电池的正极发生的电极反应为
②电解液中H+向
(2)如图所示,该装置通电5 min后,电极5的质量增加2.16 g,回答下列问题:
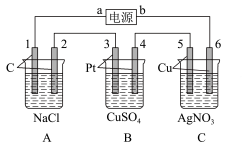
②如果B槽中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
(3)下图各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由大到小的顺序为
更新时间:2024-05-25 10:36:19
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氢能源是最具前景的应用能源之一,氢气的制备和应用是目前的研究热点。回答下列问题:
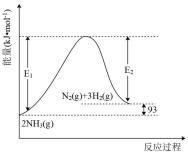
氨气中氢含量高,可通过氨热分解法制氢气。一定温度下,利用催化剂将NH3分解为N2和H2,反应过程中的能量变化如图所示。
(1)已知断开(或形成) 键、
键、 键分别需要吸收(或放出)
键分别需要吸收(或放出)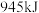 、
、 的热量,则断开
的热量,则断开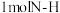 吸收的热量为
吸收的热量为___________ kJ,利用该反应制备标况下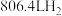 时,吸收的热量为
时,吸收的热量为___________ kJ。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
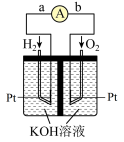
①氢氧燃料电池能量转化的主要形式是___________ ,在导线中电子流动方向为___________ (用a、b表示)。
②负极反应式为___________ 。
(3)电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一、金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I.2Li+H2=2LiH Ⅱ.LiH+H2O=LiOH+H2↑
①反应Ⅰ中的还原剂是___________ ,反应Ⅱ中的氧化剂是___________ 。
②金属锂吸收的氢气与放出的氢气的物质的量之比为___________ 。
氨气中氢含量高,可通过氨热分解法制氢气。一定温度下,利用催化剂将NH3分解为N2和H2,反应过程中的能量变化如图所示。

(1)已知断开(或形成)
 键、
键、 键分别需要吸收(或放出)
键分别需要吸收(或放出)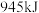 、
、 的热量,则断开
的热量,则断开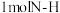 吸收的热量为
吸收的热量为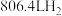 时,吸收的热量为
时,吸收的热量为(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:

①氢氧燃料电池能量转化的主要形式是
②负极反应式为
(3)电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一、金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
I.2Li+H2=2LiH Ⅱ.LiH+H2O=LiOH+H2↑
①反应Ⅰ中的还原剂是
②金属锂吸收的氢气与放出的氢气的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I 给下列有机物用系统命名法命名
(1)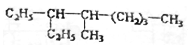
__________________
(2)
__________________
(3)以上两种物质的关系是______________ (填“同系物”或“同分异构体”
II 甲烷的氯代产物是重要的化工原料、有机溶剂
(4)一氯甲烷继续取代直到生成四氯化碳,每一步都是放热反应,因此工厂常采用热交换设备。生成的氯代甲烷在吸收塔中用水吸收,实验室中从混合物中得到氯代甲烷采用的方法是____________ (填操作名称)。根据取代反应中无机产物的性质,对设备的要求要考虑________________
(5)写出葡萄糖在氢氧化钾溶液作电解液条件下的燃料电池的电极反应式:
负极:_________________________________________________________________
正极:_________________________________________________________________
(1)
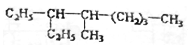
(2)

(3)以上两种物质的关系是
II 甲烷的氯代产物是重要的化工原料、有机溶剂
(4)一氯甲烷继续取代直到生成四氯化碳,每一步都是放热反应,因此工厂常采用热交换设备。生成的氯代甲烷在吸收塔中用水吸收,实验室中从混合物中得到氯代甲烷采用的方法是
(5)写出葡萄糖在氢氧化钾溶液作电解液条件下的燃料电池的电极反应式:
负极:
正极:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示是原电池的装置图。请回答:

(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为___ ;反应进行一段时间后溶液酸性将__ (填“增强”“减弱”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为___ ,B(负极)极材料为__ ,溶液C为___ 。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
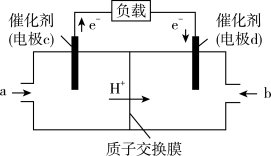
电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是__ (填“正极”或“负极”),c电极的反应方程式为__ 。若线路中转移1mol电子,则上述CH3OH燃料电池消耗的O2在标准状况下的体积为__ L。

(1)若C为稀H2SO4,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C为三种强电解质,它们在水中电离出的离子如下表所示:
图1所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
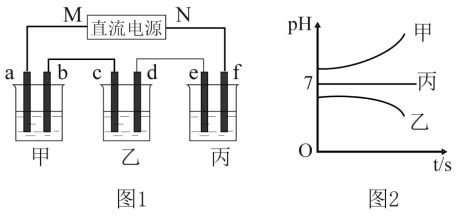
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液的pH与电解时间t的关系如图2所示。据此回答下列问题:
(1)M为电源的___ (填“正”或“负”)极,电极b上发生的电极反应为___ 。
(2)写出乙烧杯中的电池反应方程式:_____ 。
(3)若经过这一段时间后,要使丙恢复到原来的状态,需要进行的操作是___ 。
(4)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe ,A电极材料为Cu,则B电极的电极反应式为______ ;反应进行一段时间后溶液C的pH将______ (填“升高”“降低”或“基本不变”)。
(5)熔盐电池具有高的发电效率,因而受到重视, 可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO -4e-=4CO2,正极反应式为
-4e-=4CO2,正极反应式为___ 。
阳离子 | 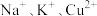 |
阴离子 | 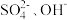 |
图1所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。

接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液的pH与电解时间t的关系如图2所示。据此回答下列问题:
(1)M为电源的
(2)写出乙烧杯中的电池反应方程式:
(3)若经过这一段时间后,要使丙恢复到原来的状态,需要进行的操作是
(4)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe ,A电极材料为Cu,则B电极的电极反应式为

(5)熔盐电池具有高的发电效率,因而受到重视, 可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO
 -4e-=4CO2,正极反应式为
-4e-=4CO2,正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】能源、资源问题是当前人类社会面临的一项重大课题。直接利用物质燃烧提供热能在当今社会仍然占很大比重,但存在利用率低的问题。燃料电池将能量转化效率比直接燃烧效率高,H2、CH4、CH3OH都是重要的能源物质。
(1)其中氢氧燃料电池是常见的燃料电池,如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
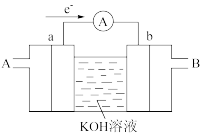
①使用时,空气从_____ 口通入(填“A”或“B”);负极是_____ (填“a”或“b”)。电流由_____ 流向_____ (填“a”或“b”)。其总反应方程式为_____ ,在碱性条件下,负极反应式为_____ 。
②假设使用的“燃料”是甲烷(酸性条件下),a极的电极反应为:_____ 。
(2)某同学设计如图的原电池,负极实验现象为_____ ,则正极的电极反应式为:_____ ,当导线中有3.01×1023个电子流过,溶液质量变化为_____ g。

(3)能把硫酸铜溶液改成氢氧化钠溶液吗_____ (填“能”或“不能”),为什么_____ 。
(1)其中氢氧燃料电池是常见的燃料电池,如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲烷(酸性条件下),a极的电极反应为:
(2)某同学设计如图的原电池,负极实验现象为

(3)能把硫酸铜溶液改成氢氧化钠溶液吗
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
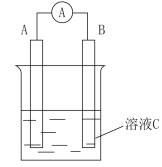
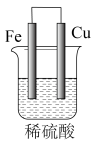
【推荐3】(1)在如图所示的原电池中,___ 是负极,发生___ 反应,正极的现象___ ,电池反应的化学方程式为___ 。
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为CH4+2O2+2KOH═K2CO3+3H2O。

①实验测得OH-定向移向B电极,则___ 处电极入口通甲烷(填A或B)。
②当消耗甲烷的体积为33.6L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为___ 。
(3)如用电解法精炼粗铜,电解液c选用CuSO4溶液,则:
①A电极的材料是___ ,电极反应式是___ ;
②B电极的材料是__ ,电极反应式是___ 。
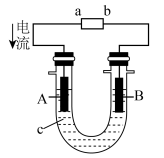

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为CH4+2O2+2KOH═K2CO3+3H2O。

①实验测得OH-定向移向B电极,则
②当消耗甲烷的体积为33.6L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为
(3)如用电解法精炼粗铜,电解液c选用CuSO4溶液,则:
①A电极的材料是
②B电极的材料是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电解原理在化学工业中有广泛的应用。如图所示为一电解池装置,U形管内装有电解液c,A、B是两块电极板,通过导线与直流电源相连。
(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试剂,试判断:
①a电极是_____ 极(填“正”或“负”),B电极是_____ 极(填“阴”或“阳”);
②A电极产生的气体为________ ,B电极上的电极反应式为______________ ;
③检验A电极上产物的方法是:_________________ 。
(2)若图示装置为用惰性电极电解CuSO4溶液的装置,其中阴极上析出Cu的质量为3.2 g,常温下,若将电解后的溶液稀释至1 L,则溶液的pH约为________ 。
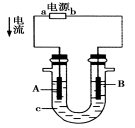
(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试剂,试判断:
①a电极是
②A电极产生的气体为
③检验A电极上产物的方法是:
(2)若图示装置为用惰性电极电解CuSO4溶液的装置,其中阴极上析出Cu的质量为3.2 g,常温下,若将电解后的溶液稀释至1 L,则溶液的pH约为
您最近一年使用:0次
【推荐2】铅的单质、氧化物、盐在现代工业中有着重要用途。
I.
(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,Pb3O4与HNO3发生非氧化还原反应生成一种盐和一种铅氧化物,其反应的化学方程式为_______ 。
II.以含铅废料(主要含Pb、PbO、PbO2、PbSO4)为原料制备高纯PbO,其主要流程如下:
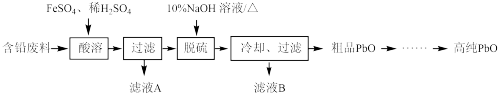
(2)“酸溶”时,在Fe2+催化下,Pb和PbO2反应生成PbSO4生成1molPbSO4转移电子的物质的量为_______ mol,写出两条增大酸溶速率的措施_______
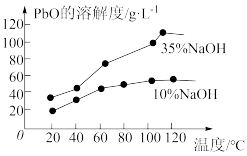
(3)已知:①PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)⇌NaHPbO2(aq),其溶解度曲线如图所示:
②粗品PbO中所含杂质不溶于NaOH溶液。
结合上述信息,完成由粗品PbO得到高纯PbO的操作:将粗品PbO溶解在一定量_____ (填“35%”或“10%”)的NaOH溶液中,加热至110℃,充分溶解后,____ (填“趁热过滤”或“蒸发浓缩”),将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO固体。
(4)将PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl2的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
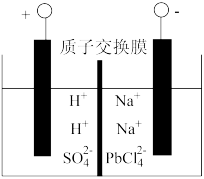
①阴极的电极反应式为_______ 。
②电解一段时间后,Na2PbCl4浓度极大减小,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是_______ 。
I.
(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,Pb3O4与HNO3发生非氧化还原反应生成一种盐和一种铅氧化物,其反应的化学方程式为
II.以含铅废料(主要含Pb、PbO、PbO2、PbSO4)为原料制备高纯PbO,其主要流程如下:

(2)“酸溶”时,在Fe2+催化下,Pb和PbO2反应生成PbSO4生成1molPbSO4转移电子的物质的量为
(3)已知:①PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)⇌NaHPbO2(aq),其溶解度曲线如图所示:

②粗品PbO中所含杂质不溶于NaOH溶液。
结合上述信息,完成由粗品PbO得到高纯PbO的操作:将粗品PbO溶解在一定量
(4)将PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl2的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①阴极的电极反应式为
②电解一段时间后,Na2PbCl4浓度极大减小,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如下图所示,回答下列问题:

(1)该装置中B电极为电解池的___________ 极(填“阴”或“阳”);
(2)A电极上的电极反应式为______________________________________ ;
电解池总反应的离子方程式为___________________________________ ;
(3)电解过程中,电解质溶液的酸性______ (填“增强”、“减弱”或“不变”);
(4)下列实验操作中必要的是_________ (填写字母);
(5)铜的相对原子质量为________________ (用带有m、V的计算式表示)。

(1)该装置中B电极为电解池的
(2)A电极上的电极反应式为
电解池总反应的离子方程式为
(3)电解过程中,电解质溶液的酸性
(4)下列实验操作中必要的是
| A.称量电解前的电极的质量; |
| B.电解后,电极在烘干称量前,必须用蒸馏水冲洗; |
| C.刮下电解后电极上析出的铜,并清洗,称量; |
| D.电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行; |
E.在有空气存在的情况下,烘干电极必须用低温烘干的方法。
(5)铜的相对原子质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】研究和开发海水及其综合利用关系到人类的可持续发展。甲、乙两实验小组分别探索从海水中制取金属镁和单质溴的实验。
(1)甲实验小组的流程如图1。
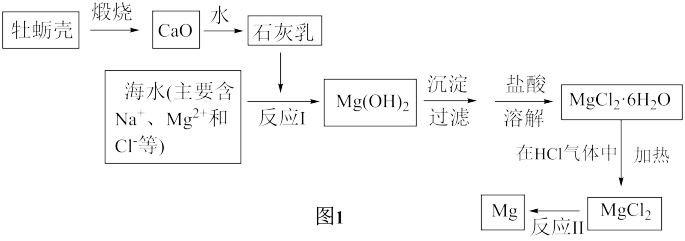
①制备石灰乳的化学反应方程式是___ 、___ 。
②写出反应Ⅰ的离子反应方程式___ 。
③反应Ⅱ是工业冶炼金属镁的反应原理,写出反应Ⅱ的化学反应方程式___ 。
(2)乙实验小组的流程如图2。

①分液漏斗使用前需检漏,检漏的方法为___ ,在步骤③中,萃取后分液漏斗内观察到的现象是___ 。
②写出步骤①发生反应的离子方程式___ ;写出步骤②发生反应的化学方程式___ 。
③在步骤③中,分离出溴单质的实验操作的名称是分液和___ ,后一实验操作用到的玻璃仪器有:___ 。
④在步骤①和步骤②之间设计了通入空气和水蒸气吹出的操作步骤的目的是___ 。
(3)图3各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为___ 。(填序号)

(1)甲实验小组的流程如图1。

①制备石灰乳的化学反应方程式是
②写出反应Ⅰ的离子反应方程式
③反应Ⅱ是工业冶炼金属镁的反应原理,写出反应Ⅱ的化学反应方程式
(2)乙实验小组的流程如图2。

①分液漏斗使用前需检漏,检漏的方法为
②写出步骤①发生反应的离子方程式
③在步骤③中,分离出溴单质的实验操作的名称是分液和
④在步骤①和步骤②之间设计了通入空气和水蒸气吹出的操作步骤的目的是
(3)图3各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】本题为《化学与生活(选修1)》选做题
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是_______ ;
②人体内最重要的供能物质是________ ;
③具有解热镇痛作用,用于治疗感冒的是_______ ;
④对支气管哮喘症有明显疗效的是_________ 。
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是________ ;
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为_________ ;
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的_______ 。
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是_________ ;
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是______ ;
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是_____________ 。
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是
②人体内最重要的供能物质是
③具有解热镇痛作用,用于治疗感冒的是
④对支气管哮喘症有明显疗效的是
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质是
A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为
A.O2+2H2O + 4e- = 4OH- B.Fe - 2e -= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的
A.锌块 B.铜块
(3)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确
的是
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池
您最近一年使用:0次