电解原理在化学工业中有广泛的应用。如图所示为一电解池装置,U形管内装有电解液c,A、B是两块电极板,通过导线与直流电源相连。
(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试剂,试判断:
①a电极是_____ 极(填“正”或“负”),B电极是_____ 极(填“阴”或“阳”);
②A电极产生的气体为________ ,B电极上的电极反应式为______________ ;
③检验A电极上产物的方法是:_________________ 。
(2)若图示装置为用惰性电极电解CuSO4溶液的装置,其中阴极上析出Cu的质量为3.2 g,常温下,若将电解后的溶液稀释至1 L,则溶液的pH约为________ 。
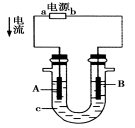
(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试剂,试判断:
①a电极是
②A电极产生的气体为
③检验A电极上产物的方法是:
(2)若图示装置为用惰性电极电解CuSO4溶液的装置,其中阴极上析出Cu的质量为3.2 g,常温下,若将电解后的溶液稀释至1 L,则溶液的pH约为
更新时间:2019-01-04 13:07:42
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】工业上可用电解法来处理含Cr2O72-的酸性废水,最终可将Cr2O72-转化成Cr(OH)3沉淀而将其除去。如图为电解装置示意图(电极材料分别为铁和石墨)。

请回答:
(1)装置中的b电极是________ (填“阳极”或“阴极”)。
(2)a电极的电极反应式是__ 。
(3)完成b电极附近溶液中所发生反应的离子方程式:Cr2O72-+6Fe2++14H+=2________+6________+7________。____________
(4)电解时用铁作阳极而不用石墨作阳极的原因是____________________________ 。
(5)电解结束后,若要检验电解液中是否还有Fe2+存在,则可选用的试剂是________ (填字母)。
A.KSCN溶液 B.CuCl2溶液 C.H2O2溶液 D.K3[Fe(CN)6]溶液

请回答:
(1)装置中的b电极是
(2)a电极的电极反应式是
(3)完成b电极附近溶液中所发生反应的离子方程式:Cr2O72-+6Fe2++14H+=2________+6________+7________。
(4)电解时用铁作阳极而不用石墨作阳极的原因是
(5)电解结束后,若要检验电解液中是否还有Fe2+存在,则可选用的试剂是
A.KSCN溶液 B.CuCl2溶液 C.H2O2溶液 D.K3[Fe(CN)6]溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺节能超过30%。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子交换膜都只允许阳离子通过

(1)图中物质X的电子式_______ ,B燃料电池中Na+的移动方向_______ (“从左到右”或“从右到左”)。
(2)分析、比较图中a%_______ b%(填“<”或“>”或“=”),原因是_______ 。
(3)A电解池中产生Y的电极方程式_______ 。
(4)写出该新工艺的总方程式_______ 。

(1)图中物质X的电子式
(2)分析、比较图中a%
(3)A电解池中产生Y的电极方程式
(4)写出该新工艺的总方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等化工产品。如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
回答下列问题:

(1)写出电解饱和食盐水的离子方程式:_______________________________ 。
(2)离子交换膜的作用为_________________ 。
(3)精制饱和食盐水从图中____ (填“a”、“b”、“c”或“d”,下同)位置补充,氢氧化钠溶液从图中____ 位置流出。
(4)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式:____________________________ 。
回答下列问题:

(1)写出电解饱和食盐水的离子方程式:
(2)离子交换膜的作用为
(3)精制饱和食盐水从图中
(4)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。
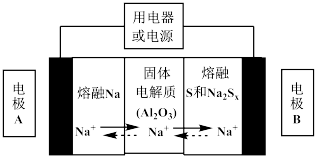
(1)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:
①根据上右表数据,请你判断该电池工作的适宜应控制在_________ (填字母)范围内。
a.100℃以下 b.100~300℃ c.300~350℃ d.350~2050℃
②放电时,电极A为_________ 极,电极B发生_________ 反应(填“氧化或还原”)
③充电时,总反应为Na2SX=2Na+xS(3<x<5),则阳极的电极反应式为:________________ 。
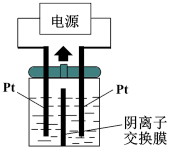
(2)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:___________ ;试分析左侧溶液蓝色逐渐变浅的可能原因是:___________ 。
(3)若把钠硫电池作为电源,按如图所示装置进行实验电解乙池和丙池:
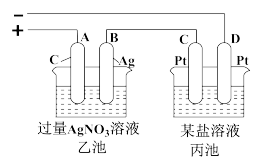
当钠硫电池中消耗0.05xmol的S时,理论上乙池中B极的质量增加__________ g;此时丙装置中___________ (填“C”或“D”)电极析出7.20g金属,则丙装置中的某盐溶液可能是_______ (填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(1)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:

①根据上右表数据,请你判断该电池工作的适宜应控制在
| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
a.100℃以下 b.100~300℃ c.300~350℃ d.350~2050℃
②放电时,电极A为
③充电时,总反应为Na2SX=2Na+xS(3<x<5),则阳极的电极反应式为:

(2)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:
(3)若把钠硫电池作为电源,按如图所示装置进行实验电解乙池和丙池:

当钠硫电池中消耗0.05xmol的S时,理论上乙池中B极的质量增加
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)25℃,吸收液 溶液在吸收
溶液在吸收 的过程中,pH随
的过程中,pH随 :
: 变化关系如下表:
变化关系如下表:
①当吸收液呈中性时,溶液中离子浓度关系正确的是:______  选填字母
选填字母
A.
B.
C.
②当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:
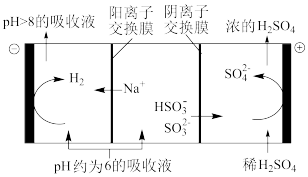
请写出 在阳极放电的电极反应式是
在阳极放电的电极反应式是______ .
 已知:
已知: ;
; ;
; ,常温下,取体积比4:1的甲烷和氢气的混合气体
,常温下,取体积比4:1的甲烷和氢气的混合气体 标况
标况 ,经完全燃烧恢复常温,放出的热为
,经完全燃烧恢复常温,放出的热为______ .
 溶液在吸收
溶液在吸收 的过程中,pH随
的过程中,pH随 :
: 变化关系如下表:
变化关系如下表: : : | 91:9 | 1:1 | 1:91 |
| pH |  |  |  |
①当吸收液呈中性时,溶液中离子浓度关系正确的是:
 选填字母
选填字母
A.

B.

C.

②当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:

请写出
 在阳极放电的电极反应式是
在阳极放电的电极反应式是 已知:
已知: ;
; ;
; ,常温下,取体积比4:1的甲烷和氢气的混合气体
,常温下,取体积比4:1的甲烷和氢气的混合气体 标况
标况 ,经完全燃烧恢复常温,放出的热为
,经完全燃烧恢复常温,放出的热为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】应用电化学原理,回答下列问题:

(1)上述三个装置中,负极反应物化学性质上的共同特点是___________ 。
(2)甲中电流计指针偏移时,盐桥(装有含琼脂的KCl饱和溶液)中离子移动的方向是___________ 。
(3)乙中正极反应式为___________ ;若将H2换成CH4,则负极反应式为___________ 。
(4)丙中铅蓄电池放电一段时间后,进行充电时,阴极的电极反应式是___________ 。

(1)上述三个装置中,负极反应物化学性质上的共同特点是
(2)甲中电流计指针偏移时,盐桥(装有含琼脂的KCl饱和溶液)中离子移动的方向是
(3)乙中正极反应式为
(4)丙中铅蓄电池放电一段时间后,进行充电时,阴极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电解原理在化学工业中有广泛应用。图中表示一个电解池,装有电解液C;A、B是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
①B是_____ 极(填“阴”或“阳”) ,B极逸出_____ (填“黄绿色”或“无色”)气体,同时B极附近溶液呈________ 色。
②电解池中A极上的电极反应式为________ ,B极上的电极反应式为______ 。
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
①A电极的材料是_________ ,电极反应式是____________ 。
② B电极的材料是_________ ,电极反应式是_________ 。
(说明:杂质发生的电极反应不必写出)
③下列说法正确的是________ 。
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)用惰性电极电解足量的CuSO4溶液。若阴极析出Cu的质量为12.8g,则阳极上产生的气体在标准状况下的体积为________ L。

(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
①B是
②电解池中A极上的电极反应式为
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
①A电极的材料是
② B电极的材料是
(说明:杂质发生的电极反应不必写出)
③下列说法正确的是
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)用惰性电极电解足量的CuSO4溶液。若阴极析出Cu的质量为12.8g,则阳极上产生的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,U形管内盛有100 mL的溶液,按要求回答下列问题:
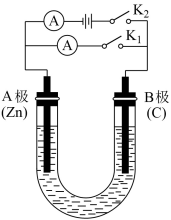
(1)断开K2,闭合K1,若所盛溶液为CuSO4溶液,则A极为___________ 极,B极的电极反应式为___________ 。若所盛溶液为KCl溶液,则B极的电极反应式为___________ 。
(2)断开K1,闭合K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可以观察到的现象是___________ 。
②B电极上的电极反应式为___________ ,总反应的化学方程式是___________ 。
③反应一段时间后断开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2 mL,将溶液充分混合,溶液的pH约为___________ 。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的___________ 。

(1)断开K2,闭合K1,若所盛溶液为CuSO4溶液,则A极为
(2)断开K1,闭合K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可以观察到的现象是
②B电极上的电极反应式为
③反应一段时间后断开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2 mL,将溶液充分混合,溶液的pH约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图装置所示,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:
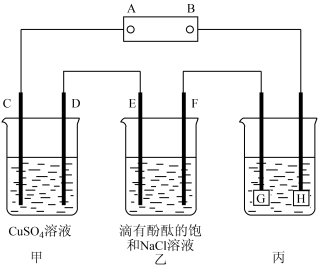
(1)B极是电源的_______ 极(填“正”或“负”)。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为________ 。
(3)现用丙装置给铜件镀银,则H应该是________ (填“镀层金属”或“镀件”),电镀液是_____ 溶液。当乙中溶液的c(OH-)=0.1 mol·L-1时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________ ,甲中溶液的pH________ (填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是____________ 。

(1)B极是电源的
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应该是
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是
您最近一年使用:0次



