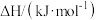在碳循环中,以 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。
_______ 0(填“>”、“<”或“=”)。从图像分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应,并说明理由______________ 。
 为原料生产尿素的反应历程与能量变化示意图如图所示。
为原料生产尿素的反应历程与能量变化示意图如图所示。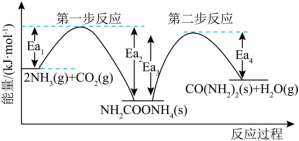

更新时间:2024-05-09 17:27:09
|
相似题推荐
【推荐1】铁触媒催化合成氨经历下图所示①⑧步基元反应(从状态I至状态Ⅶ):
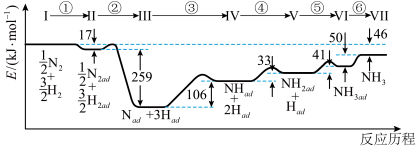
上图中“ad”表示吸附在催化剂表面的物质。完成下列问题:
(1)催化反应往往经过物质在催化剂表面的“吸附”过程和脱离催化剂表面的“脱附”过程。其中,“吸附”过程是上图中的第________ 步基元反应,“脱附”过程是_________ (填“吸热”或“放热”)过程。
(2)根据上图计算合成氨反应的焓变: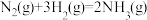 △H=
△H=___________ 。

上图中“ad”表示吸附在催化剂表面的物质。完成下列问题:
(1)催化反应往往经过物质在催化剂表面的“吸附”过程和脱离催化剂表面的“脱附”过程。其中,“吸附”过程是上图中的第
(2)根据上图计算合成氨反应的焓变:
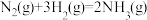 △H=
△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】CH3OH 是一种无色有刺激性气味的液体,在生产生活中有重要用途。
Ⅰ.目前工业上有一种方法是用 CO2生产燃料甲醇。一定条件下发生反应:CO2(g) +3H2(g)=CH3OH(g)+H2O(g),该反应的能量变化如图所示:
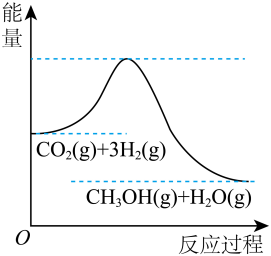
(1)你认为该反应为_____ (填放热或吸热)反应.
(2)恒容容器中,对于以上反应,能加快反应速率的是_____ 。
a.升高温度 b.充入 He c.加入催化剂 d.降低压强
Ⅱ. CH3OH 也是一种重要的燃料,一定条件下发生反应:
2CH3OH(g)+3O2(g) =2 CO2(g)+4H2O(g)。
(3)某温度下,将 4mol CH3OH 和 6 mol O2充入 2 L 的密闭容器中经过 4 min 反应达到平衡,测得 c(O2)=1.5mol·L-1,4 min 内平均反应速率 υ(H2O)=_____ 。
(4)CH3OH 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是_____ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗 6.4 g CH3OH 转移 1.2 mol 电子
(5)以 CH3OH、空气(氧气)、氢氧化钾溶液为原料,石墨为电极构成燃料电池,该电池中负极上的电极反应式是:____________________________ 。
Ⅰ.目前工业上有一种方法是用 CO2生产燃料甲醇。一定条件下发生反应:CO2(g) +3H2(g)=CH3OH(g)+H2O(g),该反应的能量变化如图所示:

(1)你认为该反应为
(2)恒容容器中,对于以上反应,能加快反应速率的是
a.升高温度 b.充入 He c.加入催化剂 d.降低压强
Ⅱ. CH3OH 也是一种重要的燃料,一定条件下发生反应:
2CH3OH(g)+3O2(g) =2 CO2(g)+4H2O(g)。
(3)某温度下,将 4mol CH3OH 和 6 mol O2充入 2 L 的密闭容器中经过 4 min 反应达到平衡,测得 c(O2)=1.5mol·L-1,4 min 内平均反应速率 υ(H2O)=
(4)CH3OH 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗 6.4 g CH3OH 转移 1.2 mol 电子
(5)以 CH3OH、空气(氧气)、氢氧化钾溶液为原料,石墨为电极构成燃料电池,该电池中负极上的电极反应式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学反应总是伴随着能量的转化,给世界带来了生机和光明。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等多种作用。
①制作冷敷袋可以利用___________ 。(填字母)
a.放热的化学变化 b.吸热的化学变化 c.放热的物理变化 d.吸热的物理变化
②某品牌冷敷袋是利用十水合碳酸钠( )与硝酸铵在一定条件下反应起作用的,该反应过程中有两种气体产生。反应的化学方程式为
)与硝酸铵在一定条件下反应起作用的,该反应过程中有两种气体产生。反应的化学方程式为___________ 。该冷敷袋的缺点是___________ 。
(2)市场出现的“暖贴”中主要成分是铁粉、炭粉、少量氯化钠和水等,“暖贴”用塑料袋密封,使用时从塑料袋中取出轻轻揉搓就会释放热量,用完后袋内有大量铁锈生成。
①“暖贴”中炭粉的作用是___________ 。
②产生大量铁锈的主要原因是___________ 。
(3)氢能是发展中的新能源,与汽油相比, 作为燃料的优点是
作为燃料的优点是___________ 。 直接燃烧的能量转换率
直接燃烧的能量转换率___________ (填写“高于”或“等于”或“低于”)燃料电池。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等多种作用。
①制作冷敷袋可以利用
a.放热的化学变化 b.吸热的化学变化 c.放热的物理变化 d.吸热的物理变化
②某品牌冷敷袋是利用十水合碳酸钠(
 )与硝酸铵在一定条件下反应起作用的,该反应过程中有两种气体产生。反应的化学方程式为
)与硝酸铵在一定条件下反应起作用的,该反应过程中有两种气体产生。反应的化学方程式为(2)市场出现的“暖贴”中主要成分是铁粉、炭粉、少量氯化钠和水等,“暖贴”用塑料袋密封,使用时从塑料袋中取出轻轻揉搓就会释放热量,用完后袋内有大量铁锈生成。
①“暖贴”中炭粉的作用是
②产生大量铁锈的主要原因是
(3)氢能是发展中的新能源,与汽油相比,
 作为燃料的优点是
作为燃料的优点是 直接燃烧的能量转换率
直接燃烧的能量转换率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】将二氧化碳资源化是实现“碳中和”目标的重要手段。回答下列问题:
利用 和重整技术可获得合成气(主要成分为CO和
和重整技术可获得合成气(主要成分为CO和 ),反应如下:
),反应如下:
I:

Ⅱ:
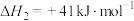
反应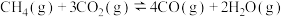 的
的
___________  ,该反应活化能
,该反应活化能 (正)
(正)___________  (逆)(填“>”“<”或“=”)。
(逆)(填“>”“<”或“=”)。
利用
 和重整技术可获得合成气(主要成分为CO和
和重整技术可获得合成气(主要成分为CO和 ),反应如下:
),反应如下:I:


Ⅱ:

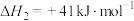
反应
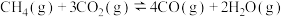 的
的
 ,该反应活化能
,该反应活化能 (正)
(正) (逆)(填“>”“<”或“=”)。
(逆)(填“>”“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在等压下化学反应所吸收或放出的热量,称为化学反应的焓变。回答下列问题:
(1)25℃、101kPa时,1g氨气完全燃烧放出18.6kJ的热量,则 △H=
△H=_______ kJ∙mol-1。
(2) 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。
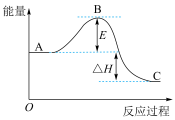
已知:0.5molSO2(g)被氧化为0.5molSO3(g)的△H=-49.5 kJ∙mol-1。则:
①E的大小对该反应的反应热_______ (填“有”或“无”)影响;该反应通常用V2O5作催化剂,加V2O5会使图中B点_______ (填“升高”或“降低”)。
②SO2氧化为SO3的热化学方程式为_______ 。
(3)已知: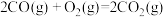 △H=-566 kJ∙mol-1 ①
△H=-566 kJ∙mol-1 ①
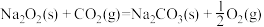 △H=-226 kJ∙mol-1②
△H=-226 kJ∙mol-1②
则CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数目为_______ 。
(4)常压下,某铝热反应的温度与能量变化如图所示:
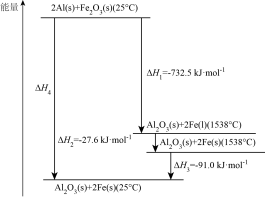
①101.3kPa、1538℃, △H=
△H=_______ kJ∙mol-1。
②101.3kPa、25℃时,该铝热反应的热化学方程式为_______ 。
(1)25℃、101kPa时,1g氨气完全燃烧放出18.6kJ的热量,则
 △H=
△H=(2)
 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。
已知:0.5molSO2(g)被氧化为0.5molSO3(g)的△H=-49.5 kJ∙mol-1。则:
①E的大小对该反应的反应热
②SO2氧化为SO3的热化学方程式为
(3)已知:
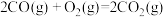 △H=-566 kJ∙mol-1 ①
△H=-566 kJ∙mol-1 ①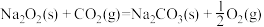 △H=-226 kJ∙mol-1②
△H=-226 kJ∙mol-1②则CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数目为
(4)常压下,某铝热反应的温度与能量变化如图所示:

①101.3kPa、1538℃,
 △H=
△H=②101.3kPa、25℃时,该铝热反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】碳和氮的氢化物是广泛的化工原料,回答下列问题:
(1)工业上合成氨的反应为
 ,反应过程中能量变化如图所示。
,反应过程中能量变化如图所示。
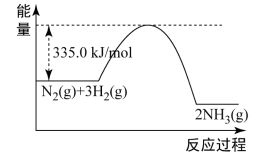
①反应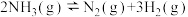 的活化能为
的活化能为________ kJ/mol,有利于该反应自发进行的条件是_________ 。
②合成氨时加入铁粉可以加快生成 的速率,在上图中画出加入铁粉后的能量变化曲线
的速率,在上图中画出加入铁粉后的能量变化曲线_______ 。
(2)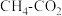 催化重整不仅可以得到合成气(CO和
催化重整不仅可以得到合成气(CO和 ),还对温室气体的减排具有重要意义。回答下列问题:
),还对温室气体的减排具有重要意义。回答下列问题:
①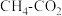 催化重整反应为
催化重整反应为
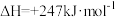 。某温度下,在体积为2L的容器中加入2mol
。某温度下,在体积为2L的容器中加入2mol 、1mol
、1mol 以及催化剂进行重整反应,5min达到平衡时
以及催化剂进行重整反应,5min达到平衡时 的转化率是50%。0-5min平均反应速率
的转化率是50%。0-5min平均反应速率
_________ 
②反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如表:
由上表判断,催化剂X______ Y(填“优于”或“劣于”),理由是____________________ 。
(1)工业上合成氨的反应为

 ,反应过程中能量变化如图所示。
,反应过程中能量变化如图所示。
①反应
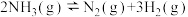 的活化能为
的活化能为②合成氨时加入铁粉可以加快生成
 的速率,在上图中画出加入铁粉后的能量变化曲线
的速率,在上图中画出加入铁粉后的能量变化曲线(2)
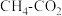 催化重整不仅可以得到合成气(CO和
催化重整不仅可以得到合成气(CO和 ),还对温室气体的减排具有重要意义。回答下列问题:
),还对温室气体的减排具有重要意义。回答下列问题:①
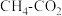 催化重整反应为
催化重整反应为
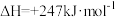 。某温度下,在体积为2L的容器中加入2mol
。某温度下,在体积为2L的容器中加入2mol 、1mol
、1mol 以及催化剂进行重整反应,5min达到平衡时
以及催化剂进行重整反应,5min达到平衡时 的转化率是50%。0-5min平均反应速率
的转化率是50%。0-5min平均反应速率

②反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如表:
积碳反应 | 消碳反应 | ||
| 75 | 172 | |
活化能/( | 催化剂X | 33 | 91 |
催化剂Y | 43 | 72 | |
由上表判断,催化剂X
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Burns和Dainton研究了反应Cl2(g)+CO(g) COCl2(g)的动力学,获得其速率方程v=k[c(Cl2)]3/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。
COCl2(g)的动力学,获得其速率方程v=k[c(Cl2)]3/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。
(1)该反应可认为经过以下反应历程:
第一步:Cl2 2Cl 快速平衡
2Cl 快速平衡
第二步:Cl+CO COCl 快速平衡
COCl 快速平衡
第三步:COCl+Cl2→COCl2+Cl 慢反应
下列表述正确的是______(填标号)。
(2)在某温度下进行实验,测得各组分初浓度和反应初速度如下:
CO的反应级数m=______ ,当实验4进行到某时刻,测得c(Cl2)=0.010mol·L-1,则此时的反应速率v=______ mol·L-1·s-1(已知: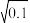 ≈0.32)。
≈0.32)。
 COCl2(g)的动力学,获得其速率方程v=k[c(Cl2)]3/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。
COCl2(g)的动力学,获得其速率方程v=k[c(Cl2)]3/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。(1)该反应可认为经过以下反应历程:
第一步:Cl2
 2Cl 快速平衡
2Cl 快速平衡第二步:Cl+CO
 COCl 快速平衡
COCl 快速平衡第三步:COCl+Cl2→COCl2+Cl 慢反应
下列表述正确的是______(填标号)。
| A.COCl属于反应的中间产物 |
| B.第一步和第二步的活化能较高 |
| C.决定总反应快慢的是第三步 |
| D.第三步的有效碰撞频率较大 |
| 实验序号 | c(Cl2)/mol·L-1 | c(CO)/mol·L-1 | v/mol·L-1·s-1 |
| 1 | 0.100 | 0.100 | 1.2×10-2 |
| 2 | 0.050 | 0.100 | 4.26×10-3 |
| 3 | 0.100 | 0.200 | 2.4×10-2 |
| 4 | 0.050 | 0.050 | 2.13×10-3 |
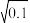 ≈0.32)。
≈0.32)。
您最近一年使用:0次
填空题
|
适中
(0.65)
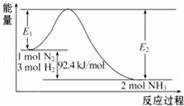
【推荐2】科学家一直致力于“人工固氮”的方法研究.用N2和H2合成NH3的能量变化如图所示。
(1)合成氨反应的热化学方程式_________________________ ,已知E2=212.4kJ/mol,则该反应正反应的活化能是______ 。
(2)反应体系中加入催化剂,反应速率______ ,E2的变化是______ 。(填“增大”、“减小”或“不变”)
(3)工业上常采用高温高压,使用催化剂的方法改变该反应的反应速率,在甲乙两个体积均为2L固定容积的密闭容器中,分别充入1molN2、3molH2和1molN2、3molH2、1molHe,反应速率甲__ 乙(填大于、小于或等于)。
(4)该反应的△S______ 0,(填大于、小于或等于),理论上在______ 条件下可以自发。
(1)合成氨反应的热化学方程式
(2)反应体系中加入催化剂,反应速率
(3)工业上常采用高温高压,使用催化剂的方法改变该反应的反应速率,在甲乙两个体积均为2L固定容积的密闭容器中,分别充入1molN2、3molH2和1molN2、3molH2、1molHe,反应速率甲
(4)该反应的△S
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)以NH3、CO2为原料生产重要的高效氮肥——尿素[CO(NH2)2],涉及反应的反应过程中能量变化示意图如图1所示:
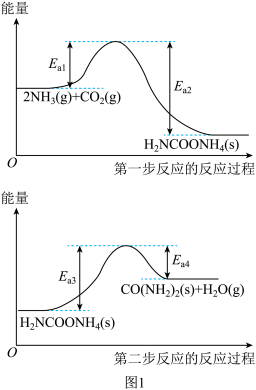
写出第一步反应的热化学方程式:_____ 。已知两步反应中第二步反应是生产尿素的决速步骤,可判断Ea1_____ (填“>”“<”或“=”)Ea3。
(2)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程,部分历程如图2所示,其中吸附在催化剂表面的物种用*标注。
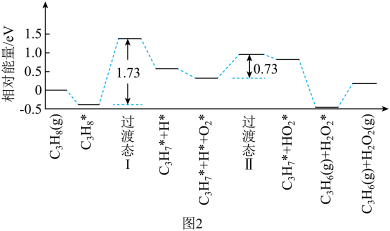
①该历程中决速步骤能垒(活化能)为_____ eV。
②该历程中最低能垒对应步骤的化学方程式为_____ 。
③该历程之后可能发生反应的化学方程式为_____ 。
(1)以NH3、CO2为原料生产重要的高效氮肥——尿素[CO(NH2)2],涉及反应的反应过程中能量变化示意图如图1所示:

写出第一步反应的热化学方程式:
(2)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程,部分历程如图2所示,其中吸附在催化剂表面的物种用*标注。

①该历程中决速步骤能垒(活化能)为
②该历程中最低能垒对应步骤的化学方程式为
③该历程之后可能发生反应的化学方程式为
您最近一年使用:0次