科学家一直致力于“人工固氮”的方法研究.用N2和H2合成NH3的能量变化如图所示。
(1)合成氨反应的热化学方程式_________________________ ,已知E2=212.4kJ/mol,则该反应正反应的活化能是______ 。
(2)反应体系中加入催化剂,反应速率______ ,E2的变化是______ 。(填“增大”、“减小”或“不变”)
(3)工业上常采用高温高压,使用催化剂的方法改变该反应的反应速率,在甲乙两个体积均为2L固定容积的密闭容器中,分别充入1molN2、3molH2和1molN2、3molH2、1molHe,反应速率甲__ 乙(填大于、小于或等于)。
(4)该反应的△S______ 0,(填大于、小于或等于),理论上在______ 条件下可以自发。
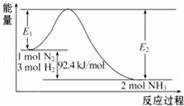
(1)合成氨反应的热化学方程式
(2)反应体系中加入催化剂,反应速率
(3)工业上常采用高温高压,使用催化剂的方法改变该反应的反应速率,在甲乙两个体积均为2L固定容积的密闭容器中,分别充入1molN2、3molH2和1molN2、3molH2、1molHe,反应速率甲
(4)该反应的△S
更新时间:2018-12-27 09:12:07
|
相似题推荐
【推荐1】汽车发动机代用燃料包括乙醇、氢气和甲烷等。回答下列问题:
(1)在25℃、 下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量
下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量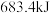 ,则乙醇燃烧热的热化学方程式为
,则乙醇燃烧热的热化学方程式为_______ 。
(2)根据图甲中的能量关系,可求得 键的键能为
键的键能为_______  。
。
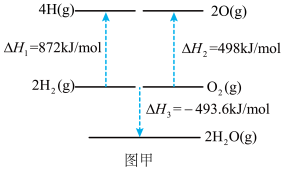
(3)甲烷完全燃烧反应的能量关系如图乙所示。

①

_______ (用含 和
和 的关系式表示)
的关系式表示)
②为提高燃料利用率,加入甲烷燃烧的催化剂,则
_______ (填“变大”、“变小”或“不变”,下同),该反应的 =
=_______ 。
(4)已知氢气的燃烧热为 ,甲烷的燃烧热为
,甲烷的燃烧热为 ,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点
,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点_______ ,_______ 。
(1)在25℃、
 下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量
下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量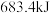 ,则乙醇燃烧热的热化学方程式为
,则乙醇燃烧热的热化学方程式为(2)根据图甲中的能量关系,可求得
 键的键能为
键的键能为 。
。
(3)甲烷完全燃烧反应的能量关系如图乙所示。

①


 和
和 的关系式表示)
的关系式表示)②为提高燃料利用率,加入甲烷燃烧的催化剂,则

 =
=(4)已知氢气的燃烧热为
 ,甲烷的燃烧热为
,甲烷的燃烧热为 ,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点
,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】我国科学家对甲烷和水蒸气催化重整反应机理进行了广泛研究,通常认为该反应分两步进行。第一步:CH4催化裂解生成H2和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如CH4→Cads/[C(H)n]ads+(2- )H2;第二步:碳(或碳氢物种)和H2O反应生成CO2和H2,如Cads/[C(H)n]ads+2H2O→CO2+(2+
)H2;第二步:碳(或碳氢物种)和H2O反应生成CO2和H2,如Cads/[C(H)n]ads+2H2O→CO2+(2+ )H2。反应过程和能量变化残图如下(过程①没有加催化剂,过程②加入催化剂),过程①和②ΔH的关系为①
)H2。反应过程和能量变化残图如下(过程①没有加催化剂,过程②加入催化剂),过程①和②ΔH的关系为①___________ ②(填“>”“<”或“=”);控制整个过程②反应速率的是第___________ 步(填“Ⅰ”或“Ⅱ”),其原因为___________

 )H2;第二步:碳(或碳氢物种)和H2O反应生成CO2和H2,如Cads/[C(H)n]ads+2H2O→CO2+(2+
)H2;第二步:碳(或碳氢物种)和H2O反应生成CO2和H2,如Cads/[C(H)n]ads+2H2O→CO2+(2+ )H2。反应过程和能量变化残图如下(过程①没有加催化剂,过程②加入催化剂),过程①和②ΔH的关系为①
)H2。反应过程和能量变化残图如下(过程①没有加催化剂,过程②加入催化剂),过程①和②ΔH的关系为①
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化石燃料燃烧时会产生 SO2进入大气,有多种方法可用于 SO2的脱除。
(1)NaClO 碱性溶液吸收法。工业上可用 NaClO 碱性溶液吸收SO2。
①反应离子方程式是__________________________________________ 。
②为了提高吸收效率,常用 Ni2O3作为催化剂。在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对SO2的吸收。该催化过程的示意图如图所示:
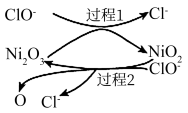
a.过程1的离子方程式是Ni2O3+ClO- =2NiO2 +Cl-,则过程2的离子方程式____________ 。
b.Ca(ClO)2也可用于脱硫,且脱硫效果比NaClO更好,原因是________________ 。
(2)碘循环工艺也能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下:
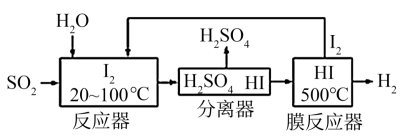
则碘循环工艺的总反应为:___________________________________________ 。
(1)NaClO 碱性溶液吸收法。工业上可用 NaClO 碱性溶液吸收SO2。
①反应离子方程式是
②为了提高吸收效率,常用 Ni2O3作为催化剂。在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对SO2的吸收。该催化过程的示意图如图所示:

a.过程1的离子方程式是Ni2O3+ClO- =2NiO2 +Cl-,则过程2的离子方程式
b.Ca(ClO)2也可用于脱硫,且脱硫效果比NaClO更好,原因是
(2)碘循环工艺也能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下:

则碘循环工艺的总反应为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以 还原
还原 的选择性催化还原(
的选择性催化还原( )技术广泛应用于烟气(含NO、
)技术广泛应用于烟气(含NO、 、
、 等)脱硝。
等)脱硝。
(1) 大量排放造成的环境问题主要有:
大量排放造成的环境问题主要有:_____ (填一种)。
(2)常压下,将一定比例的 、NO、
、NO、 、
、 的混合气体匀速通过装有催化剂的反应管,测得NO的转化率与
的混合气体匀速通过装有催化剂的反应管,测得NO的转化率与 的选择性
的选择性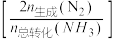 如图1所示。温度高于350℃,
如图1所示。温度高于350℃, 选择性下降的原因是
选择性下降的原因是_____ 。

(3)研究 法尾气中
法尾气中 脱除机理的流程如图2所示。其他条件一定时,在不通
脱除机理的流程如图2所示。其他条件一定时,在不通 、通入
、通入 两种情况下,
两种情况下, 的脱除率、NO的选择性
的脱除率、NO的选择性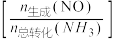 与通气时间的关系如图3所示。
与通气时间的关系如图3所示。

①反应17~19.2h时, 脱除率下降,其原因是
脱除率下降,其原因是_____ 。
②通入 后,NO选择性增大,其原因是
后,NO选择性增大,其原因是_____ 。
 还原
还原 的选择性催化还原(
的选择性催化还原( )技术广泛应用于烟气(含NO、
)技术广泛应用于烟气(含NO、 、
、 等)脱硝。
等)脱硝。(1)
 大量排放造成的环境问题主要有:
大量排放造成的环境问题主要有:(2)常压下,将一定比例的
 、NO、
、NO、 、
、 的混合气体匀速通过装有催化剂的反应管,测得NO的转化率与
的混合气体匀速通过装有催化剂的反应管,测得NO的转化率与 的选择性
的选择性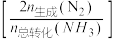 如图1所示。温度高于350℃,
如图1所示。温度高于350℃, 选择性下降的原因是
选择性下降的原因是
(3)研究
 法尾气中
法尾气中 脱除机理的流程如图2所示。其他条件一定时,在不通
脱除机理的流程如图2所示。其他条件一定时,在不通 、通入
、通入 两种情况下,
两种情况下, 的脱除率、NO的选择性
的脱除率、NO的选择性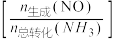 与通气时间的关系如图3所示。
与通气时间的关系如图3所示。
①反应17~19.2h时,
 脱除率下降,其原因是
脱除率下降,其原因是②通入
 后,NO选择性增大,其原因是
后,NO选择性增大,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】 和CO是常见的环境污染性气体。
和CO是常见的环境污染性气体。
(1)对于反应 来说,“
来说,“ ”可作为此反应的催化剂。其总反应分两步进行,第一步为
”可作为此反应的催化剂。其总反应分两步进行,第一步为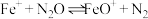 ,则第二步反应为
,则第二步反应为_______ 。已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能_______ (填“大于”“小于”或“等于”)第二步反应的活化能。
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应: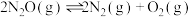 ,容器Ⅰ、Ⅱ、Ⅲ中
,容器Ⅰ、Ⅱ、Ⅲ中 的平衡转化率如图乙所示。
的平衡转化率如图乙所示。

①该反应的
_______ (填“ ”或“
”或“ ”)0。
”)0。
②若容器Ⅰ的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器Ⅰ中用 表示的反应速率为
表示的反应速率为_______ 。B点对应的平衡常数
_______ (保留两位有效数字)。
③若容器Ⅳ的体积为1L,反应在370℃下进行,则起始时反应_______ (填“向正反应方向”“向逆反应方向”或“不”)进行。
 和CO是常见的环境污染性气体。
和CO是常见的环境污染性气体。(1)对于反应
 来说,“
来说,“ ”可作为此反应的催化剂。其总反应分两步进行,第一步为
”可作为此反应的催化剂。其总反应分两步进行,第一步为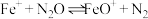 ,则第二步反应为
,则第二步反应为(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:
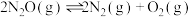 ,容器Ⅰ、Ⅱ、Ⅲ中
,容器Ⅰ、Ⅱ、Ⅲ中 的平衡转化率如图乙所示。
的平衡转化率如图乙所示。
①该反应的

 ”或“
”或“ ”)0。
”)0。②若容器Ⅰ的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器Ⅰ中用
 表示的反应速率为
表示的反应速率为
③若容器Ⅳ的体积为1L,反应在370℃下进行,则起始时反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知N2(g) +3H2(g) 2NH3(g) 298 K时,ΔH=-92.2 kJ·mol-1 ΔS=-198.2 J·K-1·mol-1,试判断该反应在常温下能否自发进行。
2NH3(g) 298 K时,ΔH=-92.2 kJ·mol-1 ΔS=-198.2 J·K-1·mol-1,试判断该反应在常温下能否自发进行。______
 2NH3(g) 298 K时,ΔH=-92.2 kJ·mol-1 ΔS=-198.2 J·K-1·mol-1,试判断该反应在常温下能否自发进行。
2NH3(g) 298 K时,ΔH=-92.2 kJ·mol-1 ΔS=-198.2 J·K-1·mol-1,试判断该反应在常温下能否自发进行。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO+2CO 2CO2+N2
2CO2+N2
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应是________ 反应(填写“吸热”、“放热”)。
(2)前2s内的平均反应速度v(N2)=________ 。
(3)此反应的平衡常数表达式为K=________ 。
(4)假设在容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是__ 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
2NO+2CO
 2CO2+N2
2CO2+N2 为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) /mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO) / mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应是
(2)前2s内的平均反应速度v(N2)=
(3)此反应的平衡常数表达式为K=
(4)假设在容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
您最近一年使用:0次

 ”表示。
”表示。
 的综合利用、实现
的综合利用、实现
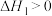
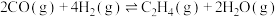




 和
和 的式子表示),该反应在
的式子表示),该反应在

