铁触媒催化合成氨经历下图所示①⑧步基元反应(从状态I至状态Ⅶ):
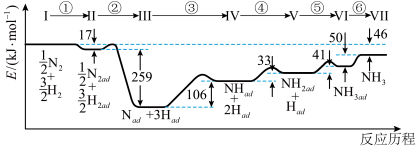
上图中“ad”表示吸附在催化剂表面的物质。完成下列问题:
(1)催化反应往往经过物质在催化剂表面的“吸附”过程和脱离催化剂表面的“脱附”过程。其中,“吸附”过程是上图中的第________ 步基元反应,“脱附”过程是_________ (填“吸热”或“放热”)过程。
(2)根据上图计算合成氨反应的焓变: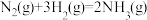 △H=
△H=___________ 。

上图中“ad”表示吸附在催化剂表面的物质。完成下列问题:
(1)催化反应往往经过物质在催化剂表面的“吸附”过程和脱离催化剂表面的“脱附”过程。其中,“吸附”过程是上图中的第
(2)根据上图计算合成氨反应的焓变:
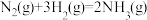 △H=
△H=
2024高三·全国·专题练习 查看更多[2]
(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
更新时间:2024-01-31 14:10:23
|
相似题推荐
填空题
|
适中
(0.65)
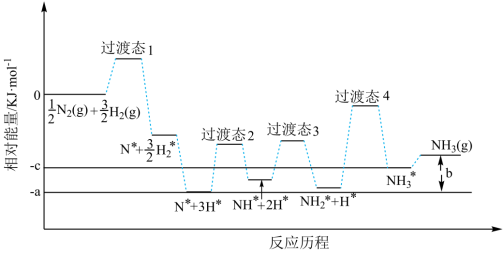
【推荐1】合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注,氮气在催化剂上的吸附活化是总反应中的控速步骤,适当提高氮气的浓度有利于合成氨反应的进行。_____ Ea(逆)(单选)。
A.> B.= C.<
2.该反应历程中决定化学反应速率快慢的基元反应是_____(单选)。
3.实际生产中,合成氨反应过程中使用的原料气N2和H2物质的量之比为1∶2.8,N2过量的原因是_____ 。
A.> B.= C.<
2.该反应历程中决定化学反应速率快慢的基元反应是_____(单选)。
| A.生成过渡态1 | B.生成过渡态2 |
| C.生成过渡态3 | D.生成过渡态4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请根据所学知识回答下列问题。
(1) 受热分解释放出
受热分解释放出 可引发白磷(
可引发白磷( )燃烧,31g
)燃烧,31g 完全燃烧生成五氧化二磷固体释放出akJ热量。下列说法中不正确的是
完全燃烧生成五氧化二磷固体释放出akJ热量。下列说法中不正确的是_______ (填字母)。
A. 的分解过程中只有共价键断裂没有共价键生成
的分解过程中只有共价键断裂没有共价键生成
B.若白磷完全燃烧释放出8akJ热量,则需要标准状况下 的体积为224L
的体积为224L
C.易燃易爆物应远离火源
(2)天然气已经成为我国主要的民用清洁能源,但天然气与空气混合达到一定比例后遇明火会发生爆炸,所以安全使用天然气,防止发生爆炸是极为重要的。已知天然气的主要成分甲烷( )燃烧时的能量变化如图所示:
)燃烧时的能量变化如图所示:
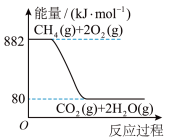
请回答下列问题。
①下列说法中正确的是_______ (填字母)。
A.天然气属于清洁能源,所以它属于新能源
B.甲烷完全燃烧时化学能全部转化为热能
C.标准状况下,44.8L甲烷完全燃烧时有8mol极性键断裂
D.用天然气做饭时,为使甲烷充分燃烧,通入的空气越多越好
② (g)完全燃烧时生成18g气态水放出的热量是
(g)完全燃烧时生成18g气态水放出的热量是_______ kJ。
③若家庭做饭需64160kJ热量,假设天然气(按 算)的热效率为80%,则需要天然气的质量为
算)的热效率为80%,则需要天然气的质量为_______ g。
(1)
 受热分解释放出
受热分解释放出 可引发白磷(
可引发白磷( )燃烧,31g
)燃烧,31g 完全燃烧生成五氧化二磷固体释放出akJ热量。下列说法中不正确的是
完全燃烧生成五氧化二磷固体释放出akJ热量。下列说法中不正确的是A.
 的分解过程中只有共价键断裂没有共价键生成
的分解过程中只有共价键断裂没有共价键生成B.若白磷完全燃烧释放出8akJ热量,则需要标准状况下
 的体积为224L
的体积为224LC.易燃易爆物应远离火源
(2)天然气已经成为我国主要的民用清洁能源,但天然气与空气混合达到一定比例后遇明火会发生爆炸,所以安全使用天然气,防止发生爆炸是极为重要的。已知天然气的主要成分甲烷(
 )燃烧时的能量变化如图所示:
)燃烧时的能量变化如图所示:
请回答下列问题。
①下列说法中正确的是
A.天然气属于清洁能源,所以它属于新能源
B.甲烷完全燃烧时化学能全部转化为热能
C.标准状况下,44.8L甲烷完全燃烧时有8mol极性键断裂
D.用天然气做饭时,为使甲烷充分燃烧,通入的空气越多越好
②
 (g)完全燃烧时生成18g气态水放出的热量是
(g)完全燃烧时生成18g气态水放出的热量是③若家庭做饭需64160kJ热量,假设天然气(按
 算)的热效率为80%,则需要天然气的质量为
算)的热效率为80%,则需要天然气的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.2SO2(g)+O2(g) 2SO3(g),反应过程的能量变化如图所示:
2SO3(g),反应过程的能量变化如图所示:

已知2mol SO2(g)和O2(g)反应生成为1mol SO3(g)的ΔΗ=-99kJ·mol-1,请回答下列问题。
(1)该反应通常用V2O5作催化剂,加V2O5会使图中B点_______ (填“升高”或“降低”)。
(2)图中ΔΗ=__________ 。
(3)如果反应速率v(SO2)为0.05mol·L-1·min-1,则v(O2)=_______ 。
Ⅱ.已知下列热化学方程式:
①H2O(l)===H2(g)+ O2(g)ΔH=+285.8 kJ/mol
O2(g)ΔH=+285.8 kJ/mol
②H2(g)+ O2(g)===H2O(g)ΔH=-241.8 kJ/mol
O2(g)===H2O(g)ΔH=-241.8 kJ/mol
③NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol
④C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ/mol
O2(g)===CO(g) ΔH=-110.5 kJ/mol
⑤C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于吸热反应的是___________ ;
(2)燃烧10 g H2生成液态水,放出的热量为__________ ;
(3)写出CO燃烧的热化学方程式__________ ;
(4)写出制水煤气的热化学方程式_____________ 。
 2SO3(g),反应过程的能量变化如图所示:
2SO3(g),反应过程的能量变化如图所示:
已知2mol SO2(g)和O2(g)反应生成为1mol SO3(g)的ΔΗ=-99kJ·mol-1,请回答下列问题。
(1)该反应通常用V2O5作催化剂,加V2O5会使图中B点
(2)图中ΔΗ=
(3)如果反应速率v(SO2)为0.05mol·L-1·min-1,则v(O2)=
Ⅱ.已知下列热化学方程式:
①H2O(l)===H2(g)+
 O2(g)ΔH=+285.8 kJ/mol
O2(g)ΔH=+285.8 kJ/mol②H2(g)+
 O2(g)===H2O(g)ΔH=-241.8 kJ/mol
O2(g)===H2O(g)ΔH=-241.8 kJ/mol③NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol
④C(s)+
 O2(g)===CO(g) ΔH=-110.5 kJ/mol
O2(g)===CO(g) ΔH=-110.5 kJ/mol⑤C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于吸热反应的是
(2)燃烧10 g H2生成液态水,放出的热量为
(3)写出CO燃烧的热化学方程式
(4)写出制水煤气的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)断裂1 mol H-H键、1 mol N-H键、 键分别需要吸收能量436 kJ。391 kJ、946 kJ,则合成氨反应的热化学方程式为
键分别需要吸收能量436 kJ。391 kJ、946 kJ,则合成氨反应的热化学方程式为___________ 。
(2)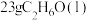 和一定量的氧气混合点燃,恰好完全反应,生成27 g液态水和
和一定量的氧气混合点燃,恰好完全反应,生成27 g液态水和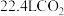 (标准状况),并放出683.5 kJ的热量,该反应的热化学方程式为
(标准状况),并放出683.5 kJ的热量,该反应的热化学方程式为___________ 。
 键分别需要吸收能量436 kJ。391 kJ、946 kJ,则合成氨反应的热化学方程式为
键分别需要吸收能量436 kJ。391 kJ、946 kJ,则合成氨反应的热化学方程式为(2)
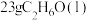 和一定量的氧气混合点燃,恰好完全反应,生成27 g液态水和
和一定量的氧气混合点燃,恰好完全反应,生成27 g液态水和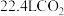 (标准状况),并放出683.5 kJ的热量,该反应的热化学方程式为
(标准状况),并放出683.5 kJ的热量,该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】非金属元素氮的单质及其化合物在生产生活中具有重要的作用。回答下列问题:
I.已知肼( )是氮的重要化合物,其与氧气反应的能量变化如图1所示
)是氮的重要化合物,其与氧气反应的能量变化如图1所示

(1) 的电子式为
的电子式为___________ ;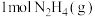 与足量
与足量 充分反应生成氮气和水蒸气的热化学方程式为
充分反应生成氮气和水蒸气的热化学方程式为___________ 。
(2)以 为原料合成的液体火箭燃料偏二甲肼(
为原料合成的液体火箭燃料偏二甲肼( )与液态氧化剂
)与液态氧化剂 反应产生大量无害气体和水,偏二甲肼与
反应产生大量无害气体和水,偏二甲肼与 反应的化学方程式为
反应的化学方程式为___________ 。
Ⅱ.图2为氮元素的“价一类”二维图,图3为工业上以A为原料制备C的工艺流程图。

(3)写出 与稀盐酸反应的离子方程式:
与稀盐酸反应的离子方程式:___________ 。
(4)写出在合金网的催化作用下A与空气中的氧气反应得到 的化学方程式:
的化学方程式:___________ 。
(5)上述工艺流程的“尾气”中主要含有氮氧化物( 、
、 )。
)。
①若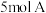 恰好能将
恰好能将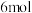 由
由 和
和 组成的混合气体完全转化为B和水,则混合气体中
组成的混合气体完全转化为B和水,则混合气体中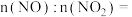
___________ 。
②在酸性条件下用酸性高锰酸钾溶液吸收 ,产物为
,产物为 和
和 ,则该反应中n(氧化产物):n(还原产物)=
,则该反应中n(氧化产物):n(还原产物)= ___________ 。
③用碱液吸收 (未配平)。已知X是一种盐,且在生成物中X与
(未配平)。已知X是一种盐,且在生成物中X与 的物质的量之比为1:1,则X的化学式为
的物质的量之比为1:1,则X的化学式为___________ 。
I.已知肼(
 )是氮的重要化合物,其与氧气反应的能量变化如图1所示
)是氮的重要化合物,其与氧气反应的能量变化如图1所示
(1)
 的电子式为
的电子式为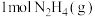 与足量
与足量 充分反应生成氮气和水蒸气的热化学方程式为
充分反应生成氮气和水蒸气的热化学方程式为(2)以
 为原料合成的液体火箭燃料偏二甲肼(
为原料合成的液体火箭燃料偏二甲肼( )与液态氧化剂
)与液态氧化剂 反应产生大量无害气体和水,偏二甲肼与
反应产生大量无害气体和水,偏二甲肼与 反应的化学方程式为
反应的化学方程式为Ⅱ.图2为氮元素的“价一类”二维图,图3为工业上以A为原料制备C的工艺流程图。

(3)写出
 与稀盐酸反应的离子方程式:
与稀盐酸反应的离子方程式:(4)写出在合金网的催化作用下A与空气中的氧气反应得到
 的化学方程式:
的化学方程式:(5)上述工艺流程的“尾气”中主要含有氮氧化物(
 、
、 )。
)。①若
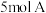 恰好能将
恰好能将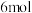 由
由 和
和 组成的混合气体完全转化为B和水,则混合气体中
组成的混合气体完全转化为B和水,则混合气体中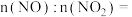
②在酸性条件下用酸性高锰酸钾溶液吸收
 ,产物为
,产物为 和
和 ,则该反应中n(氧化产物):n(还原产物)=
,则该反应中n(氧化产物):n(还原产物)= ③用碱液吸收
 (未配平)。已知X是一种盐,且在生成物中X与
(未配平)。已知X是一种盐,且在生成物中X与 的物质的量之比为1:1,则X的化学式为
的物质的量之比为1:1,则X的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.用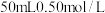 盐酸与
盐酸与 溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是_______ ;由图可知此装置除了两烧杯没有填满碎泡沫塑料外,还有何不妥之处,应如何改正?_______ ;
(2)用相同浓度和体积的氨水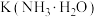 代替
代替 溶液进行上述实验,测得的中和反应反应热的数值会
溶液进行上述实验,测得的中和反应反应热的数值会_______ (填“偏大”、“偏小”、“无影响”)。
II.回答下列问题
(3)某些化学键的键能如表所示:
试回答下列问题:
已知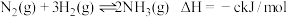 ,则
,则 键的键能是
键的键能是_______  (用含有a、b、c的式子表示)。
(用含有a、b、c的式子表示)。

(4)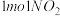 气体和
气体和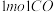 气体反应生成
气体反应生成 气体和
气体和 气体过程中的能量变化如图所示,请写出
气体过程中的能量变化如图所示,请写出 与
与 反应的热化学方程式:
反应的热化学方程式:_______ 。
(5)家用液化气的主要成分之一是丁烷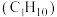 。常温常压条件下,
。常温常压条件下, 丁烷气体完全氧化生成
丁烷气体完全氧化生成 气体和液态水时放出热量
气体和液态水时放出热量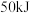 ,则表示丁烷
,则表示丁烷燃烧热 的热化学方程式为_______ 。
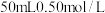 盐酸与
盐酸与 溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)用相同浓度和体积的氨水
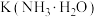 代替
代替 溶液进行上述实验,测得的中和反应反应热的数值会
溶液进行上述实验,测得的中和反应反应热的数值会II.回答下列问题
(3)某些化学键的键能如表所示:
| 化学键 |  |  |
键能/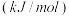 | a | b |
已知
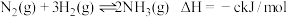 ,则
,则 键的键能是
键的键能是 (用含有a、b、c的式子表示)。
(用含有a、b、c的式子表示)。
(4)
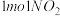 气体和
气体和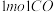 气体反应生成
气体反应生成 气体和
气体和 气体过程中的能量变化如图所示,请写出
气体过程中的能量变化如图所示,请写出 与
与 反应的热化学方程式:
反应的热化学方程式:(5)家用液化气的主要成分之一是丁烷
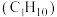 。常温常压条件下,
。常温常压条件下, 丁烷气体完全氧化生成
丁烷气体完全氧化生成 气体和液态水时放出热量
气体和液态水时放出热量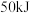 ,则表示丁烷
,则表示丁烷
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】乙烯是重要的有机化学原料,工业上可利用乙烷脱氢制备乙烯。
(1)乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
根据表格信息,乙烷裂解引发的反应主要为___________ 。
(2)经过引发的后续反应历程为(已略去链终止过程):
……
 ΔH1
ΔH1
 ΔH2
ΔH2
①C2H4(g)+H2(g)→C2H6(g)的ΔH=___________ (用含ΔH1和ΔH2的式子表示)。
②上述历程中“……”所代表的反应为___________ 。
(3)①丙烯与HCl发生加成反应,生成CH3CHClCH3和CH3CH2CH2Cl两种产物,其能量与反应历程如图所示,其中正确的说法是___________ 。

A.若反应的时间足够长,产物应该以CH3CH2CH2Cl为主
B.合成CH3CHClCH3的反应中,第I步反应为整个反应的决速步骤
C.总反应CH2=CHCH3(g)+HCl(g)=CH3CH2CH2Cl(g)的ΔH=ΔE3—ΔE4
②工业生产中,保持其他条件不变,若要提高产物中CH3CH2CH2Cl的比例,可采用的措施有___________ 、___________ 。
(1)乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
| 可能的引发反应 | 有关键的解离能(kJ/mol) |
| C2H6(g)→C2H5·(g)+H·(g) | 410 |
| C2H6(g)→2CH3·(g) | 368 |
根据表格信息,乙烷裂解引发的反应主要为
(2)经过引发的后续反应历程为(已略去链终止过程):
……
 ΔH1
ΔH1 ΔH2
ΔH2①C2H4(g)+H2(g)→C2H6(g)的ΔH=
②上述历程中“……”所代表的反应为
(3)①丙烯与HCl发生加成反应,生成CH3CHClCH3和CH3CH2CH2Cl两种产物,其能量与反应历程如图所示,其中正确的说法是

A.若反应的时间足够长,产物应该以CH3CH2CH2Cl为主
B.合成CH3CHClCH3的反应中,第I步反应为整个反应的决速步骤
C.总反应CH2=CHCH3(g)+HCl(g)=CH3CH2CH2Cl(g)的ΔH=ΔE3—ΔE4
②工业生产中,保持其他条件不变,若要提高产物中CH3CH2CH2Cl的比例,可采用的措施有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在101kPa下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
(1)该反应的反应物总能量___________ (填“大于”“小于”或“等于”)生成物总能量。
(2)氢气的燃烧热为___________
(3)该反应的热化学方程式为___________ 。
(4)若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O的键能为463kJ·mol-1,0=0的键能为498kJmol,计算H-H的键能为___________ kJ·mol-1.
(1)该反应的反应物总能量
(2)氢气的燃烧热为
(3)该反应的热化学方程式为
(4)若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O的键能为463kJ·mol-1,0=0的键能为498kJmol,计算H-H的键能为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ、工业上制硫酸的主要反应之一为2SO2(g)+O2(g) 2SO3(g),反应过程中能量的变化如图所示。
2SO3(g),反应过程中能量的变化如图所示。

(1)由图可知该反应的正反应为_______ (填“吸热”或“放热”)反应。
(2)向反应体系中加入催化剂后,图中E1_____ (填“增大”“减小”或“不变”,下同),E3______ 。
Ⅱ、如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中,试回答下列问题:

(3)写出试管内反应的离子方程式___________________________ ;
(4)实验中观察到石灰水中的现象:Ⅰ镁片溶解、Ⅱ镁片上产生大量气泡、Ⅲ_________________ ,产生上述现象Ⅲ的原因是____________________________ 。
(5)由实验推知,MgCl2溶液和H2的总能量______ (填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
 2SO3(g),反应过程中能量的变化如图所示。
2SO3(g),反应过程中能量的变化如图所示。
(1)由图可知该反应的正反应为
(2)向反应体系中加入催化剂后,图中E1
Ⅱ、如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中,试回答下列问题:

(3)写出试管内反应的离子方程式
(4)实验中观察到石灰水中的现象:Ⅰ镁片溶解、Ⅱ镁片上产生大量气泡、Ⅲ
(5)由实验推知,MgCl2溶液和H2的总能量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在等压下化学反应所吸收或放出的热量,称为化学反应的焓变。回答下列问题:
(1)25℃、 时,
时, 氨气完全燃烧放出
氨气完全燃烧放出 的热量,则
的热量,则

___________  。
。
(2) 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。

已知: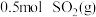 被氧化为
被氧化为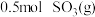 的
的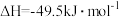 。则:
。则:
①E的大小对该反应的反应热___________ (填“有”或“无”)影响;该反应通常用 作催化剂,加
作催化剂,加 会使图中B点
会使图中B点___________ (填“升高”或“降低”)。
② 氧化为
氧化为 的热化学方程式为
的热化学方程式为___________ 。
(3)已知拆开 键、
键、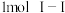 、
、 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、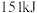 、
、 。则由氢气和碘反应生成
。则由氢气和碘反应生成 需要
需要___________ (填“放出”或“吸收”)___________  的热量。
的热量。
(4)发射卫星时可用肼( )为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:①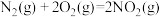
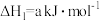
②

写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:___________ 。
(1)25℃、
 时,
时, 氨气完全燃烧放出
氨气完全燃烧放出 的热量,则
的热量,则

 。
。(2)
 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。
已知:
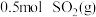 被氧化为
被氧化为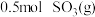 的
的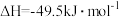 。则:
。则:①E的大小对该反应的反应热
 作催化剂,加
作催化剂,加 会使图中B点
会使图中B点②
 氧化为
氧化为 的热化学方程式为
的热化学方程式为(3)已知拆开
 键、
键、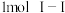 、
、 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、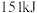 、
、 。则由氢气和碘反应生成
。则由氢气和碘反应生成 需要
需要 的热量。
的热量。(4)发射卫星时可用肼(
 )为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:①
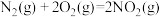
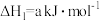
②


写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某学生为探究锌与稀盐酸反应的速率变化,用排水集气法收集反应放出的氢气。所用稀盐酸浓度有1.00mol·L-1、2.00mol·L-1两种浓度,每次实验稀盐酸的用量为25.00mL,锌有细颗粒与粗颗粒两种规格,用量为6.50g。实验温度为25℃、35℃。(已知Zn2+对该反应的反应速率无影响)
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
(2)实验①记录如下(换算成标况):
①计算在30~40s范围内盐酸的平均反应速率ν(HCl)=_______ (忽略溶液体积变化);
②反应速率最大的时间段(如0~10s)为_______ ,可能原因是_______ ;
③反应速率后段明显下降的主要影响因素是_______ 。
(3)测量氢气体积时,在不影响产生H2气体总量的情况下,往往在盐酸中分别加入相同体积的下列溶液以减慢反应速率,你认为可行的是_______(填序号)。
(4)某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。
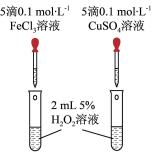
①如图可通过观察_______ 现象,比较得出Fe3+和Cu2+对H2O2分解的催化效果结论;
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______ 。
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
| 编号 | t/℃ | 锌规格 | 盐酸浓度/mol·L-1 | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | I.实验①和②探究盐酸浓度对该反应速率的影响; II.实验 III.实验 |
| ② | 25 | 粗颗粒 | 1.00 | |
| ③ | 35 | 粗颗粒 | 2.00 | |
| ④ | 25 | 细颗粒 | 2.00 |
| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积/mL | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(如0~10s)为
③反应速率后段明显下降的主要影响因素是
(3)测量氢气体积时,在不影响产生H2气体总量的情况下,往往在盐酸中分别加入相同体积的下列溶液以减慢反应速率,你认为可行的是_______(填序号)。
| A.NaNO3溶液 | B.NaCl溶液 | C.CuSO4溶液 | D.Na2CO3溶液 |

①如图可通过观察
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某研究小组同学用活性炭还原处理氮氧化物,向 恒容密闭容器中加入足量C与
恒容密闭容器中加入足量C与 发生反应,
发生反应, 。在不同实验条件下,平衡时
。在不同实验条件下,平衡时 与温度T的关系如图所示:
与温度T的关系如图所示:
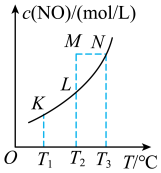
(1)结合图中数据,判断该反应的
___________ 0(填“>”或“<”),理由是___________ 。
(2)K、L、M、N四点对应的平衡常数分别为 、
、 、
、 、
、 ,判断其大小关系
,判断其大小关系_____ 。
使用氢能源可以减少汽车尾气中氮氧化合物的排放。利用甲醇与水蒸气反应可以制备氢气: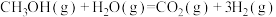 ,该反应过程中的能量变化如图:
,该反应过程中的能量变化如图:

(3)
___________ 0(填“>”“=”或“<”),途径(I)的活化能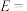
___________ 。
(4)途径(I)变为途径(II):改变的条件是___________ ,反应热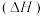
___________ (填“增大”“减小”或“不变”)。
(5)下列有关活化分子的说法正确的是___________。
 恒容密闭容器中加入足量C与
恒容密闭容器中加入足量C与 发生反应,
发生反应, 。在不同实验条件下,平衡时
。在不同实验条件下,平衡时 与温度T的关系如图所示:
与温度T的关系如图所示:
(1)结合图中数据,判断该反应的

(2)K、L、M、N四点对应的平衡常数分别为
 、
、 、
、 、
、 ,判断其大小关系
,判断其大小关系使用氢能源可以减少汽车尾气中氮氧化合物的排放。利用甲醇与水蒸气反应可以制备氢气:
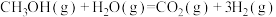 ,该反应过程中的能量变化如图:
,该反应过程中的能量变化如图:
(3)

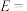
(4)途径(I)变为途径(II):改变的条件是
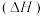
(5)下列有关活化分子的说法正确的是___________。
| A.增大反应物浓度可以提高活化分子百分数 |
| B.增大体系的压强一定能提高活化分子百分数 |
| C.使用合适的催化剂可以增大活化分子的能量 |
| D.升高温度能提高活化分子百分数 |
您最近一年使用:0次



