回答下列问题:
(1)以NH3、CO2为原料生产重要的高效氮肥——尿素[CO(NH2)2],涉及反应的反应过程中能量变化示意图如图1所示:
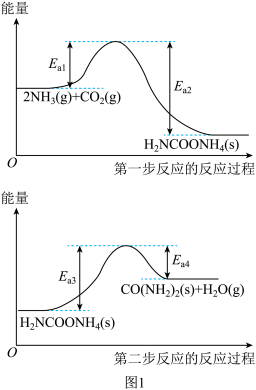
写出第一步反应的热化学方程式:_____ 。已知两步反应中第二步反应是生产尿素的决速步骤,可判断Ea1_____ (填“>”“<”或“=”)Ea3。
(2)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程,部分历程如图2所示,其中吸附在催化剂表面的物种用*标注。
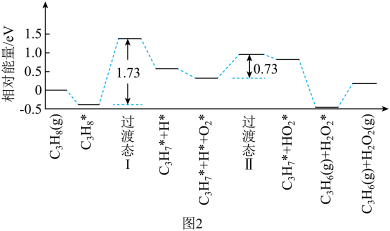
①该历程中决速步骤能垒(活化能)为_____ eV。
②该历程中最低能垒对应步骤的化学方程式为_____ 。
③该历程之后可能发生反应的化学方程式为_____ 。
(1)以NH3、CO2为原料生产重要的高效氮肥——尿素[CO(NH2)2],涉及反应的反应过程中能量变化示意图如图1所示:

写出第一步反应的热化学方程式:
(2)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程,部分历程如图2所示,其中吸附在催化剂表面的物种用*标注。

①该历程中决速步骤能垒(活化能)为
②该历程中最低能垒对应步骤的化学方程式为
③该历程之后可能发生反应的化学方程式为
2023高三·全国·专题练习 查看更多[1]
(已下线)题型15 盖斯定律与热化学方程式的书写
更新时间:2023-02-20 18:40:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】分类思想是化学重要的学科思想。下表是对部分常见的 18 电子微粒的分类。
请结合表格中的微粒(或由微粒组成的物质)完成下列问题:
(1)根据分类时呈现的规律,可推知表格中:①_________ ②_______ (填分子式)
(2)热稳定性:H2S____ SiH4(填“>”、“<”或“=”)还原性:Cl- ___ S2-(填“>”、“<”或“=”)
(3)KHS的电子式为______ , CaO2和 N2H4均含有____ 键(填“离子”、“极性”“非极性'”)
(4)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2)当它们混合时 , 即产 生大量的N2和水蒸气,并放出大量热。已知 0.2mol 液态肼 和足量H2O2反应,生成氮气和水蒸气, 放出 Q kJ 的热量。写出该反应的热化学方程式____ 。
(5)已知拆开 lmolHCl 分子中的化学键需要消耗 431kJ 能量, 根据下面的能量图,回答下列问题:
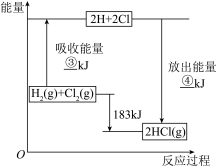
分别写出③、④ 的数值:③______ kJ;④______ kJ。
(6)已知在常温常压下:
2CH3OH(l)+ 3O2(g)=2CO2(g)+4H2O(g) ΔH= -1275.6kJ/mol
H2O(l)= H2O(g) ΔH = + .44.0kJ/mol
写出表示甲醇燃烧热的热化学方程式_______ 。
| 分子 | Ar |
| HCl H2S ① SiH4 | |
| F2 H2O2 N2H4 ② | |
| CH3F CH3OH | |
| 阳离子 | K+ Ca2+ |
| 阴离子 | Cl- S2- |
HS- O |
请结合表格中的微粒(或由微粒组成的物质)完成下列问题:
(1)根据分类时呈现的规律,可推知表格中:①
(2)热稳定性:H2S
(3)KHS的电子式为
(4)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2)当它们混合时 , 即产 生大量的N2和水蒸气,并放出大量热。已知 0.2mol 液态肼 和足量H2O2反应,生成氮气和水蒸气, 放出 Q kJ 的热量。写出该反应的热化学方程式
(5)已知拆开 lmolHCl 分子中的化学键需要消耗 431kJ 能量, 根据下面的能量图,回答下列问题:

分别写出③、④ 的数值:③
(6)已知在常温常压下:
2CH3OH(l)+ 3O2(g)=2CO2(g)+4H2O(g) ΔH= -1275.6kJ/mol
H2O(l)= H2O(g) ΔH = + .44.0kJ/mol
写出表示甲醇燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知在298K时的热化学反应方程式:
①C(s,石墨)+O2(g)=CO2(g); △H1=-393.5kJ/mol,
②2CO(g)+O2(g)=2CO2(g); △H2=-566.0kJ/mol。
则298K时,反应 C(s,石墨)+ 1/2 O2(g) = CO(g)的△H是______________
①C(s,石墨)+O2(g)=CO2(g); △H1=-393.5kJ/mol,
②2CO(g)+O2(g)=2CO2(g); △H2=-566.0kJ/mol。
则298K时,反应 C(s,石墨)+ 1/2 O2(g) = CO(g)的△H是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题:
(1)已知:氢气的燃烧热ΔH=-285.8 kJ/mol,则氢气燃烧的热化学方程式可表示为_____ 。
(2)如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,此反应的热化学方程式为________________ 。
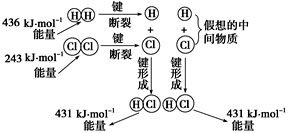
(3)已知:1 mol水蒸气变成液态水放热44 kJ,结合本题(1)、(2)信息,推知:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ΔH=
2Cl2(g)+2H2O(g) ΔH=________ kJ/mol。
(1)已知:氢气的燃烧热ΔH=-285.8 kJ/mol,则氢气燃烧的热化学方程式可表示为
(2)如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,此反应的热化学方程式为

(3)已知:1 mol水蒸气变成液态水放热44 kJ,结合本题(1)、(2)信息,推知:4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g) ΔH=
2Cl2(g)+2H2O(g) ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】N2O和CO是常见的环境污染气体。
(1)对于反应N2O(g)+CO(g) CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
第一步为Fe++N2O FeO++N2;则第二步为
FeO++N2;则第二步为____________________ (写化学方程式)。
已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能_________ (填“大于”“小于”或“等于”)第二步反应的活化能。
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g) 2N2(g)+O2(g),容器I、II、III中N2O的平衡转化率如图乙所示:
2N2(g)+O2(g),容器I、II、III中N2O的平衡转化率如图乙所示:
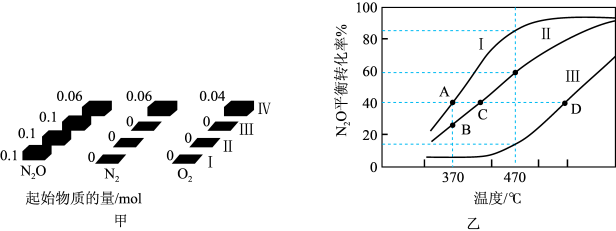
①该反应的△H_____ 0(填“>”或“<”)。
②若容器I的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器I中用O2表示的反应速率为_________ 。B点对应的平衡常数k=________ (保留两位有效数字)。
③图中A、C、D三点容器内气体密度由大到小的顺序是_______________ 。
④若容器Ⅳ体积为1L,反应在370℃下进行,则起始时反应_________ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(1)对于反应N2O(g)+CO(g)
 CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:第一步为Fe++N2O
 FeO++N2;则第二步为
FeO++N2;则第二步为已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g)
 2N2(g)+O2(g),容器I、II、III中N2O的平衡转化率如图乙所示:
2N2(g)+O2(g),容器I、II、III中N2O的平衡转化率如图乙所示:
①该反应的△H
②若容器I的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器I中用O2表示的反应速率为
③图中A、C、D三点容器内气体密度由大到小的顺序是
④若容器Ⅳ体积为1L,反应在370℃下进行,则起始时反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应过程伴随有热量的变化。
(1)下列反应中属于吸热反应的有___________ 。(填序号)
①C与H2O(g)反应制取水煤气
②食物因氧化而腐败
③煅烧石灰石(主要成分是CaCO3)制生石灰
④燃烧木炭取暖
⑤氯化铵晶体和 混合搅拌
混合搅拌
(2)已知在298K、101kPa下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热( )。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。
)。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。
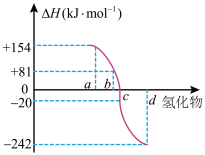
硫化氢发生分解反应的热化学方程式为___________ 。
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
①已知 ,则
,则
___________ 。
②已知 ,当放出的热量为
,当放出的热量为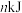 时,该反应转移电子的物质的量为
时,该反应转移电子的物质的量为___________ 。(用含m、n的代数式表示)
③制备合成气反应历程分两步,步骤Ⅰ: ;步骤Ⅱ:
;步骤Ⅱ: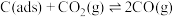 。
。
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
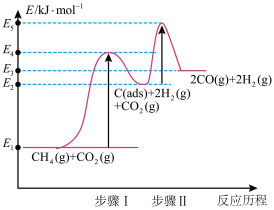
步骤Ⅱ正反应的活化能为___________ ,决定制备合成气反应速率的是___________ (填“步骤Ⅰ”或“步骤Ⅱ”)。
(1)下列反应中属于吸热反应的有
①C与H2O(g)反应制取水煤气
②食物因氧化而腐败
③煅烧石灰石(主要成分是CaCO3)制生石灰
④燃烧木炭取暖
⑤氯化铵晶体和
 混合搅拌
混合搅拌(2)已知在298K、101kPa下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热(
 )。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。
)。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。
硫化氢发生分解反应的热化学方程式为
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
| 化学键 |  | 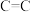 |  |  |
 | 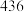 |  | 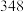 |  |
 ,则
,则
②已知
 ,当放出的热量为
,当放出的热量为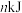 时,该反应转移电子的物质的量为
时,该反应转移电子的物质的量为③制备合成气反应历程分两步,步骤Ⅰ:
 ;步骤Ⅱ:
;步骤Ⅱ: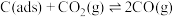 。
。上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:

步骤Ⅱ正反应的活化能为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业合成NH3的反应,解决了世界约三分之一的人粮食问题。
(1)已知:N2+3H2⇌2NH3,且该反应的v正=k正·c(N2)·c3(H2),v逆=k逆·c2(NH3),则反应 N2+
N2+ H2⇌NH3的平衡常数K=
H2⇌NH3的平衡常数K=_______ (用k正和k逆表示)。
(2)已知合成氨的反应升高温度平衡常数会减小,则该反应的正反应活化能E1和逆反应活化能E2的相对大小关系为:E1_______ E2。(填“>”、“<”或“=”)。
(3)从化学反应的角度分析工业合成氨气采取30 MPa~50 MPa高压的原因是_______ 。
(4)500 ℃时,向容积为2 L的密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,容器内的压强随时间的变化如下表所示:
①达到平衡时N2的转化率为_______ 。
②用压强表示该反应的平衡常数Kp=_______ (Kp等于平衡时生成物分压幂的乘积与反应物分压幂的乘积的比值,某物质的分压=总压×该物质的物质的量分数)。
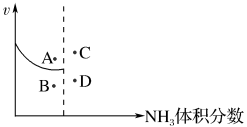
③随着反应的进行合成氨的正反应速率与NH3的体积分数的关系如下图所示,若升高温度再次达到平衡时,可能的点为_______ (从点“A、B、C、D”中选择)
(1)已知:N2+3H2⇌2NH3,且该反应的v正=k正·c(N2)·c3(H2),v逆=k逆·c2(NH3),则反应
 N2+
N2+ H2⇌NH3的平衡常数K=
H2⇌NH3的平衡常数K=(2)已知合成氨的反应升高温度平衡常数会减小,则该反应的正反应活化能E1和逆反应活化能E2的相对大小关系为:E1
(3)从化学反应的角度分析工业合成氨气采取30 MPa~50 MPa高压的原因是
(4)500 ℃时,向容积为2 L的密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,容器内的压强随时间的变化如下表所示:
| 时间/min | 0 | 10 | 20 | 30 | 40 | +∞ |
| 压强/MPa | 20 | 17 | 15 | 13.2 | 11 | 11 |
①达到平衡时N2的转化率为
②用压强表示该反应的平衡常数Kp=
③随着反应的进行合成氨的正反应速率与NH3的体积分数的关系如下图所示,若升高温度再次达到平衡时,可能的点为

您最近一年使用:0次



