CH3OH 是一种无色有刺激性气味的液体,在生产生活中有重要用途。
Ⅰ.目前工业上有一种方法是用 CO2生产燃料甲醇。一定条件下发生反应:CO2(g) +3H2(g)=CH3OH(g)+H2O(g),该反应的能量变化如图所示:
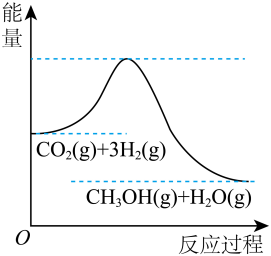
(1)你认为该反应为_____ (填放热或吸热)反应.
(2)恒容容器中,对于以上反应,能加快反应速率的是_____ 。
a.升高温度 b.充入 He c.加入催化剂 d.降低压强
Ⅱ. CH3OH 也是一种重要的燃料,一定条件下发生反应:
2CH3OH(g)+3O2(g) =2 CO2(g)+4H2O(g)。
(3)某温度下,将 4mol CH3OH 和 6 mol O2充入 2 L 的密闭容器中经过 4 min 反应达到平衡,测得 c(O2)=1.5mol·L-1,4 min 内平均反应速率 υ(H2O)=_____ 。
(4)CH3OH 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是_____ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗 6.4 g CH3OH 转移 1.2 mol 电子
(5)以 CH3OH、空气(氧气)、氢氧化钾溶液为原料,石墨为电极构成燃料电池,该电池中负极上的电极反应式是:____________________________ 。
Ⅰ.目前工业上有一种方法是用 CO2生产燃料甲醇。一定条件下发生反应:CO2(g) +3H2(g)=CH3OH(g)+H2O(g),该反应的能量变化如图所示:

(1)你认为该反应为
(2)恒容容器中,对于以上反应,能加快反应速率的是
a.升高温度 b.充入 He c.加入催化剂 d.降低压强
Ⅱ. CH3OH 也是一种重要的燃料,一定条件下发生反应:
2CH3OH(g)+3O2(g) =2 CO2(g)+4H2O(g)。
(3)某温度下,将 4mol CH3OH 和 6 mol O2充入 2 L 的密闭容器中经过 4 min 反应达到平衡,测得 c(O2)=1.5mol·L-1,4 min 内平均反应速率 υ(H2O)=
(4)CH3OH 燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗 6.4 g CH3OH 转移 1.2 mol 电子
(5)以 CH3OH、空气(氧气)、氢氧化钾溶液为原料,石墨为电极构成燃料电池,该电池中负极上的电极反应式是:
更新时间:2020-05-28 22:46:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)以下反应:①木炭与水制备水煤气,②氯酸钾分解,③炸药爆炸,④酸与碱的中和反应,⑤生石灰与水作用制熟石灰,⑥Ba(OH)2•H2O 与 NH4Cl ,⑦浓硫酸溶于水, 属于放热反应__________ .(填序号)
(2)Mg-Al-NaOH 电池中的负极反应:___________ .
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为___________ ,当线路中转移 0.2mol 电 子时,则被腐蚀铜的质量为___________ g.
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出___________ 的热量。
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是___________ ,存在非极性键的是___________ 。
(2)Mg-Al-NaOH 电池中的负极反应:
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.在1×105Pa,25℃时,H-H键、N≡N键和N-H键的键能分别为436kJ·mol-1、945kJ·mol-1和391kJ·mol-1。
(1)①根据上述数据判断工业合成氨的反应是_______ (填“吸热”或“放热”)反应;
②在25℃时,在催化剂存在下进行反应,消耗1mol氮气和3mol氢气,理论上放出或吸收的热量为Q1,则Q1为_______ kJ;
③实际生产中,当加入0.5mol氮气和1.5mol氢气放出或吸收的热量为Q2,Q1与Q2比较,正确的是_______ 。
a.Q1>2Q2 b.Q1<2Q2 c.Q1=2Q2 d.2Q1>Q2
II.某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。
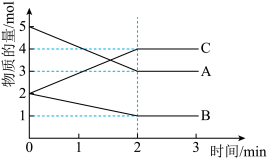
(2)该反应的化学方程式为_______ 。
(3)反应开始至2min时,B的平均反应速率为_______ 。
(4)能说明该反应已达到平衡状态的是_______ (填字母)。
a.v(A)=2v(B) b.容器内混合气体的密度保持不变
c.2v逆(A)=v正(B) d.容器内各物质浓度保持不变
(5)在密闭容器里,通入一定量的A、B、C,发生上述反应。达平衡后,当改变下列条件时,反应速率会减小的是_______ (填序号)。
①降低温度 ②加入正催化剂 ③减小容器容积
(1)①根据上述数据判断工业合成氨的反应是
②在25℃时,在催化剂存在下进行反应,消耗1mol氮气和3mol氢气,理论上放出或吸收的热量为Q1,则Q1为
③实际生产中,当加入0.5mol氮气和1.5mol氢气放出或吸收的热量为Q2,Q1与Q2比较,正确的是
a.Q1>2Q2 b.Q1<2Q2 c.Q1=2Q2 d.2Q1>Q2
II.某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。

(2)该反应的化学方程式为
(3)反应开始至2min时,B的平均反应速率为
(4)能说明该反应已达到平衡状态的是
a.v(A)=2v(B) b.容器内混合气体的密度保持不变
c.2v逆(A)=v正(B) d.容器内各物质浓度保持不变
(5)在密闭容器里,通入一定量的A、B、C,发生上述反应。达平衡后,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入正催化剂 ③减小容器容积
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)写出重晶石的化学式___________ ;写出CO2的电子式___________ 。
(2)下列变化中属于吸热反应的是___________ (填序号)。
①盐酸和碳酸氢钠反应 ②将胆矾加热变为白色粉末 ③苛性钠固体溶于水
④氢氧化钡和氯化铵晶体反应 ⑤生石灰跟水反应生成熟石灰 ⑥镁和盐酸反应
(3)写出氨的催化氧化的化学反应方程式___________ 。
(4)写出工业上制取粗硅的化学反应方程式___________ 。
(1)写出重晶石的化学式
(2)下列变化中属于吸热反应的是
①盐酸和碳酸氢钠反应 ②将胆矾加热变为白色粉末 ③苛性钠固体溶于水
④氢氧化钡和氯化铵晶体反应 ⑤生石灰跟水反应生成熟石灰 ⑥镁和盐酸反应
(3)写出氨的催化氧化的化学反应方程式
(4)写出工业上制取粗硅的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理:2NO(g)+2CO(g)===N2(g)+2CO2(g),在298 K、100 kPa下,ΔH=-113 kJ/mol,ΔS=-145 J/(mol·K).
(1)为了提高该反应的速率和NO的转化率,采取的正确措施为________ .
(2)该反应达到平衡时若缩小体积,则混合气体的平均相对分子质量________ ,若升高温度,则该反应的平衡常数________ (均填“增大”、“减小”或“不变”).
(3)该条件下反应__________________ (填“能”或“不能”)自发进行.
(4)在如图中画出在某时刻条件改变后的图象_______ (其他条件不变).
t1:增大NO的浓度
t2:降低温度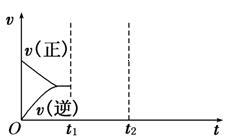
(1)为了提高该反应的速率和NO的转化率,采取的正确措施为
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
(3)该条件下反应
(4)在如图中画出在某时刻条件改变后的图象
t1:增大NO的浓度
t2:降低温度

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究 之间的转化具有重要意义。
之间的转化具有重要意义。
已知:

将一定量 气体充入恒容的密闭容器中,控制反应温度为
气体充入恒容的密闭容器中,控制反应温度为 。
。
(1)下列可以作为反应达到平衡的判据是___________(填编号)。
(2)反应温度 时,体系中
时,体系中 、
、 随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为
随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为 ,
, 随t(时间)变化曲线如图虚线所示。
随t(时间)变化曲线如图虚线所示。
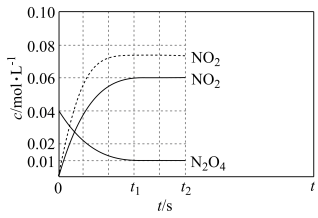
①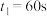 ,在0~60s时段,反应速率
,在0~60s时段,反应速率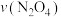 为
为___________ 
②反应温度为
___________ (填“大于”或“小于”) 。
。
③温度 时反应达平衡后,将反应容器的容积减少一半,平衡向
时反应达平衡后,将反应容器的容积减少一半,平衡向___________ (填“正反应”或“逆反应”)方向移动。
④ 时刻反应达到平衡,混合气体平衡总压强为p,
时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为75%,则反应
气体的平衡转化率为75%,则反应 的平衡常数
的平衡常数
___________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)NO氧化反应: 分两步进行,其反应过程能量变化示意图如图。
分两步进行,其反应过程能量变化示意图如图。
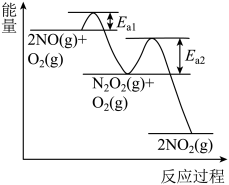
Ⅰ.

Ⅱ.

决定NO氧化反应速率的步骤是___________ (填“Ⅰ”或“Ⅱ”)。
 之间的转化具有重要意义。
之间的转化具有重要意义。已知:


将一定量
 气体充入恒容的密闭容器中,控制反应温度为
气体充入恒容的密闭容器中,控制反应温度为 。
。(1)下列可以作为反应达到平衡的判据是___________(填编号)。
| A.气体的压强不变 | B. |
| C.K不变 | D.容器内颜色不变 |
(2)反应温度
 时,体系中
时,体系中 、
、 随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为
随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为 ,
, 随t(时间)变化曲线如图虚线所示。
随t(时间)变化曲线如图虚线所示。
①
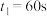 ,在0~60s时段,反应速率
,在0~60s时段,反应速率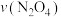 为
为
②反应温度为

 。
。③温度
 时反应达平衡后,将反应容器的容积减少一半,平衡向
时反应达平衡后,将反应容器的容积减少一半,平衡向④
 时刻反应达到平衡,混合气体平衡总压强为p,
时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为75%,则反应
气体的平衡转化率为75%,则反应 的平衡常数
的平衡常数
(3)NO氧化反应:
 分两步进行,其反应过程能量变化示意图如图。
分两步进行,其反应过程能量变化示意图如图。
Ⅰ.


Ⅱ.


决定NO氧化反应速率的步骤是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知25℃时有关弱酸的电离常数如表:
(1)25℃时,将20mL0.1mol·L-1CH3COOH溶液和20mL0.1mol·L-1HSCN溶液分别与20mL0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示。
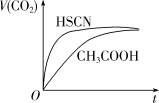
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是___ 。
(2)若保持温度不变,在醋酸溶液中通入一定量氨,下列量会变小的是___ (填字母)。
a.c(CH3COO-) b.c(H+) c.Kw d.醋酸的电离常数
| 弱酸 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
(1)25℃时,将20mL0.1mol·L-1CH3COOH溶液和20mL0.1mol·L-1HSCN溶液分别与20mL0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示。

反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是
(2)若保持温度不变,在醋酸溶液中通入一定量氨,下列量会变小的是
a.c(CH3COO-) b.c(H+) c.Kw d.醋酸的电离常数
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s) 2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:
2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:

(1)已知该反应只有高温下能自发进行,则该反应的△H___________ 0(填“>”、“<”或“=”)。
(2)在上述反应条件下,从反应开始到平衡,用V(B)=___________ mol·L-1·min-1,500℃时的平衡常数K=___________ ;
(3)在反应温度和容器体积不变的条件下,下列能说明上述反应达到平衡状态的是_________ ;
A.混合气体的压强保持不变 B.气体C的体积分数保持不变
C.混合气体的密度保持不变 D.B的正反应速率等于C的逆反应速率
(4)在500℃时,上述反应达到平衡后,在8min时将容器体积迅速压缩为1.0L,反应在12min建立新的平衡,画出8~15min内C气体物质的量浓度随时间变化的示意图。_______
 2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:
2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:
(1)已知该反应只有高温下能自发进行,则该反应的△H
(2)在上述反应条件下,从反应开始到平衡,用V(B)=
(3)在反应温度和容器体积不变的条件下,下列能说明上述反应达到平衡状态的是
A.混合气体的压强保持不变 B.气体C的体积分数保持不变
C.混合气体的密度保持不变 D.B的正反应速率等于C的逆反应速率
(4)在500℃时,上述反应达到平衡后,在8min时将容器体积迅速压缩为1.0L,反应在12min建立新的平衡,画出8~15min内C气体物质的量浓度随时间变化的示意图。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示.由图中数据分析:
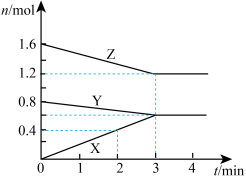
(1)该反应的化学方程式:_____________________ ;
(2)反应开始至2min末,X的反应速率为__________________ ;
(3)平衡时Z的转化率为_________________ 。
(4)3min后图中曲线所表示的含义是_______________ 。

(1)该反应的化学方程式:
(2)反应开始至2min末,X的反应速率为
(3)平衡时Z的转化率为
(4)3min后图中曲线所表示的含义是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一定条件下,恒容密闭容器中发生某可逆反应,A、B、C三种气体的物质的量浓度随时间的变化如图所示。请回答下列问题:
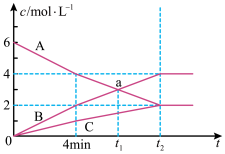
(1)此反应的化学方程式为___ 。
(2)反应从开始至4min末,用A表示的平均反应速率为____ 。
(3)t2的值___ 8(填“大于”、“等于”或“小于”),其原因是___ 。
(4)某同学经分析得出如下结论,其中正确的是___ (填选项序号)。
①该反应在t1时刻达到了反应限度
②保持条件不变,延续足够长的时间,容器中将可能不存在A物质
③该反应达到了反应限度后物质B的质量将保持不变
④改变反应条件将可能改变反应的限度

(1)此反应的化学方程式为
(2)反应从开始至4min末,用A表示的平均反应速率为
(3)t2的值
(4)某同学经分析得出如下结论,其中正确的是
①该反应在t1时刻达到了反应限度
②保持条件不变,延续足够长的时间,容器中将可能不存在A物质
③该反应达到了反应限度后物质B的质量将保持不变
④改变反应条件将可能改变反应的限度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下图是一个电化学过程的示意图。已知甲池的总反应式为2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O

(1)请回答图中甲、乙两池的名称。
甲池是________ 装置,乙池是________ 装置。
(2)请回答下列电极的名称;
通入CH3OH的电极名称是_________ ,B(石墨)电极的名称是____________ 。
(3)写出电极反应式;通入O2的电极的电极反应式为_______________________ 。
A(Fe)电极的电极反应式为_______________________ 。
(4)乙池中反应的化学方程式为________________________ 。
 2K2CO3+6H2O
2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称。
甲池是
(2)请回答下列电极的名称;
通入CH3OH的电极名称是
(3)写出电极反应式;通入O2的电极的电极反应式为
A(Fe)电极的电极反应式为
(4)乙池中反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】右图是一个化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O。

(1)请回答图中甲、乙两池的名称。甲池是________ 装置,乙池是________ 装置。
(2)请回答下列电极的名称:通入CH3OH的电极名称是__________________ ,B(石墨)电极的名称是______________________ 。
(3)写出电极反应式:通入O2的电极的电极反应式是__________________ 。A(Fe)电极的电极反应式为_______________________________________ 。
(4)乙池中反应的化学方程式为________________________________________ 。
(5)当乙池中A(Fe)极的质量增加4.32g时,甲池中理论上消耗O2__________ mL(标准状况下)。

(1)请回答图中甲、乙两池的名称。甲池是
(2)请回答下列电极的名称:通入CH3OH的电极名称是
(3)写出电极反应式:通入O2的电极的电极反应式是
(4)乙池中反应的化学方程式为
(5)当乙池中A(Fe)极的质量增加4.32g时,甲池中理论上消耗O2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】依据事实,完成下列各题
(1)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,则乙醇燃烧的热化学方程式为_______________________________ 。
(2)有科技工作者利用稀土金属氧化物作为固体电解质制造出了甲醇空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。
①这个电池的正极发生的反应是______________________________ ;
负极发生的反应是_________________________________________ 。
②在稀土氧化物的固体电解质中,O2-的移动方向是_____________________________ 。
③甲醇可以在内燃机中燃烧直接产生动力推动机动车运行,而科技工作者要花费大量的精力研究甲醇燃料汽车。主要原因是_______________________________ 。
(1)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,则乙醇燃烧的热化学方程式为
(2)有科技工作者利用稀土金属氧化物作为固体电解质制造出了甲醇空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。
①这个电池的正极发生的反应是
负极发生的反应是
②在稀土氧化物的固体电解质中,O2-的移动方向是
③甲醇可以在内燃机中燃烧直接产生动力推动机动车运行,而科技工作者要花费大量的精力研究甲醇燃料汽车。主要原因是
您最近一年使用:0次



