名校
解题方法
1 . 下列各组物质:
① 和
和
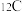 和
和
④ 和
和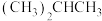
⑤癸烷和十六烷
⑥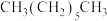 和
和
(1)互为同位素的是___________ 。
(2)互为同分异构体的是___________ 。
(3)互为同素异形体的是___________ 。
(4)互为同系物的是___________ 。
(5)同一种物质的是___________ 。
①
 和
和
②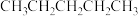 和
和
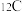 和
和
④
 和
和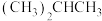
⑤癸烷和十六烷
⑥
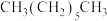 和
和
⑦ 和
和
(1)互为同位素的是
(2)互为同分异构体的是
(3)互为同素异形体的是
(4)互为同系物的是
(5)同一种物质的是
您最近一年使用:0次
名校
解题方法
2 . 油酸熔点为14℃,沸点为360℃,不溶于水,密度为0.89g•cm-3,其摩尔质量为282g•mol-1。其分子结构如图所示。_______ 。
(2)油酸分子式为_______ 。
(3)常温下,欲分离油酸和水的混合物,除烧杯、铁架台外,还需_______ 。
利用油膜法能近似测定分子直径和阿伏加德罗常数。先取0.5mL的油酸溶解于酒精中形成1L溶液。再取0.020mL上述溶液滴入水中,测得油酸分散的面积约为1.0×10-2m2。假设在水面上油酸呈单分子紧密排列,如图所示。_______ m。
(5)若把油酸分子近似为球体,根据球体的体积计算公式:V=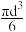 。计算本实验测定的阿伏加德罗常数(NA)约为
。计算本实验测定的阿伏加德罗常数(NA)约为_______ 。

| A.电子式 | B.结构式 | C.球棍模型 | D.空间填充模型 |
| A.C18H34O2 | B.C18H36O2 | C.C19H38O | D.C19H36O |
A. | B. | C. | D. |
利用油膜法能近似测定分子直径和阿伏加德罗常数。先取0.5mL的油酸溶解于酒精中形成1L溶液。再取0.020mL上述溶液滴入水中,测得油酸分散的面积约为1.0×10-2m2。假设在水面上油酸呈单分子紧密排列,如图所示。

| A.10-3 | B.10-6 | C.10-9 | D.10-12 |
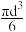 。计算本实验测定的阿伏加德罗常数(NA)约为
。计算本实验测定的阿伏加德罗常数(NA)约为
您最近一年使用:0次
3 . 已知CaF2的熔点为1402℃,可作电冶金的助熔剂。CaF2的晶胞图以及晶胞的投影图(晶胞所有面的投影均相同)。
(1)下列说法正确的是______ 。(不定项)
(2)已知CaF2的晶胞边长为5.4626×10-10m。则萤石的密度为______ g•cm-3。(保留两位小数)
(1)下列说法正确的是

| A.CaF2属于共价晶体 | B.晶胞中有4个Ca2+ |
| C.与Ca2+最近的F-有8个 | D.与F-最近的Ca2+有6个 |
(2)已知CaF2的晶胞边长为5.4626×10-10m。则萤石的密度为
您最近一年使用:0次
4 . 含NO 的废水可用黄铁矿(主要成分为FeS2)处理,在细菌作用下发生以下反应。
的废水可用黄铁矿(主要成分为FeS2)处理,在细菌作用下发生以下反应。
(1)请完成下列离子方程式______ 。
6NO +_______FeS2+_______H+=3N2↑+2Fe3++
+_______FeS2+_______H+=3N2↑+2Fe3++ _______+
_______+ _______
_______
(2)当上述反应生成标准状况6.72L气体时,转移电子数为______ 个。
 的废水可用黄铁矿(主要成分为FeS2)处理,在细菌作用下发生以下反应。
的废水可用黄铁矿(主要成分为FeS2)处理,在细菌作用下发生以下反应。(1)请完成下列离子方程式
6NO
 +_______FeS2+_______H+=3N2↑+2Fe3++
+_______FeS2+_______H+=3N2↑+2Fe3++ _______+
_______+ _______
_______(2)当上述反应生成标准状况6.72L气体时,转移电子数为
您最近一年使用:0次
5 . 铜的配合物在自然界中广泛存在,请回答下列问题:
(1)硫酸铜溶液中存在多种微粒,硫酸铜溶液呈蓝色的原因是其中存在配离子_______ (填化学式),配体中提供孤电子对的原子是_______ (填元素符号)。
(2)同学甲设计如下制备铜的配合物的实验:
①结合化学用语,用平衡移动原理解释试管c中浑浊液转变为深蓝色溶液的原因_______ 。
②由上述实验可得出以下结论:
结论1:配合物的形成与_______ 、_______ 有关;
结论2:结合实验,试管b、c中深蓝色配离子的稳定性强弱顺序为:_______ >_______ (填化学式)。
③实验结束后,向c试管中加入乙醇,并用玻璃棒摩擦试管壁,析出深蓝色晶体[Cu(NH3)4]SO4·H2O,解释析出晶体的原因:_______ 。
(1)硫酸铜溶液中存在多种微粒,硫酸铜溶液呈蓝色的原因是其中存在配离子
(2)同学甲设计如下制备铜的配合物的实验:

①结合化学用语,用平衡移动原理解释试管c中浑浊液转变为深蓝色溶液的原因
②由上述实验可得出以下结论:
结论1:配合物的形成与
结论2:结合实验,试管b、c中深蓝色配离子的稳定性强弱顺序为:
③实验结束后,向c试管中加入乙醇,并用玻璃棒摩擦试管壁,析出深蓝色晶体[Cu(NH3)4]SO4·H2O,解释析出晶体的原因:
您最近一年使用:0次
名校
解题方法
6 . 科学家从延胡索中提取出一种有机物M,可用作染料的媒染剂或食品调味料。某小组展开对其分子组成的研究:
(1)经燃烧分析实验测定,M完全燃烧的产物仅有 和
和 ,分子中碳元素的质量分数为41.38%,氢元素的质量分数为3.45%,由此可知M实验式为
,分子中碳元素的质量分数为41.38%,氢元素的质量分数为3.45%,由此可知M实验式为___________ 。
(2)小组成员利用质谱法测定M的相对分子质量为116,则其分子式为___________ 。
(3)M的红外光谱图如下,若M中仅含有2种官能团,则官能团的名称是___________ 、___________ 。___________ 。___________ (填选项序号)。
a.与丙烯互为同系物
b.其存在顺反异构体
c.分子中的碳原子的杂化方式均为sp2
d.分子中所有的碳原子处于同一平面内
(1)经燃烧分析实验测定,M完全燃烧的产物仅有
 和
和 ,分子中碳元素的质量分数为41.38%,氢元素的质量分数为3.45%,由此可知M实验式为
,分子中碳元素的质量分数为41.38%,氢元素的质量分数为3.45%,由此可知M实验式为(2)小组成员利用质谱法测定M的相对分子质量为116,则其分子式为
(3)M的红外光谱图如下,若M中仅含有2种官能团,则官能团的名称是


a.与丙烯互为同系物
b.其存在顺反异构体
c.分子中的碳原子的杂化方式均为sp2
d.分子中所有的碳原子处于同一平面内
您最近一年使用:0次
名校
解题方法
7 . 学好有机化学,从认识有机物的组成和结构开始。请用所学知识回答下列问题:
(1) 的化学名称为
的化学名称为_______ ,含有的手性碳原子数为_______ ,其与足量 发生加成反应后得到的产物
发生加成反应后得到的产物_______ (填“是”或“不是”)手性分子。
(2) 的一氯代物有
的一氯代物有_______ 种,其与酸性 溶液发生反应后得到的有机产物为
溶液发生反应后得到的有机产物为_______ (写结构简式)。
(3) 分子中最多有
分子中最多有_______ 个原子共平面。
(4) 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ , 该物质与足量
该物质与足量 溶液反应,生成
溶液反应,生成 的体积(标准状况下)为
的体积(标准状况下)为_______ L。
(1)
 的化学名称为
的化学名称为 发生加成反应后得到的产物
发生加成反应后得到的产物(2)
 的一氯代物有
的一氯代物有 溶液发生反应后得到的有机产物为
溶液发生反应后得到的有机产物为(3)
 分子中最多有
分子中最多有(4)
 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为 该物质与足量
该物质与足量 溶液反应,生成
溶液反应,生成 的体积(标准状况下)为
的体积(标准状况下)为
您最近一年使用:0次
昨日更新
|
15次组卷
|
2卷引用:河北省邢台市邢襄联盟2023-2024学年高二下学期5月第三次月考化学试题
名校
8 . 请按要求完成下列方程式的书写。
(1) 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(2)金属钠投入氯化钠溶液_______ 。
(3)酸性条件下 与
与 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:_______ 。
(4)氢氧化铁受热分解:_______ 。
(1)
 与
与 反应的化学方程式:
反应的化学方程式:(2)金属钠投入氯化钠溶液
(3)酸性条件下
 与
与 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:(4)氢氧化铁受热分解:
您最近一年使用:0次
名校
解题方法
9 . 化学电源是人类生产和生活的重要能量来源之一,回答下列问题。
(1)为了探究化学反应中的能量变化,某同学设计了如下两个实验。___________ (填序号)。
A.图1和图2的气泡均产生在锌棒表面
B.图1中温度计的示数高于图2的示数
C.图2中产生气体的速度比1快
D.图1和图2中温度计的示数相等,且均高于室温
②图②装置中,正极的电极反应方程式为___________ 。
(2)将反应2Fe3++Fe=3Fe2+设计成原电池装置,负极的电极反应方程式为___________ ,离子导体为___________ 。
(3)甲烷碱性燃料电池以KOH溶液为电解质溶液,电池反应为CH4+2O2+2OH- CO
CO +3H2O,该电池的负极电极反应方程式为
+3H2O,该电池的负极电极反应方程式为___________ ,K+向___________ 极(填正或负)移动,若电路中通过0.4mol电子,则理论上消耗甲烷的体积为(标况)___________ 。
(1)为了探究化学反应中的能量变化,某同学设计了如下两个实验。
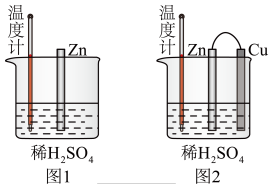
A.图1和图2的气泡均产生在锌棒表面
B.图1中温度计的示数高于图2的示数
C.图2中产生气体的速度比1快
D.图1和图2中温度计的示数相等,且均高于室温
②图②装置中,正极的电极反应方程式为
(2)将反应2Fe3++Fe=3Fe2+设计成原电池装置,负极的电极反应方程式为
(3)甲烷碱性燃料电池以KOH溶液为电解质溶液,电池反应为CH4+2O2+2OH-
 CO
CO +3H2O,该电池的负极电极反应方程式为
+3H2O,该电池的负极电极反应方程式为
您最近一年使用:0次
名校
解题方法
10 . 写出下列反应的离子方程式。
(1)Ba(OH)2溶液和Na2SO4溶液反应:___________ 。
(2)CaCO3溶液和盐酸溶液反应:___________ 。
(3)CuO和稀硫酸反应:___________ 。
(4)Na2CO3和醋酸溶液反应:___________ 。
(5)Cu(OH)2和稀硝酸反应:___________ 。
(1)Ba(OH)2溶液和Na2SO4溶液反应:
(2)CaCO3溶液和盐酸溶液反应:
(3)CuO和稀硫酸反应:
(4)Na2CO3和醋酸溶液反应:
(5)Cu(OH)2和稀硝酸反应:
您最近一年使用:0次



