21-22高一下·全国·单元测试
解题方法
1 . 硝酸( )
)
(1)物理性质:无色、_______ 气味、_______ 挥发液体,能与水以任意比例互溶,常用浓硝酸的质量分数大约为69%。
(2)化学性质
硝酸为_______ 酸,具有以下性质:
①具有酸的通性;
②不稳定性:_______ ;
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出_______ 。
A.与金属反应:
铜与浓硝酸:_______ ;
铜与稀硝酸:_______ ;
银与浓硝酸:_______ ;
常温下浓硝酸与铁、铝发生_______ 。
B.与非金属反应:
碳与浓硝酸:_______ 。
C.与其他还原剂反应,如H2S、SO2、Fe2+等。
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,_______ (不能用强热和稀硫酸);
②工业制法:
氨的催化氧化法:_______ ;_______ ;_______ ;
尾气处理:_______ (用NaOH溶液吸收尾气)。
(4)用途:_______ 等。
 )
)(1)物理性质:无色、
(2)化学性质
硝酸为
①具有酸的通性;
②不稳定性:
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出
A.与金属反应:
铜与浓硝酸:
铜与稀硝酸:
银与浓硝酸:
常温下浓硝酸与铁、铝发生
B.与非金属反应:
碳与浓硝酸:
C.与其他还原剂反应,如H2S、SO2、Fe2+等。
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,
②工业制法:
氨的催化氧化法:
尾气处理:
(4)用途:
您最近一年使用:0次
21-22高一下·全国·单元测试
2 . 乙醇化学性质
(1)与Na反应——置换反应
化学方程式为_______ ,与水和Na反应相比反应剧烈程度缓和得多。
(2)氧化反应
①燃烧
化学方程式:CH3CH2OH+3O2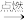
_______ 。
现象:产生_______ 色火焰,放出_______ 热。
②催化氧化:催化剂可以是_______ 或_______ 。
化学方程式:2CH3CH2OH+O2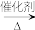
_______ 。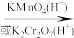
_______ 。
(1)与Na反应——置换反应
化学方程式为
(2)氧化反应
①燃烧
化学方程式:CH3CH2OH+3O2
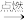
现象:产生
②催化氧化:催化剂可以是
化学方程式:2CH3CH2OH+O2
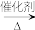
乙醛的结构简式为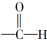 或
或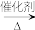
您最近一年使用:0次
3 . 海水水资源的利用
(1)海水水资源利用,主要包括_______ 和直接利用海水进行循环冷却等。
(2)海水淡化:通过从海水中提取淡水或从海水中把_______ 分离出去,都可以达到淡化海水的目的。海水淡化的方法主要有_______ 、_______ 等。其中_______ 的历史最久,技术和工艺也比较成熟,但成本较高。
(1)海水水资源利用,主要包括
(2)海水淡化:通过从海水中提取淡水或从海水中把
您最近一年使用:0次
4 . 乙醇俗称_______ ,_______ 、有特殊香味的_______ ,密度比水的_______ ,_______ 挥发,与水以任意比例互溶,是优良的有机溶剂。
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
5 . 同分异构体
(1)概念
①同分异构现象:化合物具有相同的___________ ,但具有不同___________ 的现象。同分异构现象是有机物种类繁多的重要原因之一。
②同分异构体:具有___________ 的化合物互称为___________ 。
(2)写出C4H10的同分异构体:___________ 和___________ ,其名称分别为___________ 和___________ 。
(3)戊烷的同分异构体有___________ 种,己烷的同分异构体有___________ 种。
(1)概念
①同分异构现象:化合物具有相同的
②同分异构体:具有
(2)写出C4H10的同分异构体:
(3)戊烷的同分异构体有
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
6 . 烷烃的结构
(1)甲烷的结构
甲烷的空间结构是___________ 结构,___________ 原子位于正四面体的中心,4个___________ 原子位于4个顶点上。分子中的4个C—H的长度和强度___________ ,相互之间的夹角___________ ,为109°28′。
(2)空间示意图是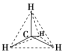 。甲烷的
。甲烷的___________ 模型为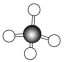 ,空间填充模型为
,空间填充模型为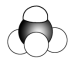 。
。
(1)甲烷的结构
甲烷的空间结构是
(2)空间示意图是
 。甲烷的
。甲烷的 ,空间填充模型为
,空间填充模型为 。
。
您最近一年使用:0次
22-23高一下·全国·单元测试
解题方法
7 . 金属冶炼的方法:
(1)加热分解法:
①制Hg: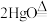
_______ 。
②制Ag: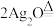
_______ 。
(2)电解法:
①制Mg: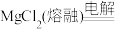
_______ 。
②制Al: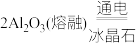
_______ 。
③制Na: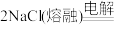
_______ 。
(3)热还原法:
①常用还原剂有_______ 氢气、铝等。
②高炉炼铁:CO还原Fe2O3的化学方程式为
_______ 。
③铝热反应:Al还原Fe2O3的化学方程式为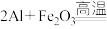
_______ 。
(1)加热分解法:
①制Hg:
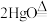
②制Ag:
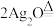
(2)电解法:
①制Mg:
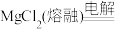
②制Al:
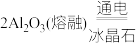
③制Na:
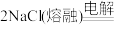
(3)热还原法:
①常用还原剂有
②高炉炼铁:CO还原Fe2O3的化学方程式为

③铝热反应:Al还原Fe2O3的化学方程式为
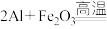
您最近一年使用:0次
22-23高一下·全国·单元测试
8 . 1.海水的化学资源利用
(1)海水中的化学元素:_______ 。
(2)海水中化学资源的利用
①从海水中提取_______ 和重水,用于_______ 开发。
②开发_______ 、_______ 等新型能源。
(1)海水中的化学元素:
(2)海水中化学资源的利用

①从海水中提取
②开发
您最近一年使用:0次
23-24高一下·全国·单元测试
解题方法
9 . 化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是___________(填字母,下同)。
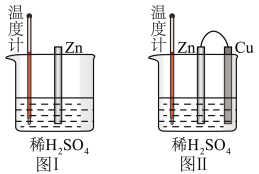
(2)为了探究化学反应中的能量变化,某兴趣小组设计了如下两个实验(如图所示)。试回答下列问题:
①有关反应一段时间后的实验现象,下列说法正确的是___________ 。
A.图I中温度计的示数高于图II的示数
B.图I中锌片是负极,图II中铜片是正极
C.图I和图II的气泡均产生于锌棒表面
D.图II中产生气体的速率比I慢
E.图I和图II中溶液酸性均增强
F.图II的外电路中电流方向Zn→Cu。
②在图II实验中,兴趣小组观察到的实验现象是___________ ,写出图II实验中铜上电极反应式___________ 。
③在图II实验中,如果把硫酸换成硫酸铜溶液,请写出电池总反应的离子方程式:___________ ;当电路中转移0.25mol电子时,消耗负极材料的质量为___________ g[M(Zn)=65g/mol]。
(3)根据原电池原理可以制造化学电池。如:电动汽车上用的铅蓄电池是由一组海绵状铅板和另一组结构相似的充满二氧化铅的铅板做为两电极,用H2SO4作电解质溶液构成。放电时,电池总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。试写出放电时正极的电极反应式:___________ 。
(4)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极,CH3OH为燃料,采用氢氧化钠溶液为电解液,电池工作时消耗1molCH3OH,则电路中通过___________ mol电子。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是___________(填字母,下同)。
| A.KOH+HCl=KCl+H2O | B.Cu+Fe3+=Fe2++Cu2+ |
| C.Na2O+H2O=2NaOH | D.Fe+H2SO4=FeSO4+H2↑ |
(2)为了探究化学反应中的能量变化,某兴趣小组设计了如下两个实验(如图所示)。试回答下列问题:
①有关反应一段时间后的实验现象,下列说法正确的是

A.图I中温度计的示数高于图II的示数
B.图I中锌片是负极,图II中铜片是正极
C.图I和图II的气泡均产生于锌棒表面
D.图II中产生气体的速率比I慢
E.图I和图II中溶液酸性均增强
F.图II的外电路中电流方向Zn→Cu。
②在图II实验中,兴趣小组观察到的实验现象是
③在图II实验中,如果把硫酸换成硫酸铜溶液,请写出电池总反应的离子方程式:
(3)根据原电池原理可以制造化学电池。如:电动汽车上用的铅蓄电池是由一组海绵状铅板和另一组结构相似的充满二氧化铅的铅板做为两电极,用H2SO4作电解质溶液构成。放电时,电池总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。试写出放电时正极的电极反应式:
(4)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极,CH3OH为燃料,采用氢氧化钠溶液为电解液,电池工作时消耗1molCH3OH,则电路中通过
您最近一年使用:0次
名校
10 . I.氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2.某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
(1)将20mLNO2和NO的混合气体通入倒立于水槽且盛满水的试管中,充分反应后试管中剩余10mL气体,则原混合气体中NO2与NO的体积比为___________。
II.氨气与二氧化氮的反应:将收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图所示装置进行实验(加热装置和夹持装置省略)。___________ ,Y管中反应的化学方程式为___________ 。
(3)Z的作用为___________ 。
III.硝酸和硝酸盐是化工中的重要原料
(4)Cu(NO3)2受热易分解,分解反应为2Cu(NO3)2 CuO+4NO2↑+O2↑。某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃。则下列判断正确的是___________。
CuO+4NO2↑+O2↑。某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃。则下列判断正确的是___________。
(5)1.52g铜镁合金完全溶解于足量浓硝酸中,得到标况下NO2和N2O4的混合气体1120mL,向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀;则该合金中n(Cu):n(Mg)=______ ;NO2和N2O4的混合气体中,NO2的体积分数为___________ 。
(1)将20mLNO2和NO的混合气体通入倒立于水槽且盛满水的试管中,充分反应后试管中剩余10mL气体,则原混合气体中NO2与NO的体积比为___________。
| A.1∶1 | B.1∶3 | C.3∶1 | D.2∶1 |
II.氨气与二氧化氮的反应:将收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图所示装置进行实验(加热装置和夹持装置省略)。

(3)Z的作用为
III.硝酸和硝酸盐是化工中的重要原料
(4)Cu(NO3)2受热易分解,分解反应为2Cu(NO3)2
 CuO+4NO2↑+O2↑。某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃。则下列判断正确的是___________。
CuO+4NO2↑+O2↑。某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃。则下列判断正确的是___________。| A.产物中有氧气,所以木条复燃 | B.不能确定NO2是否助燃 |
| C.NO2肯定也能助燃 | D.NO2肯定不能助燃 |
(5)1.52g铜镁合金完全溶解于足量浓硝酸中,得到标况下NO2和N2O4的混合气体1120mL,向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀;则该合金中n(Cu):n(Mg)=
您最近一年使用:0次
2023-12-20更新
|
1158次组卷
|
2卷引用:第五章 化工生产中的重要非金属元素 单元测试



