1 . 为除去粗盐中的 、
、 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
 、
、 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
| A.步骤①:根据粗盐的质量和溶解度来确定烧杯和量筒的规格 |
B.步骤②~④: 、 、 和 和 的滴加“顺序”和“量”不可调整 的滴加“顺序”和“量”不可调整 |
C.步骤⑥:用玻璃棒搅拌滤液,直到没有气泡冒出,且 试纸检验滤液呈碱性 试纸检验滤液呈碱性 |
| D.步骤①~⑦:需要的实验用品有分液漏斗、蒸发皿、玻璃棒、陶土网和胶头滴管 |
您最近半年使用:0次
名校
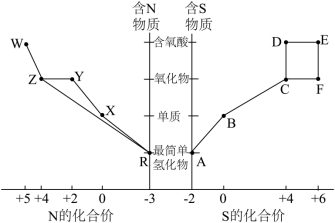
2 . I.元素的“价—类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。
(1)写出实验室利用两种固体物质加热制备物质R的化学方程式___________ 。
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是___________ 。
(3)写出物质E的浓溶液与碳单质反应的化学方程式:___________ 。
(4)写出物质Z与水反应的离子方程式:___________ ,当反应消耗0.3mol物质Z时,转移电子数为___________ 。
(5)下列有关图中所示含N、S物质的叙述,正确的是___________(填标号)。
II.粗盐中含有泥沙及 、
、 、
、 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程: 溶液、
溶液、 溶液等药品以及必备的实验仪器若干。请回答下列问题:
溶液等药品以及必备的实验仪器若干。请回答下列问题:
(6)操作③按a、b、c顺序依次加入过量的试剂。若a为NaOH溶液,则c为___________ 。
(7)加盐酸调溶液pH的目的是___________ 。
(1)写出实验室利用两种固体物质加热制备物质R的化学方程式
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是
(3)写出物质E的浓溶液与碳单质反应的化学方程式:
(4)写出物质Z与水反应的离子方程式:
(5)下列有关图中所示含N、S物质的叙述,正确的是___________(填标号)。
| A.在催化剂的作用下,R可将Y、Z还原为X |
| B.图中所示的物质中,只有W、D、E属于电解质 |
| C.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生 |
| D.Z、C、F均能与NaOH溶液反应,都是酸性氧化物 |
II.粗盐中含有泥沙及
 、
、 、
、 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程: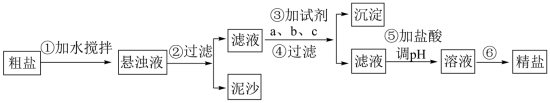
 溶液、
溶液、 溶液等药品以及必备的实验仪器若干。请回答下列问题:
溶液等药品以及必备的实验仪器若干。请回答下列问题:(6)操作③按a、b、c顺序依次加入过量的试剂。若a为NaOH溶液,则c为
(7)加盐酸调溶液pH的目的是
您最近半年使用:0次
名校
解题方法
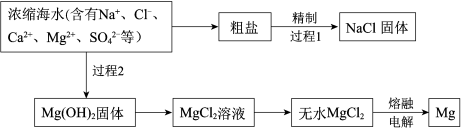
3 . 浩瀚的海洋中蕴藏着丰富的资源。
过程1除去粗盐中的Ca2+、Mg2+、SO 杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液过滤除去沉淀,再加入适量的盐酸。
杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液过滤除去沉淀,再加入适量的盐酸。
①加入沉淀剂的顺序正确的是___________ (填序号)。
A.abc B.bac C.cba
②加入适量盐酸,反应的离子方程式有2H++CO =H2O+CO2↑和
=H2O+CO2↑和___________ 。
(2)海水提镁。
过程2中加入的试剂是___________ 。由无水MgCl2获得Mg的化学方程式是___________ 。
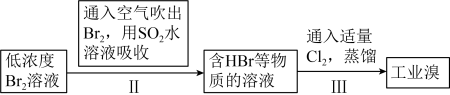
(3)海水提溴。
主要工业生产流程如下图所示:___________ 。
②吸收塔中,A吸收了Br2后的溶液中含有Br‒和BrO ,则A是
,则A是___________ (填序号)。
a.NaCl溶液 b.Na2CO3溶液 c.SO2气体
③从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是___________ 。
过程1除去粗盐中的Ca2+、Mg2+、SO
 杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液过滤除去沉淀,再加入适量的盐酸。
杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液过滤除去沉淀,再加入适量的盐酸。①加入沉淀剂的顺序正确的是
A.abc B.bac C.cba
②加入适量盐酸,反应的离子方程式有2H++CO
 =H2O+CO2↑和
=H2O+CO2↑和(2)海水提镁。
过程2中加入的试剂是
(3)海水提溴。
主要工业生产流程如下图所示:
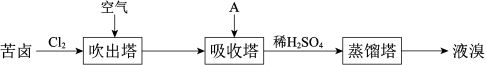
②吸收塔中,A吸收了Br2后的溶液中含有Br‒和BrO
 ,则A是
,则A是a.NaCl溶液 b.Na2CO3溶液 c.SO2气体
③从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是
您最近半年使用:0次
解题方法
4 . 从海水中可提取多种化工原料,下图是工业上对海水的几项综合利用的示意图。试回答下列问题: 的化学方程式:
的化学方程式:___________ ,___________ ;
(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?___________ ;
(3)电解无水 可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为
可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为___________ ;
(4)海边盐碱地(含较多 、
、 )不利于植物生长,盐碱地产生碱性的原因:
)不利于植物生长,盐碱地产生碱性的原因:___________ (用离子方程式表示);农业上用石膏降低其碱性的反应原理:___________ (用化学方程式表示);
(5)用海滩上的贝壳制 ,而不从异地山中开凿石灰石制取,主要考虑到
,而不从异地山中开凿石灰石制取,主要考虑到___________ 问题。

 的化学方程式:
的化学方程式:(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?
(3)电解无水
 可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为
可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为(4)海边盐碱地(含较多
 、
、 )不利于植物生长,盐碱地产生碱性的原因:
)不利于植物生长,盐碱地产生碱性的原因:(5)用海滩上的贝壳制
 ,而不从异地山中开凿石灰石制取,主要考虑到
,而不从异地山中开凿石灰石制取,主要考虑到
您最近半年使用:0次
名校
5 . 海水中有丰富的资源,海底有丰富的矿藏、石油、天然气等,海水中还含有大量的电解质,它们电离产生 、
、 、
、 、
、 、
、 、
、 、
、 等,都是重要资源。开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
等,都是重要资源。开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
(1)写出步骤②、⑦、⑧分离提纯的方法:
②___________ ,⑦___________ ,⑧___________ 。
(2)步骤⑦分离提纯过程中需要选用的玻璃仪器除烧杯外,还需要的仪器是___________ 。
(3)步骤③的条件是通直流电,其离子方程式为___________ 。
(4)初步提纯后的粗盐中含有 、
、 、
、 等杂质,精制时所用的试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,下列试剂添加顺序合理的是___________。
等杂质,精制时所用的试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,下列试剂添加顺序合理的是___________。
(5)流程⑥将溴单质从水溶液中分离出来是基于溴单质具有挥发性。对粗溴一般做如下处理:___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 等,都是重要资源。开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
等,都是重要资源。开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
(1)写出步骤②、⑦、⑧分离提纯的方法:
②
(2)步骤⑦分离提纯过程中需要选用的玻璃仪器除烧杯外,还需要的仪器是
(3)步骤③的条件是通直流电,其离子方程式为
(4)初步提纯后的粗盐中含有
 、
、 、
、 等杂质,精制时所用的试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,下列试剂添加顺序合理的是___________。
等杂质,精制时所用的试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,下列试剂添加顺序合理的是___________。| A.②③④① | B.③④②① | C.④③②① | D.③②④① |
(5)流程⑥将溴单质从水溶液中分离出来是基于溴单质具有挥发性。对粗溴一般做如下处理:
您最近半年使用:0次
名校
6 . 地球上的大部分水是以海水形式存在的,海水淡化可以缓解淡水资源不足。下列有关海水淡化的方法在原理上可行的是
①加明矾使海水中的盐分沉淀而淡化 ②蒸馏海水,将水蒸气冷凝
③将海水暴晒,滤掉析出的盐 ④将海水加压,使水分子通过半透膜以滤去盐分
①加明矾使海水中的盐分沉淀而淡化 ②蒸馏海水,将水蒸气冷凝
③将海水暴晒,滤掉析出的盐 ④将海水加压,使水分子通过半透膜以滤去盐分
| A.①② | B.②③ | C.①③ | D.②④ |
您最近半年使用:0次
名校
7 . 我国海洋资源十分丰富。下列物质是从海水中提取制备并用到电解法的是
| A.溴单质、碘单质 | B.粗盐、淡水 | C.纯碱、氢气 | D.钠、镁 |
您最近半年使用:0次
解题方法
8 . 浩瀚的海洋是一个巨大的物质宝库,工业上常用浓缩海水提取溴,工艺流程如图。

下列说法正确的是

下列说法正确的是
| A.海水晒盐是化学变化 |
| B.步骤②中体现了溴易升华的性质 |
C.步骤③反应的离子方程式为  |
| D.①~④的目的是富集溴元素 |
您最近半年使用:0次
名校
解题方法
9 . 食盐是日常生活的必需品,也是重要的化工原料。粗盐常含有少量 、
、 、
、 等杂质离子。实验室提纯NaCl的流程如下:
等杂质离子。实验室提纯NaCl的流程如下:

下列说法错误 的是
 、
、 、
、 等杂质离子。实验室提纯NaCl的流程如下:
等杂质离子。实验室提纯NaCl的流程如下:
下列说法
| A.试剂a为BaCl2,试剂b为Na2CO3 | B.流程图中,操作x为过滤 |
C.m g粗盐提纯后得到n g NaCl固体,则 | D.国家规定的加碘食盐中含KIO3 |
您最近半年使用:0次
10 . 海洋是巨大的化学资源宝库,含有80多种元素。下图为利用海水制备部分物质的过程(已知:二氧化硫具有较强的还原性)。下列说法正确的是

| A.制取NaHCO3的反应是利用物质之间溶解度的差异实现的 |
| B.用澄清的石灰水可鉴别NaHCO3溶液和Na2CO3溶液 |
| C.在第③、④、⑤反应中,溴元素经历了被还原、被氧化、被还原的过程 |
| D.工业可利用氯碱工业原理制备金属钠 |
您最近半年使用:0次



