1 . 海洋是一个巨大的化学资源宝库,其中含量较高的离子有
A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
2 . 海水综合利用符合可持续发展的原则,其联合工业体系(部分)如图所示,下列说法中正确的是


| A.①工业上采用电解熔融氧化镁的方法冶炼镁 |
| B.②海水淡化主要有蒸馏法、电渗析法和离子交换法 |
| C.③海水提溴工艺中,分离出溴的方法是用酒精萃取 |
| D.④的主要产品之一与石灰乳反应可得漂白液 |
您最近一年使用:0次
名校
3 . 用利用海水可以提取溴和镁,提取过程如下:
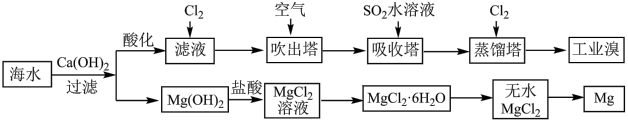
(1)从 溶液中得到
溶液中得到 晶体的主要实验操作是
晶体的主要实验操作是___________ 、洗涤、烘干。
(2)用 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为___________ 。
(3)海水提溴要经过“空气吹出、 吸收、通入氯气后再蒸馏”,其目的是
吸收、通入氯气后再蒸馏”,其目的是___________ 。
(4)已知海水中 含量为
含量为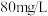 ,依据上述流程,若将
,依据上述流程,若将 海水中的溴元素转化为工业溴,至少需要标准状况下
海水中的溴元素转化为工业溴,至少需要标准状况下 的体积为
的体积为___________ L(忽略 溶解)。
溶解)。

(1)从
 溶液中得到
溶液中得到 晶体的主要实验操作是
晶体的主要实验操作是(2)用
 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为(3)海水提溴要经过“空气吹出、
 吸收、通入氯气后再蒸馏”,其目的是
吸收、通入氯气后再蒸馏”,其目的是(4)已知海水中
 含量为
含量为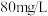 ,依据上述流程,若将
,依据上述流程,若将 海水中的溴元素转化为工业溴,至少需要标准状况下
海水中的溴元素转化为工业溴,至少需要标准状况下 的体积为
的体积为 溶解)。
溶解)。
您最近一年使用:0次
名校
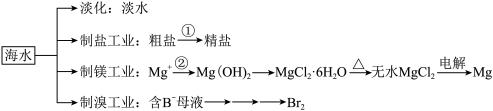
4 . 海水中有非常丰富的化学资源,从海水中可提取多种化工原料。某工厂对海水资源综合开发利用的部分工艺流程如图所示,回答下列问题:_______ 等(任填一种即可)。
(2)由海水晒制的粗盐中含有 、
、 、
、 等离子,步骤①中所加试剂及有关操作的先后顺序为(试剂写化学式)
等离子,步骤①中所加试剂及有关操作的先后顺序为(试剂写化学式)_______ 、_______ 、 、过滤、
、过滤、 。
。
(3)步骤②中加入的物质是_______ (填物质名称)。
(4)利用下图所示装置模拟工业上从母液中提取溴,在B瓶中得到较浓的溴水。 至反应完全,发生反应的的离子方程式是
至反应完全,发生反应的的离子方程式是_______ ;再关闭a、c,打开b、d、e,由b向A中鼓入足量热空气,同时由e向B中通入足量_______ ;关闭b、e,打开a,再由a向B中缓缓鼓入足量 ,即可在B中得到较浓的溴水。
,即可在B中得到较浓的溴水。
(2)由海水晒制的粗盐中含有
 、
、 、
、 等离子,步骤①中所加试剂及有关操作的先后顺序为(试剂写化学式)
等离子,步骤①中所加试剂及有关操作的先后顺序为(试剂写化学式) 、过滤、
、过滤、 。
。(3)步骤②中加入的物质是
(4)利用下图所示装置模拟工业上从母液中提取溴,在B瓶中得到较浓的溴水。
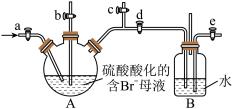
 至反应完全,发生反应的的离子方程式是
至反应完全,发生反应的的离子方程式是 ,即可在B中得到较浓的溴水。
,即可在B中得到较浓的溴水。
您最近一年使用:0次
2023-07-13更新
|
79次组卷
|
2卷引用:黑龙江省大兴安岭实验中学2023-2024学年高二上学期开学考试化学试卷
名校
5 . 海水中含有丰富的资源。如图是由海水制取某些产品的流程,下列有关说法中正确的是
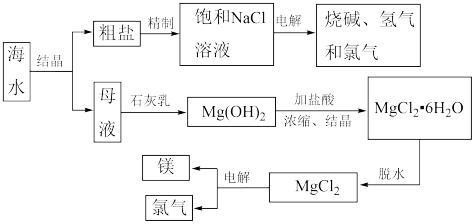

| A.由海水制取粗盐的方法是降温结晶 |
B.可用 溶液除去粗盐中的 溶液除去粗盐中的 |
C.石灰乳就是 溶液 溶液 |
D.电解 的反应属于氧化还原反应 的反应属于氧化还原反应 |
您最近一年使用:0次
2023-06-11更新
|
151次组卷
|
2卷引用:黑龙江省哈尔滨市第六中学2022-2023学年高一下学期期中考试化学试题
6 . 下列生产过程中属于物理变化的是
| A.海水晒盐 | B.粮食酿酒 | C.石油裂化 | D.海水中提取金属Mg |
您最近一年使用:0次
名校
解题方法
7 . 已知MgO、MgCl2的熔点分别为2800 ℃、714 ℃,将MgO、MgCl2加热熔融后通电电解,都可得到金属镁。海水中含有MgCl2,工业上从海水中提取镁,正确的方法是
A.海水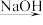 Mg(OH)2 Mg(OH)2 Mg Mg |
B.海水 MgCl2溶液 MgCl2溶液 MgCl2(熔融) MgCl2(熔融)  Mg Mg |
C.海水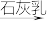 Mg(OH)2 Mg(OH)2 MgO MgO Mg Mg |
D.海水 Mg(OH)2 Mg(OH)2 MgCl2溶液 MgCl2溶液 MgCl2(熔融) MgCl2(熔融) Mg Mg |
您最近一年使用:0次
2022-12-02更新
|
401次组卷
|
5卷引用:黑龙江省勃利县高级中学2022-2023学年高一下学期5月月考化学试题
黑龙江省勃利县高级中学2022-2023学年高一下学期5月月考化学试题四川省成都市蒲江县蒲江中学2020-2021学年高二上学期开学考试化学试题(已下线)8.1.2 海水资源的开发利用(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)课中-8.1.1 金属矿物 海水资源的开发利用-人教2019必修第二册天津市实验中学滨海学校黄南民族班2021-2022学年高三上学期期中质量监测化学试题
名校
8 . 南海是一个巨大的资源宝库,海水开发利用的部分过程如图所示,下列说法错误的是

| A.物质X可以选用CaO |
| B.操作1中玻璃棒的作用是引流 |
| C.第①步中,蒸发结晶、高温烘干可以得到干燥的MgCl2·6H2O固体 |
D.第②步反应的离子方程式为:Br2+SO2+2H2O=SO +2Br-+4H+ +2Br-+4H+ |
您最近一年使用:0次
2022-11-09更新
|
186次组卷
|
6卷引用:黑龙江省龙西北名校联合体2023-2024学年高三上学期期中考试化学试题
名校
9 . 下列有关说法正确的是
| A.必须通过化学变化才能从海水中获得食盐 |
| B.海水中的溴、碘可用四氯化碳直接萃取得到 |
| C.海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等 |
| D.海水水资源的利用只有海水淡化 |
您最近一年使用:0次
名校
10 . 利用海水能够提取溴和镁,提取过程如下:
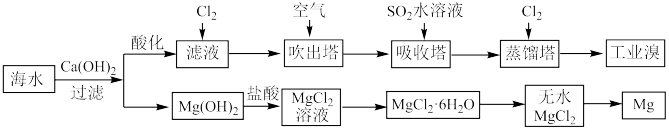
(1)提取溴的过程中,经过2次Br- →Br2转化的目的是_______ , 蒸馏塔中发生反应的离子方程式是_______ 。向溴水中加入CCl4,充分振荡、静置后Br2的CCl4溶液在_______ (上或下)层。
(2)从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作_______ 、_______ 、过滤、洗涤、干燥(在HCl气流的保护下);由无水氯化镁得到镁的化学方程式是_______ 。
(3)据上述流程,将20 m3海水中溴元素(海水中Br-离子含量为64 mg·L-1)转化为工业溴,整个流程中至少需要标准状况下Cl2的体积为_______ L (忽略Cl2溶解)。

(1)提取溴的过程中,经过2次Br- →Br2转化的目的是
(2)从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作
(3)据上述流程,将20 m3海水中溴元素(海水中Br-离子含量为64 mg·L-1)转化为工业溴,整个流程中至少需要标准状况下Cl2的体积为
您最近一年使用:0次



