名校
1 . 2023年8月14日13时,福岛核污染水开始排入海洋。下列有关说法正确的是
| A.核污染水在海洋这种庞大的分散系中不会产生较大危害 |
B.核污染水中的放射性 (相对原子质量为3)与 (相对原子质量为3)与 (相对原子质量为1)的摩尔质量相同 (相对原子质量为1)的摩尔质量相同 |
| C.人类可以从海洋中提取大量Na、Cl等重要元素 |
| D.向海水中加活性炭可以将海水淡化 |
您最近一年使用:0次
2 . 海洋中的化学资源具有巨大的开发潜力,海水的综合利用示意图如下,下列有关说法正确的是
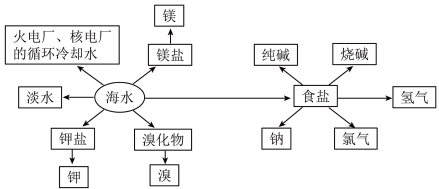
A.向 的食盐水中先通入NH3,再通入CO2即可析出小苏打进而制备纯碱 的食盐水中先通入NH3,再通入CO2即可析出小苏打进而制备纯碱 |
| B.海水提取溴采用先吹出再吸收的目的是提高溴的浓度 |
| C.制镁过程中可直接蒸发MgCl2溶液制备无水MgCl2 |
| D.火电厂利用物质燃烧产生的热能直接转化为电能来实现火力发电 |
您最近一年使用:0次
2023-12-31更新
|
133次组卷
|
3卷引用:河南省濮阳市油田第一中学2023-2024学年高三上学期第五次考试理科综合试题-高中化学
河南省濮阳市油田第一中学2023-2024学年高三上学期第五次考试理科综合试题-高中化学浙江省北斗星盟2024届高三上学期12月联考-化学试题 (已下线)压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
名校
3 . 粗盐中常含有杂质 、
、 和
和 ,为将杂质除尽设计如下步骤:
,为将杂质除尽设计如下步骤:
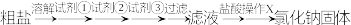
下列有关说法中,正确的是
 、
、 和
和 ,为将杂质除尽设计如下步骤:
,为将杂质除尽设计如下步骤: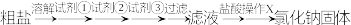
下列有关说法中,正确的是
A.试剂③一定不是 溶液 溶液 |
| B.过滤所得沉淀中只含有三种成分 |
| C.操作X为降温结晶 |
D.加稀盐酸时,首先发生反应 |
您最近一年使用:0次
2023-11-08更新
|
68次组卷
|
2卷引用:河南省周口市项城市2023-2024学年高三上学期11月期中联考化学试题
解题方法
4 . 下列有关物质的工业制备说法不正确的是
| A.氨的催化氧化法制备硝酸 | B.煅烧黄铁矿(FeS2)生产硫酸 |
| C.氯气与石灰乳制取漂白粉 | D.冷却结晶法提取海水中的食盐 |
您最近一年使用:0次
名校
解题方法
5 . 常言道:“一方水土养一方人”,广东省作为我国大陆南端的沿海省份,非常重视海水资源的综合利用。下列物质不需要通过化学变化就能够从海水中大量获得的是
| A.粗盐 | B.碘 | C.苛性钠 | D.金属镁 |
您最近一年使用:0次
6 . 海洋中有丰富的食品、矿产、能源、药物和水产资源等,海水的综合利用如图所示。下列有关说法正确的是
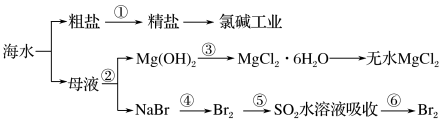

| A.含氮、磷的大量废水排入海洋,易引发赤潮 |
B.第③步中加入盐酸溶解得到 溶液,再直接蒸发,用到坩埚 溶液,再直接蒸发,用到坩埚 |
| C.在第④⑤⑥步中溴元素均被氧化 |
D.在第①步中除去粗盐中的 、 、 、 、 、 、 等杂质,加入药品的顺序为 等杂质,加入药品的顺序为 溶液→ 溶液→ 溶液→ 溶液→ 溶液→过滤后加盐酸 溶液→过滤后加盐酸 |
您最近一年使用:0次
2023-08-15更新
|
134次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高二上学期11月期中化学试题
名校
7 . 水荒目前已成为世界性的问题,是制约社会进步和经济发展的瓶颈。海水淡化是获得淡水的重要途径,下列不属于海水淡化方法的是
| A.蒸馏法 | B.电渗析法 | C.萃取法 | D.离子交换法 |
您最近一年使用:0次
名校
解题方法
8 . 从海水中不仅可获得淡水,而且可按如图工艺流程提取溴和镁。
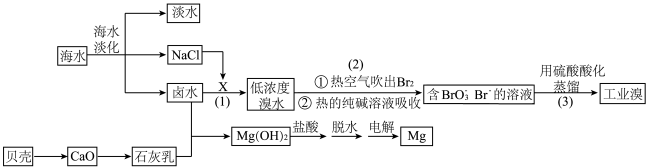
回答下列问题:
(1)海水淡化的方法有___________ 、电渗析法和反渗透法。
(2)步骤(1)中的X是一种黄绿色单质,X的电子式为___________ ,制备X的方法是电解饱和 溶液,电解时的离子方程式为
溶液,电解时的离子方程式为___________ 。
(3)检验某 溶液中是否混有
溶液中是否混有 的方法是
的方法是___________ 。
(4)溴单质与热的纯碱溶液反应有气体生成,该反应的化学方程式为___________ 。
(5)步骤(3)发生反应的离子方程式为___________ 。
(6)写出冶练金属镁的化学方程式:___________ 。

回答下列问题:
(1)海水淡化的方法有
(2)步骤(1)中的X是一种黄绿色单质,X的电子式为
 溶液,电解时的离子方程式为
溶液,电解时的离子方程式为(3)检验某
 溶液中是否混有
溶液中是否混有 的方法是
的方法是(4)溴单质与热的纯碱溶液反应有气体生成,该反应的化学方程式为
(5)步骤(3)发生反应的离子方程式为
(6)写出冶练金属镁的化学方程式:
您最近一年使用:0次
2023-07-07更新
|
97次组卷
|
2卷引用:河南省新乡市2022-2023学年高一下学期7月期末考试化学试题
名校
9 . 海洋中有丰富的食品、矿产、能源、药物和水产等资源,下图为海水综合利用的部分流程。回答下列问题:
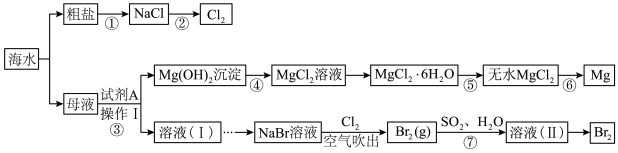
(1)粗盐中可溶性杂质离子包含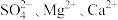 。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
。要除去这些杂质离子得到精盐水,加入试剂的顺序可为_______ (填字母)。
a.NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸
b.NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸
c.BaCl2溶液、Na2CO3溶液、NaOH溶液、盐酸
(2)步骤③加入的试剂A是_______ ,然后进行的操作Ⅰ是_______ 。
(3)步骤①~⑦中,涉及氧化还原反应的步骤有_______ 。
(4)步骤⑥的化学方程式为_______ 。
(5)步骤⑦的离子方程式为_______ 。

(1)粗盐中可溶性杂质离子包含
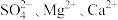 。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
。要除去这些杂质离子得到精盐水,加入试剂的顺序可为a.NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸
b.NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸
c.BaCl2溶液、Na2CO3溶液、NaOH溶液、盐酸
(2)步骤③加入的试剂A是
(3)步骤①~⑦中,涉及氧化还原反应的步骤有
(4)步骤⑥的化学方程式为
(5)步骤⑦的离子方程式为
您最近一年使用:0次
名校
10 . I.海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和制得镁、溴等重要的化工产品。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和___________ 。离子交换法净化水的过程如图所示。下列说法正确的是___________ (填序号)。
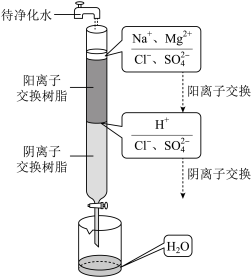
A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有 被除去
被除去
C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:
(2)工业上通过 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是___________ 。制备溴时通入热空气可以吹出溴,是利用了溴的___________ 。
Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:
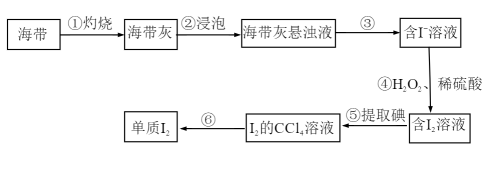
(3)实验步骤①不会用到下列仪器中的___________ (填字母)
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是___________
(5)步骤④中反应的离子方程式为___________
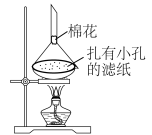
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理________ ;棉花的作用是________ 。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和

A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有
 被除去
被除去C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:

(2)工业上通过
 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:

(3)实验步骤①不会用到下列仪器中的
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是
(5)步骤④中反应的离子方程式为
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理

您最近一年使用:0次



