从海水中不仅可获得淡水,而且可按如图工艺流程提取溴和镁。
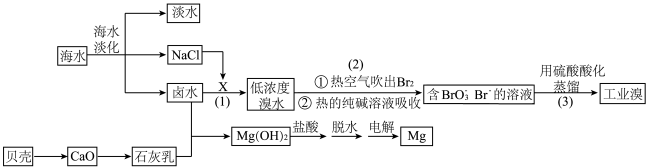
回答下列问题:
(1)海水淡化的方法有___________ 、电渗析法和反渗透法。
(2)步骤(1)中的X是一种黄绿色单质,X的电子式为___________ ,制备X的方法是电解饱和 溶液,电解时的离子方程式为
溶液,电解时的离子方程式为___________ 。
(3)检验某 溶液中是否混有
溶液中是否混有 的方法是
的方法是___________ 。
(4)溴单质与热的纯碱溶液反应有气体生成,该反应的化学方程式为___________ 。
(5)步骤(3)发生反应的离子方程式为___________ 。
(6)写出冶练金属镁的化学方程式:___________ 。

回答下列问题:
(1)海水淡化的方法有
(2)步骤(1)中的X是一种黄绿色单质,X的电子式为
 溶液,电解时的离子方程式为
溶液,电解时的离子方程式为(3)检验某
 溶液中是否混有
溶液中是否混有 的方法是
的方法是(4)溴单质与热的纯碱溶液反应有气体生成,该反应的化学方程式为
(5)步骤(3)发生反应的离子方程式为
(6)写出冶练金属镁的化学方程式:
更新时间:2023-07-07 12:00:16
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】从海水中可提取多种化工原料,下图是工业上对海水的几项综合利用的示意图。试回答下列问题: 的化学方程式:
的化学方程式:___________ ,___________ ;
(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?___________ ;
(3)电解无水 可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为
可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为___________ ;
(4)海边盐碱地(含较多 、
、 )不利于植物生长,盐碱地产生碱性的原因:
)不利于植物生长,盐碱地产生碱性的原因:___________ (用离子方程式表示);农业上用石膏降低其碱性的反应原理:___________ (用化学方程式表示);
(5)用海滩上的贝壳制 ,而不从异地山中开凿石灰石制取,主要考虑到
,而不从异地山中开凿石灰石制取,主要考虑到___________ 问题。

 的化学方程式:
的化学方程式:(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?
(3)电解无水
 可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为
可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为(4)海边盐碱地(含较多
 、
、 )不利于植物生长,盐碱地产生碱性的原因:
)不利于植物生长,盐碱地产生碱性的原因:(5)用海滩上的贝壳制
 ,而不从异地山中开凿石灰石制取,主要考虑到
,而不从异地山中开凿石灰石制取,主要考虑到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】含钠化合物在工业生产和日常生活中应用广泛,请回答下列有关问题:
(1)钠元素的碱性氧化物的化学式为___________ ,钠另一种氧化物是一种淡黄色固体,写出其用于呼吸面具供氧剂的一个化学方程式:___________ 。
(2)NaOH是一种强碱,若实验室用NaOH浓溶液配制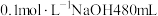 ,需量取密度为
,需量取密度为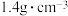 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液___________ mL,该实验所需的玻璃仪器除玻璃棒、量筒、烧杯之外,还有___________ ,若量取浓NaOH溶液时俯视,则最终配制溶液浓度___________ (填“偏大”、“偏小”或“无影响”)。当450mL所配溶液与标准状况下672mLCO2恰好反应时,发生反应的离子方程式为___________ 。
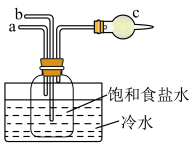
(3)如图是实验室模拟“侯氏制碱法”制取NaHCO3的部分装置。下列说正确的是___________(填序号)
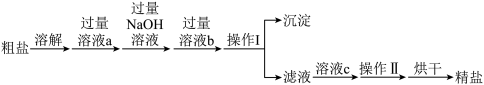
(4)粗盐常含有少量 以及泥沙等杂质,实验室中可用如下流程提纯NaCl,下列说法中正确的是___________(填序号)
以及泥沙等杂质,实验室中可用如下流程提纯NaCl,下列说法中正确的是___________(填序号)
(1)钠元素的碱性氧化物的化学式为
(2)NaOH是一种强碱,若实验室用NaOH浓溶液配制
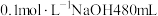 ,需量取密度为
,需量取密度为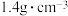 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液(3)如图是实验室模拟“侯氏制碱法”制取NaHCO3的部分装置。下列说正确的是___________(填序号)

| A.a先通入CO2,然后b通入NH3,c中放碱石灰 |
| B.b先通入NH3,然后a通入CO2,c中放碱石灰 |
| C.a先通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉 |
| D.b先通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉 |
(4)粗盐常含有少量
 以及泥沙等杂质,实验室中可用如下流程提纯NaCl,下列说法中正确的是___________(填序号)
以及泥沙等杂质,实验室中可用如下流程提纯NaCl,下列说法中正确的是___________(填序号)
| A.溶液a和NaOH可用一种试剂来代替 |
| B.溶液a和溶液b的添加顺序可以互换 |
| C.操作Ⅱ为蒸发结晶,蒸发过程中当蒸发皿中有大量晶体析出时停止加热 |
| D.粗盐提纯的整个操作过程中共有两处需要使用玻璃棒 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海水是巨大的资源宝库,人类从海水中提取某些化工原料的简单流程如下:

已知:溴单质的沸点为 ,氧化镁的熔点为
,氧化镁的熔点为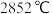 ,氯化镁的熔点为
,氯化镁的熔点为 。
。
请回答下列问题。
(1)流程中,试剂①和②适宜选用___________ 。
(2)工业上采用电解熔融氯化镁而不用电解熔融氧化镁制金属镁,其原因是___________ 。
(3)工业上利用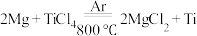 制备金属Ti,该方法属于
制备金属Ti,该方法属于___________ 。
A.热分解法 B.热还原法 C.电解法
(4)“吹出塔”中通入热空气吹出 ,利用了
,利用了
___________ 的性质。
(5)“吸收塔”中发生反应的离子方程式为___________ 。
(6)“蒸馏塔”中温度应控制在___________ 。
A.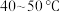 B.
B.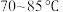 C.100℃以上
C.100℃以上

已知:溴单质的沸点为
 ,氧化镁的熔点为
,氧化镁的熔点为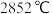 ,氯化镁的熔点为
,氯化镁的熔点为 。
。请回答下列问题。
(1)流程中,试剂①和②适宜选用
| 试剂① | 试剂② | |
| A | NaOH溶液 | 盐酸 |
| B | NaOH溶液 | 硫酸 |
| C | 石灰乳 | 盐酸 |
| D | 澄清石灰水 | 硝酸 |
(3)工业上利用
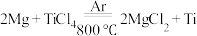 制备金属Ti,该方法属于
制备金属Ti,该方法属于A.热分解法 B.热还原法 C.电解法
(4)“吹出塔”中通入热空气吹出
 ,利用了
,利用了
(5)“吸收塔”中发生反应的离子方程式为
(6)“蒸馏塔”中温度应控制在
A.
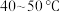 B.
B.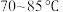 C.100℃以上
C.100℃以上
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
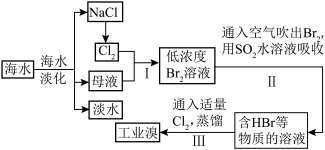
(1)从海水中可以得到食盐。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是___ 。
A.①④②⑤③B.④①②⑤③C.②⑤④①③D.②④⑤①③
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为___ 。
(3)步骤Ⅱ用SO2水溶液吸收Br2同时有H2SO4生成,吸收率可达95%,有关反应的离子方程式为___ ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是___ 。

(1)从海水中可以得到食盐。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是
A.①④②⑤③B.④①②⑤③C.②⑤④①③D.②④⑤①③
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为
(3)步骤Ⅱ用SO2水溶液吸收Br2同时有H2SO4生成,吸收率可达95%,有关反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
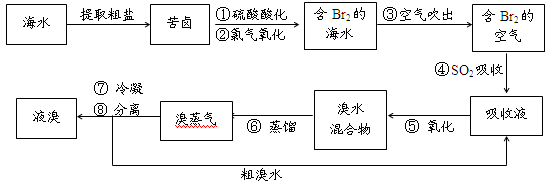
41、溴在元素周期表中位于_________ 周期,_________ 族。
42、步骤①中用硫酸酸化可提高Cl2的利用率,其原因是_____________________ 。
43、步骤④的离子方程式:_______________________________________ 。
44、步骤⑥的蒸馏过程中,溴出口温度要控制在80—90℃。温度过高或过低都不利于生产,请解释原因:__________________________________________ 。
45、步骤⑧中溴气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是_____________ ,分离时液溴从分离器的_____ (填“上口”或“下口”)排出。
46、不直接用步骤②后含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氧化”的原因是________________________________________________ 。
47、下列有关溴单质的叙述正确的是_____________

41、溴在元素周期表中位于
42、步骤①中用硫酸酸化可提高Cl2的利用率,其原因是
43、步骤④的离子方程式:
44、步骤⑥的蒸馏过程中,溴出口温度要控制在80—90℃。温度过高或过低都不利于生产,请解释原因:
45、步骤⑧中溴气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是
46、不直接用步骤②后含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氧化”的原因是
47、下列有关溴单质的叙述正确的是
| A.是易挥发的深红棕色液体 |
| B.实验室少量液溴可保存在橡皮塞的棕色瓶中,并且加少量的水液封 |
| C.可用酒精从溴水中萃取溴 |
| D.溴可以与NaI溶液反应,置换出碘单质 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海洋中有丰富的资源,从中可以制取氯溴碘的单质及其化合物
Ⅰ氯气是一种重要的化工原料,是氯碱工业的主要产品之一,它是一种常用的消毒剂。由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上利用氯气和石灰乳生产漂白粉的主要化学方程式是___________________________ ,在空气中漂白粉长期存放会变质而失效的原理是(用化学方程式说明)________ 、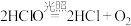 。
。
Ⅱ海水中溴元素以 形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:

请回答下列问题。
(1)将海水浓缩的方法是________ 。
(2)步骤①反应的化学方程式是________________________________ 。
(3)步骤②通入热空气吹出 ,利用了
,利用了 的
的________ (填字母)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
Ⅲ碘及其化合物在科研、生活等方面有广泛用途。如图所示为从海带中制取碘的工艺流程。
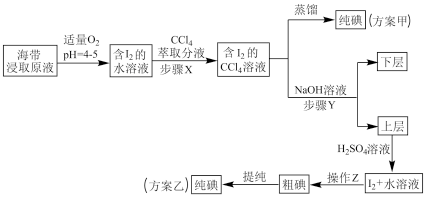
已知: 。
。
(1)步骤X中,萃取后分液漏斗内观察到的现象是__________________ 。
(2)下列有关步骤Y的说法中正确的是_______ (填字母)。
A.应控制 溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D. 溶液可以用乙醇代替
溶液可以用乙醇代替
(3)向上层清液中加入 溶液,发生反应的化学方程式为
溶液,发生反应的化学方程式为_______________________ ,由于碘单质在水中的溶解度较小,且通过富集后得到的碘单质浓度较大,操作Z的名称为___________ 。
Ⅰ氯气是一种重要的化工原料,是氯碱工业的主要产品之一,它是一种常用的消毒剂。由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上利用氯气和石灰乳生产漂白粉的主要化学方程式是
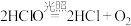 。
。Ⅱ海水中溴元素以
 形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
请回答下列问题。
(1)将海水浓缩的方法是
(2)步骤①反应的化学方程式是
(3)步骤②通入热空气吹出
 ,利用了
,利用了 的
的A.氧化性 B.还原性 C.挥发性 D.腐蚀性
Ⅲ碘及其化合物在科研、生活等方面有广泛用途。如图所示为从海带中制取碘的工艺流程。

已知:
 。
。(1)步骤X中,萃取后分液漏斗内观察到的现象是
(2)下列有关步骤Y的说法中正确的是
A.应控制
 溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
溶液的浓度和体积 B.将碘单质转化成碘离子进入水层C.主要是除去海带浸取原液中的有机杂质 D.
 溶液可以用乙醇代替
溶液可以用乙醇代替(3)向上层清液中加入
 溶液,发生反应的化学方程式为
溶液,发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】已知海水提取镁的主要步骤如下:
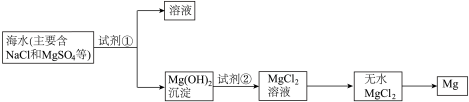
(1)关于加入试剂①作沉淀剂,有以下方法,请完成下列问题。
a._____________ ;
b.____________ ;
c.____________ 。
(2)框图中加入的试剂①应该是_______ (填物质名称),加入试剂②的溶质是_______ (填化学式)。工业上由无水 制取镁的化学方程式为
制取镁的化学方程式为___________ 。

(1)关于加入试剂①作沉淀剂,有以下方法,请完成下列问题。
| 方法 | 是否合理 | 简述理由 |
| 方法:高温加热蒸发海水后,再加入沉淀剂 | a | b |
| 你认为合理的其他方法是c |
a.
b.
c.
(2)框图中加入的试剂①应该是
 制取镁的化学方程式为
制取镁的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】从海水中提取一些重要的化工产品的工艺流程如图所示。
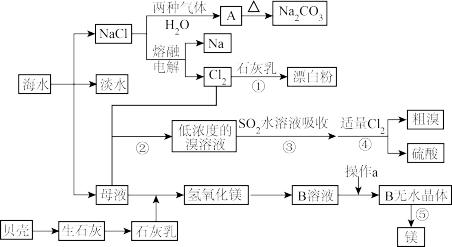
根据上述流程图回答下列问题:
(1)图中A的化学式为___ ,在制取A的过程中需向饱和NaCl溶液中先后通入两种气体,后通入气体的化学式为_______ 。
(2)反应①化学方程式为______ 。
(3)海水淡化处理的方法有____________ 。(写出2种即可)
(4)过程⑤的化学方程式为_________ 。
(5)过程③用 水溶液吸收溴单质,吸收率可达93%,生成两种强酸,写出反应的离子方程式
水溶液吸收溴单质,吸收率可达93%,生成两种强酸,写出反应的离子方程式_____ 。
(6)过程②到过程④的变化为“ ”,其目的是
”,其目的是_____ 。

根据上述流程图回答下列问题:
(1)图中A的化学式为
(2)反应①化学方程式为
(3)海水淡化处理的方法有
(4)过程⑤的化学方程式为
(5)过程③用
 水溶液吸收溴单质,吸收率可达93%,生成两种强酸,写出反应的离子方程式
水溶液吸收溴单质,吸收率可达93%,生成两种强酸,写出反应的离子方程式(6)过程②到过程④的变化为“
 ”,其目的是
”,其目的是
您最近一年使用:0次
【推荐3】海水中有丰富的自然资源,下图是海水联合利用的工业体系简图。
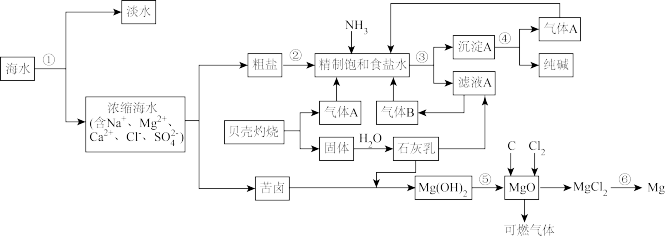
回答下列问题:
Ⅰ.海水淡化
(1)人类可以从海水中获得淡水,以解决淡水资源危机。下列不属于海水淡化方法的是___________(填正确答案标号)。
Ⅱ.粗盐提纯
(2)粗盐中可溶性的杂质离子有 、
、 、
、 。要除去这些杂质离子得到精制盐水,需要依次加入NaOH溶液、
。要除去这些杂质离子得到精制盐水,需要依次加入NaOH溶液、 浴液、
浴液、 溶液、盐酸,其中
溶液、盐酸,其中 溶液的作用是
溶液的作用是___________ ,加入盐酸前需要完成的实验操作的名称是___________ 。
Ⅲ.纯碱制取
(3)上述流程中气体A的化学式为___________ ,向精制饱和食盐水中先通入的气体是___________ ,写出生成沉淀A的化学方程式___________ ,在制纯碱的过程中,循环使用的物质是___________ 。
Ⅳ.海水提镁
(4)氧化镁、碳、氯气在高温下反应生成氯化镁的化学方程式为___________ 。工业上从母液中获取 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是___________ 。

回答下列问题:
Ⅰ.海水淡化
(1)人类可以从海水中获得淡水,以解决淡水资源危机。下列不属于海水淡化方法的是___________(填正确答案标号)。
| A.蒸馏法 | B.离子交换法 | C.沉淀法 | D.电渗析法 |
Ⅱ.粗盐提纯
(2)粗盐中可溶性的杂质离子有
 、
、 、
、 。要除去这些杂质离子得到精制盐水,需要依次加入NaOH溶液、
。要除去这些杂质离子得到精制盐水,需要依次加入NaOH溶液、 浴液、
浴液、 溶液、盐酸,其中
溶液、盐酸,其中 溶液的作用是
溶液的作用是Ⅲ.纯碱制取
(3)上述流程中气体A的化学式为
Ⅳ.海水提镁
(4)氧化镁、碳、氯气在高温下反应生成氯化镁的化学方程式为
 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是
您最近一年使用:0次



