名校
1 . 地球上的大部分水是以海水形式存在的,海水淡化可以缓解淡水资源不足。下列有关海水淡化的方法在原理上可行的是
①加明矾使海水中的盐分沉淀而淡化 ②蒸馏海水,将水蒸气冷凝
③将海水暴晒,滤掉析出的盐 ④将海水加压,使水分子通过半透膜以滤去盐分
①加明矾使海水中的盐分沉淀而淡化 ②蒸馏海水,将水蒸气冷凝
③将海水暴晒,滤掉析出的盐 ④将海水加压,使水分子通过半透膜以滤去盐分
| A.①② | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
2 . 海洋是巨大的化学资源宝库,含有80多种元素。下图为利用海水制备部分物质的过程(已知:二氧化硫具有较强的还原性)。下列说法正确的是

| A.制取NaHCO3的反应是利用物质之间溶解度的差异实现的 |
| B.用澄清的石灰水可鉴别NaHCO3溶液和Na2CO3溶液 |
| C.在第③、④、⑤反应中,溴元素经历了被还原、被氧化、被还原的过程 |
| D.工业可利用氯碱工业原理制备金属钠 |
您最近一年使用:0次
3 . 下列有关物质的工业制备方法不合理的是
| A.用蒸发结晶法提取海水中的食盐 | B.氯气与澄清石灰水制取漂白粉 |
| C.用“吹出法”从海水中提取溴 | D.催化裂化将重油转化为汽油等物质 |
您最近一年使用:0次
名校
4 . 我国沿海城市采用反渗透法将海水淡化,得到淡水供市民使用,剩余母液继续加工获得其他产品。某实验小组同学模拟工业生产流程,进行如图实验。

回答下列问题:
(1)海水淡化的方法还有___________ (写一种)。
(2)制取 第一次通入
第一次通入 时发生反应的离子方程式为
时发生反应的离子方程式为___________ 。
(3)步骤①包括加热蒸发浓缩、___________ 、过滤。
(4)若要验证所得无水 中不含
中不含 ,最简单的方法是
,最简单的方法是___________ 。
(5)通电时无水 在熔融状态下反应的化学方程式为
在熔融状态下反应的化学方程式为___________ 。
(6)写出钛铁矿在高温下经氧化得到四氯化铁的化学方程式___________ 。
(7)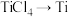 需要在氩气中进行的原因是
需要在氩气中进行的原因是___________ 。

回答下列问题:
(1)海水淡化的方法还有
(2)制取
 第一次通入
第一次通入 时发生反应的离子方程式为
时发生反应的离子方程式为(3)步骤①包括加热蒸发浓缩、
(4)若要验证所得无水
 中不含
中不含 ,最简单的方法是
,最简单的方法是(5)通电时无水
 在熔融状态下反应的化学方程式为
在熔融状态下反应的化学方程式为(6)写出钛铁矿在高温下经氧化得到四氯化铁的化学方程式
(7)
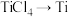 需要在氩气中进行的原因是
需要在氩气中进行的原因是
您最近一年使用:0次
5 . 从海水中提取金属镁和精盐的工艺流程如图,已知粗盐中含有泥沙、NaCl、 、
、 、
、 。下列说法正确的是
。下列说法正确的是

 、
、 、
、 。下列说法正确的是
。下列说法正确的是
A.除杂试剂及添加顺序可能为 、 、 |
| B.沉镁时所加试剂的俗称为石灰石 |
C.固体 可用作干燥剂 可用作干燥剂 |
| D.Mg在空气中燃烧的产物只有MgO |
您最近一年使用:0次
解题方法
6 . 浩瀚的海洋中蕴藏着丰富的资源。

(1)粗盐精制:过程1除去粗盐中的Ca2+、Mg2+、 杂质时,粗盐溶解后加入沉淀剂:
杂质时,粗盐溶解后加入沉淀剂:
a.过量的Na2CO3溶液 b.过量的BaCl2溶液
c.过量的NaOH溶液 d.过滤除去沉淀,再加入适量的盐酸
①加入沉淀剂的顺序正确的是___________ (填序号)。
A.abc B.bac C.cba
②加入适量盐酸,反应的离子方程式有___________ 和___________ 。
(2)海水提镁:
①过程2中在工业上常加入的试剂是___________ 。
②由Mg(OH)2固体获得MgCl2溶液的离子方程式是___________ 。

(1)粗盐精制:过程1除去粗盐中的Ca2+、Mg2+、
 杂质时,粗盐溶解后加入沉淀剂:
杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液 b.过量的BaCl2溶液
c.过量的NaOH溶液 d.过滤除去沉淀,再加入适量的盐酸
①加入沉淀剂的顺序正确的是
A.abc B.bac C.cba
②加入适量盐酸,反应的离子方程式有
(2)海水提镁:
①过程2中在工业上常加入的试剂是
②由Mg(OH)2固体获得MgCl2溶液的离子方程式是
您最近一年使用:0次
解题方法
7 . 海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是
| A.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.海底多金属结核矿含有铁、锰、钴等多种金属元素 |
| D.无论是海水波浪发电还是潮汐发电都是将化学能转化为电能 |
您最近一年使用:0次
解题方法
8 . 海洋资源的利用具有广阔前景。回答下列问题:
(1)海带灰中富含以 形式存在的碘元素。从海带中提取
形式存在的碘元素。从海带中提取 的过程如图所示:
的过程如图所示:

①灼烧海带时不需用到下列仪器中的_______ (填字母)。
a.漏斗 b.酒精灯 c.坩埚 d.泥三角
②向滤液中加入稀硫酸和 溶液进行反应,写出该反应的离子方程式
溶液进行反应,写出该反应的离子方程式_______ 。
(2)如图是从海水中提取镁的简单流程。

①操作A的名称是_______ 。
②由无水 制取Mg的化学方程式为
制取Mg的化学方程式为_______ 。
(3)从海水中提取溴的方法为吹出法,主要流程如下:

①吸收塔中反应的化学方程式为_______ 。
②蒸馏塔中控制温度不超过100℃,原因是_______ 。
③经该方法处理后,1 海水最终得到38.4g
海水最终得到38.4g  ,若总提取率为60%,则原海水中溴的浓度是
,若总提取率为60%,则原海水中溴的浓度是_______ mg/L。
(4)聚四氟乙烯气态膜法提取溴的基本原理如图所示:

①经处理后的含 海水透过膜孔与NaOH吸收液发生反应,该反应的离子方程式为
海水透过膜孔与NaOH吸收液发生反应,该反应的离子方程式为_______ ,得到富集液后再加酸、精馏可得 。
。
②聚四氟乙烯气态膜法与吹出法相比,优点是_______ (写出一条)。
(1)海带灰中富含以
 形式存在的碘元素。从海带中提取
形式存在的碘元素。从海带中提取 的过程如图所示:
的过程如图所示:
①灼烧海带时不需用到下列仪器中的
a.漏斗 b.酒精灯 c.坩埚 d.泥三角
②向滤液中加入稀硫酸和
 溶液进行反应,写出该反应的离子方程式
溶液进行反应,写出该反应的离子方程式(2)如图是从海水中提取镁的简单流程。

①操作A的名称是
②由无水
 制取Mg的化学方程式为
制取Mg的化学方程式为(3)从海水中提取溴的方法为吹出法,主要流程如下:

①吸收塔中反应的化学方程式为
②蒸馏塔中控制温度不超过100℃,原因是
③经该方法处理后,1
 海水最终得到38.4g
海水最终得到38.4g  ,若总提取率为60%,则原海水中溴的浓度是
,若总提取率为60%,则原海水中溴的浓度是(4)聚四氟乙烯气态膜法提取溴的基本原理如图所示:

①经处理后的含
 海水透过膜孔与NaOH吸收液发生反应,该反应的离子方程式为
海水透过膜孔与NaOH吸收液发生反应,该反应的离子方程式为 。
。②聚四氟乙烯气态膜法与吹出法相比,优点是
您最近一年使用:0次
9 . 海水是巨大的资源宝库,利用海水为原料可获得许多化工产品。回答下列问题:
(1)从海水提取的粗盐中含有 等杂质离子,精制时一般步骤如下:
等杂质离子,精制时一般步骤如下:
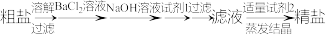
加入的试剂1、2分别是___________ 、___________ 。
(2)海水中溴元素主要以 形式存在,工业上从海水中提取溴的流程如下:
形式存在,工业上从海水中提取溴的流程如下:

①写出“氧化”过程中发生反应的离子方程式___________ 。
②将吹出后的含 空气按一定速率通入吸收塔,用
空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式
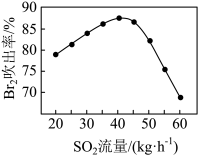
和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式___________ ;吹出时 的吹出率与吸收塔中
的吹出率与吸收塔中 流量的关系如图所示。
流量的关系如图所示。 流量过大,
流量过大, 吹出率反而下降的原因是
吹出率反而下降的原因是___________ 。
(3)工业上也可用 溶液代替二氧化硫水溶液吸收
溶液代替二氧化硫水溶液吸收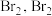 最终转化为
最终转化为 和
和 则发生反应的化学方程式为
则发生反应的化学方程式为___________ ;当有 个电子发生转移时理论上吸收
个电子发生转移时理论上吸收 的质量为
的质量为___________ g。
(4)第一次“氧化”后已获得游离态的溴,“吹出”又将之转变成化合态的溴,其目的是___________ 。
(1)从海水提取的粗盐中含有
 等杂质离子,精制时一般步骤如下:
等杂质离子,精制时一般步骤如下: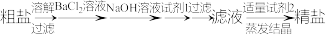
加入的试剂1、2分别是
(2)海水中溴元素主要以
 形式存在,工业上从海水中提取溴的流程如下:
形式存在,工业上从海水中提取溴的流程如下:
①写出“氧化”过程中发生反应的离子方程式
②将吹出后的含
 空气按一定速率通入吸收塔,用
空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式
和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式 的吹出率与吸收塔中
的吹出率与吸收塔中 流量的关系如图所示。
流量的关系如图所示。 流量过大,
流量过大, 吹出率反而下降的原因是
吹出率反而下降的原因是
(3)工业上也可用
 溶液代替二氧化硫水溶液吸收
溶液代替二氧化硫水溶液吸收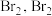 最终转化为
最终转化为 和
和 则发生反应的化学方程式为
则发生反应的化学方程式为 个电子发生转移时理论上吸收
个电子发生转移时理论上吸收 的质量为
的质量为(4)第一次“氧化”后已获得游离态的溴,“吹出”又将之转变成化合态的溴,其目的是
您最近一年使用:0次
解题方法
10 . 海洋资源的利用具有非常广阔的前景。

I.海水制盐。
(1)粗盐中可溶性杂质离子包含 、
、 、
、 。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
。要除去这些杂质离子得到精盐水,加入试剂的顺序可为___________ (填字母)。
a. 溶液、
溶液、 溶液、
溶液、 溶液、盐酸
溶液、盐酸
b. 溶液、
溶液、 溶液、
溶液、 溶液、盐酸
溶液、盐酸
c. 溶液、
溶液、 溶液、
溶液、 溶液、盐酸
溶液、盐酸
(2)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式:___________ 。
Ⅱ.海水提溴。
(3)工业上常用“吹出法”提取溴,请写出用 吸收
吸收 的化学反应方程式:
的化学反应方程式:___________ 。
(4)含 的海水经“空气吹出、
的海水经“空气吹出、 吸收、通入氯气”后再蒸馏的目的是
吸收、通入氯气”后再蒸馏的目的是___________ 。
Ⅲ.从海带中提取碘的实验过程如图所示。

(5)步骤①中灼烧海带时,应将海带放入___________ (填仪器名称)中灼烧。
(6)请写出步骤④反应的离子方程式:___________ 。
Ⅳ.海水淡化。
(7)列举一种海水淡化的方法:___________ 。

I.海水制盐。
(1)粗盐中可溶性杂质离子包含
 、
、 、
、 。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
。要除去这些杂质离子得到精盐水,加入试剂的顺序可为a.
 溶液、
溶液、 溶液、
溶液、 溶液、盐酸
溶液、盐酸b.
 溶液、
溶液、 溶液、
溶液、 溶液、盐酸
溶液、盐酸c.
 溶液、
溶液、 溶液、
溶液、 溶液、盐酸
溶液、盐酸(2)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式:
Ⅱ.海水提溴。
(3)工业上常用“吹出法”提取溴,请写出用
 吸收
吸收 的化学反应方程式:
的化学反应方程式:(4)含
 的海水经“空气吹出、
的海水经“空气吹出、 吸收、通入氯气”后再蒸馏的目的是
吸收、通入氯气”后再蒸馏的目的是Ⅲ.从海带中提取碘的实验过程如图所示。

(5)步骤①中灼烧海带时,应将海带放入
(6)请写出步骤④反应的离子方程式:
Ⅳ.海水淡化。
(7)列举一种海水淡化的方法:
您最近一年使用:0次



