海水是巨大的资源宝库,利用海水为原料可获得许多化工产品。回答下列问题:
(1)从海水提取的粗盐中含有 等杂质离子,精制时一般步骤如下:
等杂质离子,精制时一般步骤如下:
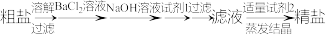
加入的试剂1、2分别是___________ 、___________ 。
(2)海水中溴元素主要以 形式存在,工业上从海水中提取溴的流程如下:
形式存在,工业上从海水中提取溴的流程如下:

①写出“氧化”过程中发生反应的离子方程式___________ 。
②将吹出后的含 空气按一定速率通入吸收塔,用
空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式
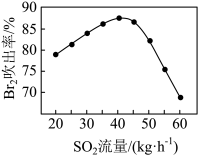
和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式___________ ;吹出时 的吹出率与吸收塔中
的吹出率与吸收塔中 流量的关系如图所示。
流量的关系如图所示。 流量过大,
流量过大, 吹出率反而下降的原因是
吹出率反而下降的原因是___________ 。
(3)工业上也可用 溶液代替二氧化硫水溶液吸收
溶液代替二氧化硫水溶液吸收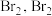 最终转化为
最终转化为 和
和 则发生反应的化学方程式为
则发生反应的化学方程式为___________ ;当有 个电子发生转移时理论上吸收
个电子发生转移时理论上吸收 的质量为
的质量为___________ g。
(4)第一次“氧化”后已获得游离态的溴,“吹出”又将之转变成化合态的溴,其目的是___________ 。
(1)从海水提取的粗盐中含有
 等杂质离子,精制时一般步骤如下:
等杂质离子,精制时一般步骤如下: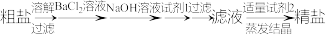
加入的试剂1、2分别是
(2)海水中溴元素主要以
 形式存在,工业上从海水中提取溴的流程如下:
形式存在,工业上从海水中提取溴的流程如下:
①写出“氧化”过程中发生反应的离子方程式
②将吹出后的含
 空气按一定速率通入吸收塔,用
空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式
和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式 的吹出率与吸收塔中
的吹出率与吸收塔中 流量的关系如图所示。
流量的关系如图所示。 流量过大,
流量过大, 吹出率反而下降的原因是
吹出率反而下降的原因是
(3)工业上也可用
 溶液代替二氧化硫水溶液吸收
溶液代替二氧化硫水溶液吸收 最终转化为
最终转化为 和
和 则发生反应的化学方程式为
则发生反应的化学方程式为 个电子发生转移时理论上吸收
个电子发生转移时理论上吸收 的质量为
的质量为(4)第一次“氧化”后已获得游离态的溴,“吹出”又将之转变成化合态的溴,其目的是
更新时间:2023-07-13 07:10:47
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】镁及其合金是一种用途很广的金属材料,工业上从海水(含有NaCl和 等)中提取镁的生产流程如图所示。
等)中提取镁的生产流程如图所示。

回答下列问题:
(1)该生产中,利用到贝壳中的主要成分是_______ 。
(2)每升海水中含 的质量约为1.2g,则海水中
的质量约为1.2g,则海水中 的物质的量浓度是
的物质的量浓度是_______ mol/L。
(3)实验室模拟“过滤”操作时,用到的玻璃仪器有_______ 。
(4)“中和”操作中发生的离子方程式是_______ 。
(5)“电解”操作中发生的化学方程式是_______ 。
(6)该流程中循环利用的物质是_______ 。
 等)中提取镁的生产流程如图所示。
等)中提取镁的生产流程如图所示。
回答下列问题:
(1)该生产中,利用到贝壳中的主要成分是
(2)每升海水中含
 的质量约为1.2g,则海水中
的质量约为1.2g,则海水中 的物质的量浓度是
的物质的量浓度是(3)实验室模拟“过滤”操作时,用到的玻璃仪器有
(4)“中和”操作中发生的离子方程式是
(5)“电解”操作中发生的化学方程式是
(6)该流程中循环利用的物质是
您最近一年使用:0次
【推荐2】海水资源的利用具有非常广阔的前景。下面是海水综合利用联合工业体系的简图:
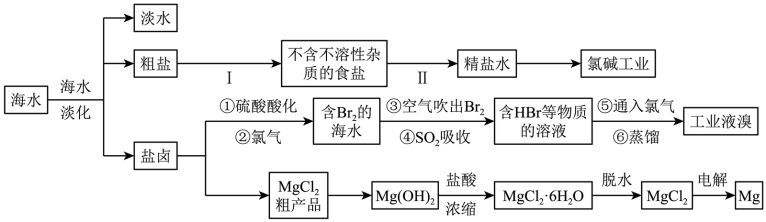
回答下列问题:
I.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法主要有__ 、__ 等。
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是___ 。
(3)粗盐中可溶性的杂质离子主要有SO 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是___ 。
Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为___ ;从理论上考虑下列也能吸收Br2的是___ 。
A.NaCl B.FeCl2 C.Na2SO3 D.H2O E.K2S
(5)经过步骤①②已获得Br2,不直接用含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、通入氯气”后再蒸馏,其目的是___ 。
Ⅳ.海水提镁
(6)该工业生产过程中,为了使MgCl2转化为Mg(OH)2,应加入的试剂为___ 。

回答下列问题:
I.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法主要有
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是
(3)粗盐中可溶性的杂质离子主要有SO
 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸,其中Na2CO3溶液的作用是Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为
A.NaCl B.FeCl2 C.Na2SO3 D.H2O E.K2S
(5)经过步骤①②已获得Br2,不直接用含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、通入氯气”后再蒸馏,其目的是
Ⅳ.海水提镁
(6)该工业生产过程中,为了使MgCl2转化为Mg(OH)2,应加入的试剂为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】I.海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和溴的过程r如下:
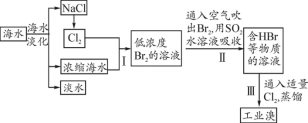
(1)步骤Ⅰ获得Br2的化学反应的离子方程式为___________ 。
(2)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为___________ 。在该反应中,氧化剂是___________ (填化学式);若反应中生成2 mol HBr,则消耗___________ mol SO2。
(3)根据上述反应可判断出SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是___________ 。
II.A是一种重要的化工原料,部分性质及转化关系如下图:

请回答。
(4)D中官能团的名称是___________ 。
(5)A→B的反应类型是___________。
(6)写出A→C反应的化学方程式:___________ 。

(1)步骤Ⅰ获得Br2的化学反应的离子方程式为
(2)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为
(3)根据上述反应可判断出SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
II.A是一种重要的化工原料,部分性质及转化关系如下图:

请回答。
(4)D中官能团的名称是
(5)A→B的反应类型是___________。
| A.取代反应 | B.加成反应 | C.氧化反应 | D.还原反应 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有 、
、 、
、 以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是___________ 。
(2)第②步操作的目的是除去粗盐中的___________ (填化学式,下同),第⑥步操作的目的是除去滤液中___________ 和___________ 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、 、
、 、
、___________ 和___________ 。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是___________ 。
(5)过量 溶液和过量
溶液和过量 溶液滴加顺序
溶液滴加顺序___________ (填可以或不可以)调换,理由是___________ 。
(6)写出第③步一定能发生的离子反应方程___________ 。
 、
、 、
、 以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是
(2)第②步操作的目的是除去粗盐中的
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、
 、
、 、
、(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是
(5)过量
 溶液和过量
溶液和过量 溶液滴加顺序
溶液滴加顺序(6)写出第③步一定能发生的离子反应方程
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】Ⅰ.食盐是日常生活的必需品,也是重要的化工原料,粗盐中常含有少量的 、
、 、
、 等杂质离子。实验室提纯NaCl的流程如下:
等杂质离子。实验室提纯NaCl的流程如下:
(1)下列关于食盐的说法错误的是___________。
(2)在粗盐提纯的实验中,无需进行的操作有___________。
Ⅱ.实验室里需要纯净的氯化钠溶液,原料为混有硫酸钠、碳酸氢铵杂质的氯化钠。某学生设计了如下方案:

(3)操作①应在___________ (填容器名称)中进行反应。
(4)操作②是否可改为加硝酸钡溶液?为什么?___________ 。
(5)进行操作②后,如何判断 已除尽,方法是
已除尽,方法是___________ 。
(6)下列物质的分类正确的是___________。
Ⅲ.获得的纯净氯化钠用以进行后续实验:以石墨为电极电解饱和食盐水的装置如图所示,饱和食盐水中滴有酚酞试液。

(7)下列判断正确的是___________。
Ⅲ.某课外活动小组进行胶体的制备实验,并检验其相关的性质。
(8)资料表明:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL___________ 饱和溶液,加热片刻,即可制备 胶体。
胶体。
(9)小组成员为了证实制得的液体确实是胶体,采用的方法是___________ 。
 、
、 、
、 等杂质离子。实验室提纯NaCl的流程如下:
等杂质离子。实验室提纯NaCl的流程如下:(1)下列关于食盐的说法错误的是___________。
| A.现在生产的食盐大部分用于食用 | B.生理盐水是0.9%的食盐溶液 |
| C.海水晒盐,又称为盐田法 | D.目前我国食盐年产量名列世界第一 |
(2)在粗盐提纯的实验中,无需进行的操作有___________。
| A.溶解 | B.过滤 | C.蒸馏 | D.蒸发 |
Ⅱ.实验室里需要纯净的氯化钠溶液,原料为混有硫酸钠、碳酸氢铵杂质的氯化钠。某学生设计了如下方案:

(3)操作①应在
(4)操作②是否可改为加硝酸钡溶液?为什么?
(5)进行操作②后,如何判断
 已除尽,方法是
已除尽,方法是(6)下列物质的分类正确的是___________。
| 选项 | 碱 | 酸 | 盐 | 酸性氧化物 |
| A | 纯碱 | 盐酸 | 烧碱 | 二氧化硫 |
| B | 烧碱 | 硫酸 | 食盐 | 氯化氢 |
| C | 苛性钠 | 醋酸 | 石灰石 | 水 |
| D | 苛性钠 | 碳酸 | 苏打 | 三氧化硫 |
| A.A | B.B | C.C | D.D |
Ⅲ.获得的纯净氯化钠用以进行后续实验:以石墨为电极电解饱和食盐水的装置如图所示,饱和食盐水中滴有酚酞试液。

(7)下列判断正确的是___________。
| A.A极为正极,B为负极 |
| B.通电一段时间后,A电极附近溶液先变红 |
C.A电极上有 产生,B电极上有 产生,B电极上有 产生 产生 |
| D.通电一段时间后,B电极附近溶液pH变大 |
Ⅲ.某课外活动小组进行胶体的制备实验,并检验其相关的性质。
(8)资料表明:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL
 胶体。
胶体。(9)小组成员为了证实制得的液体确实是胶体,采用的方法是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】阳离子交换膜法电解饱和食盐水、具有综合能耗低、环境污染小等优点。生产流程如图所示:

(1)粗盐提纯后还含有Ca2+、Mg2+及SO 等杂质离子,电解之前需要精制食盐水。除去粗盐中杂质离子的试剂的加入顺序是
等杂质离子,电解之前需要精制食盐水。除去粗盐中杂质离子的试剂的加入顺序是___________ (填写字母序号),过滤,再加入适量盐酸。
a.NaOH b. BaCl2 c.Na2 CO3
(2)电解饱和食盐水的化学方程式为_____________ 。电解一段时间后 , 若向浓烧碱溶液中通入CO2气体,使所得溶液c(HCO ):c(CO
):c(CO )=2∶1,则此时溶液中的c(H+)=
)=2∶1,则此时溶液中的c(H+)=_______ mol·L-1(室温下,H2CO3 Ka1=4×10-7, Ka2=5×10-11)
(3)电解结束后,能够脱去阳极液中游离氯的试剂或方法是________ (填字母序号)。
a.Na2SO3 b.NaNO3 c.热空气吹出 d.降低阳极区液面上方的气压
(4)食盐水中的I-若进入电解槽,可被电解产生的Cl2氧化为ICl,并进一步转化为IO 。IO
。IO 可继续被氧化为高碘酸根(IO
可继续被氧化为高碘酸根(IO ),与Na+结合生成溶解度较小的NaIO4沉积于阳离子交换膜上,影响膜的寿命。
),与Na+结合生成溶解度较小的NaIO4沉积于阳离子交换膜上,影响膜的寿命。
①ICl为有毒的黑色晶体,可用氢氧化钠溶液吸收,请写出相应的离子反应方程式:________ 。
②请写出NaIO3被 Cl2氧化为NaIO4的化学反应方程式为____________ 。
(5)研究表明食盐水中I-含量≤0.2 mg•L-1时对离子交换膜影响可忽略。现将1m3含I-浓度为1.47 mg•L-1 的食盐水进行处理,为达到使用标准,理论上至少 需要0.05 mol•L-1 NaClO溶液_________ L。(已知NaClO的反应产物为NaCl,溶液体积变化忽略不计)

(1)粗盐提纯后还含有Ca2+、Mg2+及SO
 等杂质离子,电解之前需要精制食盐水。除去粗盐中杂质离子的试剂的加入顺序是
等杂质离子,电解之前需要精制食盐水。除去粗盐中杂质离子的试剂的加入顺序是a.NaOH b. BaCl2 c.Na2 CO3
(2)电解饱和食盐水的化学方程式为
 ):c(CO
):c(CO )=2∶1,则此时溶液中的c(H+)=
)=2∶1,则此时溶液中的c(H+)=(3)电解结束后,能够脱去阳极液中游离氯的试剂或方法是
a.Na2SO3 b.NaNO3 c.热空气吹出 d.降低阳极区液面上方的气压
(4)食盐水中的I-若进入电解槽,可被电解产生的Cl2氧化为ICl,并进一步转化为IO
 。IO
。IO 可继续被氧化为高碘酸根(IO
可继续被氧化为高碘酸根(IO ),与Na+结合生成溶解度较小的NaIO4沉积于阳离子交换膜上,影响膜的寿命。
),与Na+结合生成溶解度较小的NaIO4沉积于阳离子交换膜上,影响膜的寿命。①ICl为有毒的黑色晶体,可用氢氧化钠溶液吸收,请写出相应的离子反应方程式:
②请写出NaIO3被 Cl2氧化为NaIO4的化学反应方程式为
(5)研究表明食盐水中I-含量≤0.2 mg•L-1时对离子交换膜影响可忽略。现将1m3含I-浓度为1.47 mg•L-1 的食盐水进行处理,为达到使用标准,理论上
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】海洋是巨大的化学资源宝库,如图是从海水中提取溴的流程图(部分)。

(1)过程1发生反应的离子方程式是____ 。该反应可证明氧化性:Cl2____ Br2(填“>”、“<”或者“=”),从原子结构角度解释原因____ 。
(2)写出过程2中发生的主要反应的化学方程式:____ 。
(3)上述过程2中将Br2转化成Br-的目的是____ 。
(4)若过程2用Na2CO3溶液吸收溴,补全方程式:____ 。
3Br2+ Na2CO3+ H2O= NaBr+ NaBrO3+ NaHCO3
反应中消耗3molBr2转移电子的物质的量为____ 。

(1)过程1发生反应的离子方程式是
(2)写出过程2中发生的主要反应的化学方程式:
(3)上述过程2中将Br2转化成Br-的目的是
(4)若过程2用Na2CO3溶液吸收溴,补全方程式:
3Br2+ Na2CO3+ H2O= NaBr+ NaBrO3+ NaHCO3
反应中消耗3molBr2转移电子的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】海水是巨大的资源宝库,以下是人类从海水中提取某些重要化工原料的简单流程示意图。

请回答下列问题:
(1)海洋资源的综合利用中,由海水淡化获取淡水资源具有巨大的开发潜力,海水淡化的主要方法有反渗透法、________ 、________ 。
(2)“吹出”时,常采用热空气吹出溴,利用了________ (填溴的一种物理性质)。
(3)苦卤“酸化”后,通入 发生反应的离子方程式是
发生反应的离子方程式是________ ,用 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为________ 。
(4)工业上也可用 溶液代替二氧化硫水溶液吸收
溶液代替二氧化硫水溶液吸收 ,会生成无色气体,反应后的溶液中含有
,会生成无色气体,反应后的溶液中含有 ,写出发生反应的化学方程式
,写出发生反应的化学方程式________ ,当有2mol电子发生转移时,理论上参加反应的 的质量为
的质量为________ g。
(5)从海水中提取的溴约占世界溴年产量的 ,从海水中提取溴依据上述图示的主要步骤可表示为________(填标号)。
,从海水中提取溴依据上述图示的主要步骤可表示为________(填标号)。

请回答下列问题:
(1)海洋资源的综合利用中,由海水淡化获取淡水资源具有巨大的开发潜力,海水淡化的主要方法有反渗透法、
(2)“吹出”时,常采用热空气吹出溴,利用了
(3)苦卤“酸化”后,通入
 发生反应的离子方程式是
发生反应的离子方程式是 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为(4)工业上也可用
 溶液代替二氧化硫水溶液吸收
溶液代替二氧化硫水溶液吸收 ,会生成无色气体,反应后的溶液中含有
,会生成无色气体,反应后的溶液中含有 ,写出发生反应的化学方程式
,写出发生反应的化学方程式 的质量为
的质量为(5)从海水中提取的溴约占世界溴年产量的
 ,从海水中提取溴依据上述图示的主要步骤可表示为________(填标号)。
,从海水中提取溴依据上述图示的主要步骤可表示为________(填标号)。| A.氧化→吸收→吹出→氧化 |
| B.氧化→吸收→氧化→吹出→蒸馏 |
| C.吹出→氧化→吸收→氧化 |
| D.氧化→吹出→吸收→氧化→蒸馏 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海洋中有丰富的矿产、能源、水产……等资源,部分化学资源获取途径如下:
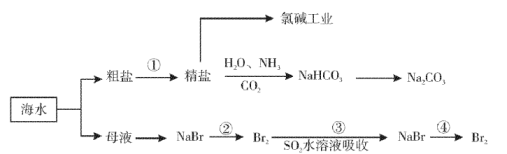
请回答下列有关问题:
(1)下列有关实验室模拟步骤①的说法正确的是___________ 。
a.溶解粗盐时,尽量使溶液稀些,以保证食盐完全溶解
b.滤去不溶性杂质后,将滤液移到坩埚内加热浓缩
c.当蒸发到剩有少量液体时停止加热,利用余热蒸干
d.制得的晶体转移到新过滤器中,需用大量水进行洗涤
(2)“氯碱工业“通过电解饱和食盐水可制得NaOH溶液、 和另一种无色无味的气体,该气体的化学式为
和另一种无色无味的气体,该气体的化学式为___________ 。
(3)下列有关说法正确的是___________ (填字母序号)。
a.在第②、③、④步骤中,溴元素均被氧化
b.用澄清的石灰水可鉴别 溶液和
溶液和 溶液
溶液
c.除去粗盐中 、
、 、
、 加入试剂的先后顺序为NaOH、
加入试剂的先后顺序为NaOH、 、
、
d.海水中还含有碘元素,将海水中的碘升华可直接制备单质碘
(4)某活动小组模拟上述工业原理制备 。实验装置如图所示(夹持、固定用的仪器未画出)。
。实验装置如图所示(夹持、固定用的仪器未画出)。
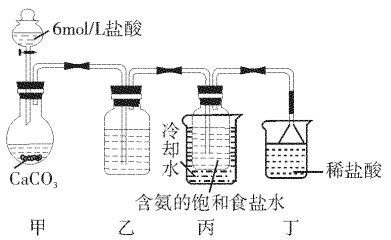
①乙装置盛装的试剂是___________ ;丁装置的作用为___________ 。
②丙中发生反应的化学方程式为___________ 。
③实验时分离出 晶体的操作为
晶体的操作为___________ (填操作名称),该操作所需要的玻璃仪器有___________ 。

请回答下列有关问题:
(1)下列有关实验室模拟步骤①的说法正确的是
a.溶解粗盐时,尽量使溶液稀些,以保证食盐完全溶解
b.滤去不溶性杂质后,将滤液移到坩埚内加热浓缩
c.当蒸发到剩有少量液体时停止加热,利用余热蒸干
d.制得的晶体转移到新过滤器中,需用大量水进行洗涤
(2)“氯碱工业“通过电解饱和食盐水可制得NaOH溶液、
 和另一种无色无味的气体,该气体的化学式为
和另一种无色无味的气体,该气体的化学式为(3)下列有关说法正确的是
a.在第②、③、④步骤中,溴元素均被氧化
b.用澄清的石灰水可鉴别
 溶液和
溶液和 溶液
溶液c.除去粗盐中
 、
、 、
、 加入试剂的先后顺序为NaOH、
加入试剂的先后顺序为NaOH、 、
、
d.海水中还含有碘元素,将海水中的碘升华可直接制备单质碘
(4)某活动小组模拟上述工业原理制备
 。实验装置如图所示(夹持、固定用的仪器未画出)。
。实验装置如图所示(夹持、固定用的仪器未画出)。
①乙装置盛装的试剂是
②丙中发生反应的化学方程式为
③实验时分离出
 晶体的操作为
晶体的操作为
您最近一年使用:0次



