名校
解题方法
1 . 食盐是日常生活的必需品,也是重要的化工原料。粗盐常含有少量 、
、 、
、 等杂质离子。实验室提纯NaCl的流程如下:
等杂质离子。实验室提纯NaCl的流程如下:

下列说法错误 的是
 、
、 、
、 等杂质离子。实验室提纯NaCl的流程如下:
等杂质离子。实验室提纯NaCl的流程如下:
下列说法
| A.试剂a为BaCl2,试剂b为Na2CO3 | B.流程图中,操作x为过滤 |
C.m g粗盐提纯后得到n g NaCl固体,则 | D.国家规定的加碘食盐中含KIO3 |
您最近半年使用:0次
名校
2 . 海带、紫菜等藻类植物富含以碘化物形式存在的碘元素,以保护自身在退潮时不受空气中少量臭氧(O3)的影响。下列流程可以从海带中提取碘单质:

(1)灼烧的目的是___________ ;操作③名称是___________ ;
(2)④中发生反应的离子方程式为___________ ;除了H2O2外,还能完成此步转化的有___________ ;
a.Cl2 b.SO2 c.O2 d.FeCl2溶液
(3)⑤需要用的主要玻璃仪器有___________ ,静置分层后,可以看到上层溶液呈___________ 色,下层溶液呈___________ 色,若想尽可能多地将I2从水中提取到有机层中,下列操作可行的有___________ ;
a.充分振荡 b.多次萃取 c.换用酒精作为萃取剂
(4)我省深居内陆,居民可通过食用加碘食盐的方式补充碘元素的摄入,要测定食盐中的碘元素(以KIO3形式存在),可在酸性条件下加入KI将其转化为I2进行定量检测,该转化的离子方程式为___________ 。

(1)灼烧的目的是
(2)④中发生反应的离子方程式为
a.Cl2 b.SO2 c.O2 d.FeCl2溶液
(3)⑤需要用的主要玻璃仪器有
a.充分振荡 b.多次萃取 c.换用酒精作为萃取剂
(4)我省深居内陆,居民可通过食用加碘食盐的方式补充碘元素的摄入,要测定食盐中的碘元素(以KIO3形式存在),可在酸性条件下加入KI将其转化为I2进行定量检测,该转化的离子方程式为
您最近半年使用:0次
名校
解题方法
3 . 某小组设计如图所示实验探究卤素的性质,实验过程中观察到乙中现象:无色→蓝色→棕黄色→无色。已知: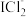 (红色)、
(红色)、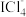 (棕色)、
(棕色)、 (无色)。
(无色)。 +5I- +6H+=3I2+3H2O。
+5I- +6H+=3I2+3H2O。
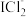 (红色)、
(红色)、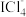 (棕色)、
(棕色)、 (无色)。
(无色)。 +5I- +6H+=3I2+3H2O。
+5I- +6H+=3I2+3H2O。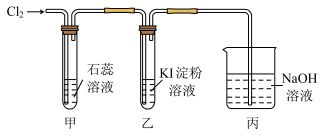
| A.丙的作用是吸收尾气,避免氯气排入空气中污染环境 |
| B.甲中现象是先变红色后褪色,微热后又变红色 |
C.乙中变棕黄色是因为I2 被氧化成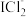 和 和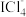 的混合物 的混合物 |
D.反应结束后,可用淀粉KI试纸和醋酸检验乙中无色溶液是否含 |
您最近半年使用:0次
2024-03-18更新
|
174次组卷
|
2卷引用:河北省2023-2024学年高三下学期3月省级联测化学试题
4 . 下列指定反应的离子方程式书写正确的是
A. 溶液与过量NaOH溶液反应: 溶液与过量NaOH溶液反应: |
B. 溶液与 溶液与 溶液反应: 溶液反应: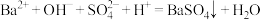 |
C.酸性条件下 溶液与KI溶液发生反应生成 溶液与KI溶液发生反应生成 : : |
D.MgO与稀盐酸反应: |
您最近半年使用:0次
5 . 碘化钾( )是重要的精细化学产品,常用于有机合成、医疗等。某同学在实验室设计如下装置制备
)是重要的精细化学产品,常用于有机合成、医疗等。某同学在实验室设计如下装置制备 (部分夹持仪器已省略)。
(部分夹持仪器已省略)。

实验步骤:
Ⅰ.______________________________;
Ⅱ.关闭 ,在各装置中加入相应试剂,向装置
,在各装置中加入相应试剂,向装置 中滴入
中滴入 的
的 溶液,制得含有
溶液,制得含有 的
的 溶液;
溶液;
Ⅱ.打开 和分液漏斗的活塞,向上述溶液中通入
和分液漏斗的活塞,向上述溶液中通入 直至饱和,可制得
直至饱和,可制得 溶液,同时有黄色沉淀生成;
溶液,同时有黄色沉淀生成;
Ⅳ.关闭 ,向Ⅲ所得混合液中滴入稀硫酸,水浴加热,使
,向Ⅲ所得混合液中滴入稀硫酸,水浴加热,使 充分逸出;
充分逸出;
Ⅴ.把装置 中混合液倒入烧杯,为除去稀硫酸,加入足量试剂
中混合液倒入烧杯,为除去稀硫酸,加入足量试剂 ,再经过一系列操作可得
,再经过一系列操作可得 成品。
成品。
回答下列问题:
(1)将步骤Ⅰ为______________________________ 。
(2)装置 中盛放
中盛放 的仪器名称为
的仪器名称为______ 。写出装置 中生成
中生成 反应的化学方程式:
反应的化学方程式:____________ 。关于该反应,下列酸能代替稀硫酸的是______ (填字母)。
a.稀盐酸 b.稀硝酸 c.亚硫酸 d.浓硫酸
(3)步骤Ⅱ生成 、
、 溶液的反应中,被氧化的碘与被还原的碘的物质的量之比为
溶液的反应中,被氧化的碘与被还原的碘的物质的量之比为______ 。
(4)写出步骤Ⅲ反应生成 的离子方程式:
的离子方程式:________________________ 。
(5)步骤Ⅴ加入足量试剂 为
为______ (填化学式),“一系列操作”包括过滤、洗涤、合并滤液、______ 。
(6) 纯度测定
纯度测定
精确称量 样品
样品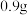 ,加水
,加水 溶解,加稀盐酸
溶解,加稀盐酸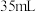 ,用
,用 的
的 溶液滴定至完全,消耗
溶液滴定至完全,消耗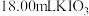 溶液,已知
溶液,已知 ,则样品中
,则样品中 的质量分数为
的质量分数为______ 。
 )是重要的精细化学产品,常用于有机合成、医疗等。某同学在实验室设计如下装置制备
)是重要的精细化学产品,常用于有机合成、医疗等。某同学在实验室设计如下装置制备 (部分夹持仪器已省略)。
(部分夹持仪器已省略)。
实验步骤:
Ⅰ.______________________________;
Ⅱ.关闭
 ,在各装置中加入相应试剂,向装置
,在各装置中加入相应试剂,向装置 中滴入
中滴入 的
的 溶液,制得含有
溶液,制得含有 的
的 溶液;
溶液;Ⅱ.打开
 和分液漏斗的活塞,向上述溶液中通入
和分液漏斗的活塞,向上述溶液中通入 直至饱和,可制得
直至饱和,可制得 溶液,同时有黄色沉淀生成;
溶液,同时有黄色沉淀生成;Ⅳ.关闭
 ,向Ⅲ所得混合液中滴入稀硫酸,水浴加热,使
,向Ⅲ所得混合液中滴入稀硫酸,水浴加热,使 充分逸出;
充分逸出;Ⅴ.把装置
 中混合液倒入烧杯,为除去稀硫酸,加入足量试剂
中混合液倒入烧杯,为除去稀硫酸,加入足量试剂 ,再经过一系列操作可得
,再经过一系列操作可得 成品。
成品。回答下列问题:
(1)将步骤Ⅰ为
(2)装置
 中盛放
中盛放 的仪器名称为
的仪器名称为 中生成
中生成 反应的化学方程式:
反应的化学方程式:a.稀盐酸 b.稀硝酸 c.亚硫酸 d.浓硫酸
(3)步骤Ⅱ生成
 、
、 溶液的反应中,被氧化的碘与被还原的碘的物质的量之比为
溶液的反应中,被氧化的碘与被还原的碘的物质的量之比为(4)写出步骤Ⅲ反应生成
 的离子方程式:
的离子方程式:(5)步骤Ⅴ加入足量试剂
 为
为(6)
 纯度测定
纯度测定精确称量
 样品
样品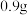 ,加水
,加水 溶解,加稀盐酸
溶解,加稀盐酸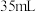 ,用
,用 的
的 溶液滴定至完全,消耗
溶液滴定至完全,消耗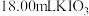 溶液,已知
溶液,已知 ,则样品中
,则样品中 的质量分数为
的质量分数为
您最近半年使用:0次
名校
解题方法
6 . 下列指定反应的离子方程式书写正确的是
A. 溶液与过量NaOH溶液反应: 溶液与过量NaOH溶液反应: |
B. 溶液与 溶液与 溶液反应: 溶液反应: |
C.酸性条件下 溶液与KI溶液发生反应生成I2: 溶液与KI溶液发生反应生成I2: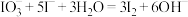 |
D.KBr与 发生置换反应生成 发生置换反应生成 : : |
您最近半年使用:0次
2024-01-08更新
|
70次组卷
|
2卷引用:辽宁省阜新市高级中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
7 . 根据所学知识,完成下列问题
Ⅰ.现有下列十种物质:①蔗糖 ②熔融 ③稀盐酸 ④液氨 ⑤高锰酸钾粉末 ⑥
③稀盐酸 ④液氨 ⑤高锰酸钾粉末 ⑥ ⑦
⑦ 晶体 ⑧乙醇 ⑨饱和
晶体 ⑧乙醇 ⑨饱和 溶液 ⑩铜丝
溶液 ⑩铜丝
(1)上述状态下物质中可导电的是________ (填序号,下同);
(2)上述状态下物质中不能导电,但属于电解质的是________ ;
(3)写出用物质⑨制备胶体的离子方程式:________ ,设计简单的方法判断胶体已制备成功________ 。
Ⅱ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾( )。碘酸钾和氢碘酸溶液能发生下列反应:
)。碘酸钾和氢碘酸溶液能发生下列反应:
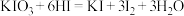
(4)请用单线桥法标出该反应的电子转移的方向和数目:________ .
(5)该反应的还原剂是________ (填化学式),还原产物是________ (填化学式)。
Ⅲ.高铁酸钠 是一种新型绿色消毒剂,可以用次氯酸钠溶液和铁盐溶液进行制备,其制备原理如下:
是一种新型绿色消毒剂,可以用次氯酸钠溶液和铁盐溶液进行制备,其制备原理如下:
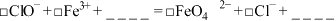
(6)请补齐上述方程式,并对该方程式进行配平:________
Ⅰ.现有下列十种物质:①蔗糖 ②熔融
 ③稀盐酸 ④液氨 ⑤高锰酸钾粉末 ⑥
③稀盐酸 ④液氨 ⑤高锰酸钾粉末 ⑥ ⑦
⑦ 晶体 ⑧乙醇 ⑨饱和
晶体 ⑧乙醇 ⑨饱和 溶液 ⑩铜丝
溶液 ⑩铜丝(1)上述状态下物质中可导电的是
(2)上述状态下物质中不能导电,但属于电解质的是
(3)写出用物质⑨制备胶体的离子方程式:
Ⅱ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(
 )。碘酸钾和氢碘酸溶液能发生下列反应:
)。碘酸钾和氢碘酸溶液能发生下列反应: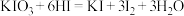
(4)请用单线桥法标出该反应的电子转移的方向和数目:
(5)该反应的还原剂是
Ⅲ.高铁酸钠
 是一种新型绿色消毒剂,可以用次氯酸钠溶液和铁盐溶液进行制备,其制备原理如下:
是一种新型绿色消毒剂,可以用次氯酸钠溶液和铁盐溶液进行制备,其制备原理如下: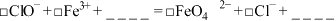
(6)请补齐上述方程式,并对该方程式进行配平:
您最近半年使用:0次
名校
解题方法
8 . 为检验某加碘食盐中是否含有 ,取相同食盐样品进行下表所示实验:
,取相同食盐样品进行下表所示实验:
已知:
下列说法中正确的是
 ,取相同食盐样品进行下表所示实验:
,取相同食盐样品进行下表所示实验:已知:

| 实验① | 实验② | 实验③ |
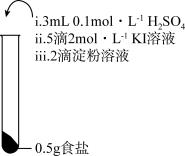 | 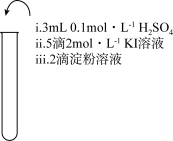 | 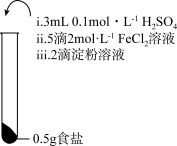 |
| 振荡,溶液迅速变为蓝色 | 振荡,一段时间后溶液变为浅蓝色 | 振荡,溶液变为浅黄色 |
A.仅由实验①就能证明食盐样品中存在 |
B.以上实验说明离子的还原性: |
C.实验③能证明食盐样品中不存在 |
D.实验②中发生反应的离子方程式为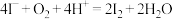 |
您最近半年使用:0次
2023-11-04更新
|
284次组卷
|
2卷引用:北京交通大学附属中学2023-2024学年高一上学期期中考试化学试题
解题方法
9 . 室温下,探究0.1mol∙L-1NaHSO3溶液的性质,下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | 是否含有 | 向2mL NaHSO3溶液中滴加几滴Ba(NO3)2溶液,观察溶液中是否有白色沉淀产生 |
| B |  是否水解 是否水解 | 向2mL NaHSO3溶液中滴加几滴酚酞试液,观察溶液颜色变化 |
| C |  是否有还原性 是否有还原性 | 向2mL NaHSO3溶液中滴加几滴KMnO4溶液,观察溶液颜色变化 |
| D |  是否有氧化性 是否有氧化性 | 向2mL NaHSO3溶液中滴加几滴KIO3溶液,充分反应后滴加几滴淀粉溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 下列离子方程式书写不正确的是
A.少量Cl2通入Na2SO3溶液中: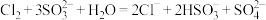 |
B.向明矾溶液中滴加 溶液至沉淀物质的量最大: 溶液至沉淀物质的量最大: |
C.将稀醋酸加入NaIO3和NaI的混合溶液中: |
D.将少量稀硝酸加入硫酸亚铁溶液中: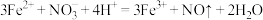 |
您最近半年使用:0次



