2024高一上·黑龙江·学业考试
1 . 海洋是一个巨大的化学资源宝库,其中含量较高的离子有
A. | B. | C. | D. |
您最近一年使用:0次
23-24高一下·全国·课后作业
2 . 海洋中有丰富的资源,下图为海水资源利用的部分过程。下列有关说法正确的是
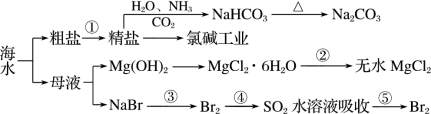
A.在第①步中除去粗盐中的 、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.操作④的目的是对溴进行富集 |
| C.工业上通过电解饱和 MgCl2溶液制取金属镁 |
D.反应④的离子方程式为:Br2+SO2+2H2O=2HBr+2H++SO |
您最近一年使用:0次
解题方法
3 . 海水中有取之不尽的化学资源,从海水中可提取多种化工原料。如图是某工厂综合利用海水资源的示意图。
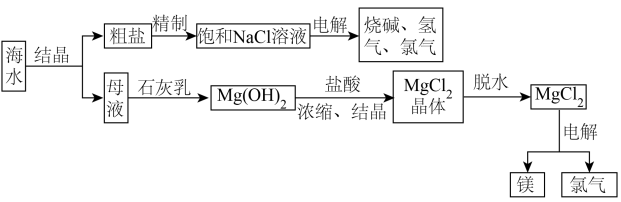
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、 等杂质,精制后可得饱和NaCl溶液。精制过程中,通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,最后向溶液中加入盐酸至溶液呈中性。写出加入盐酸后溶液中可能发生反应的离子方程式:
等杂质,精制后可得饱和NaCl溶液。精制过程中,通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,最后向溶液中加入盐酸至溶液呈中性。写出加入盐酸后溶液中可能发生反应的离子方程式:___________ 。
(2)海水中提取食盐后的母液中含有K+、Na+、Mg2+等。从离子反应的角度考虑,向母液中加入石灰乳的作用是___________ 。
(3)海水中的镁元素处于___________ (填“游离态”或“化合态”),从海水中提取氯化镁的反应___________ (填“是”或“不是”)氧化还原反应,用电解法冶炼金属镁的反应___________ (填“是”或“不是”)氧化还原反应,原因是___________ 。
(4)电解熔融的氯化镁所得的镁蒸气冷却后即为固体镁,可以冷却镁蒸气的气体氛围为___________(填字母)。

试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、
 等杂质,精制后可得饱和NaCl溶液。精制过程中,通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,最后向溶液中加入盐酸至溶液呈中性。写出加入盐酸后溶液中可能发生反应的离子方程式:
等杂质,精制后可得饱和NaCl溶液。精制过程中,通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,最后向溶液中加入盐酸至溶液呈中性。写出加入盐酸后溶液中可能发生反应的离子方程式:(2)海水中提取食盐后的母液中含有K+、Na+、Mg2+等。从离子反应的角度考虑,向母液中加入石灰乳的作用是
(3)海水中的镁元素处于
(4)电解熔融的氯化镁所得的镁蒸气冷却后即为固体镁,可以冷却镁蒸气的气体氛围为___________(填字母)。
| A.H2 | B.CO2 | C.空气 | D.O2 |
您最近一年使用:0次
4 . 下列关于粗盐提纯的说法中正确的是
| A.溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解 |
| B.滤去不溶性杂质后,将滤液移至蒸发皿内加热浓缩 |
| C.当蒸发到剩余少量液体时停止加热,利用余热将液体蒸干 |
| D.将制得的晶体转移到新制过滤器中用大量水洗涤 |
您最近一年使用:0次
解题方法
5 . 海洋是一个巨大的化学资源宝库。海水综合利用的部分流程如下:
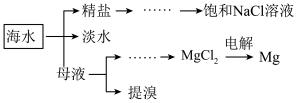
已知:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。
(1)粗盐中常含Ca2+、Mg2+、SO 等杂质离子,可依次加入NaOH溶液、
等杂质离子,可依次加入NaOH溶液、_______ 、_______ 、稀盐酸来进行提纯。
(2)从分离出粗盐后的海水(苦卤)中提取溴的流程如下:
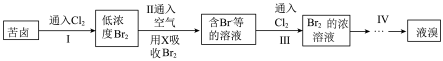
回答下列问题:
①若X试剂为SO2该反应的化学方程式是_______ 。
②步骤Ⅲ的离子反应方程式:_______ 。
③工业上每获得1molBr2,需要消耗标准状况下Cl2_______ L。
④步骤Ⅳ包含萃取、分液和蒸馏,萃取用到的萃取剂是_______ (填四氯化碳或酒精),分液时,下层液体先从_______ ,上层液体从_______ 。

已知:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。
(1)粗盐中常含Ca2+、Mg2+、SO
 等杂质离子,可依次加入NaOH溶液、
等杂质离子,可依次加入NaOH溶液、(2)从分离出粗盐后的海水(苦卤)中提取溴的流程如下:

回答下列问题:
①若X试剂为SO2该反应的化学方程式是
②步骤Ⅲ的离子反应方程式:
③工业上每获得1molBr2,需要消耗标准状况下Cl2
④步骤Ⅳ包含萃取、分液和蒸馏,萃取用到的萃取剂是
您最近一年使用:0次
2023-03-29更新
|
189次组卷
|
2卷引用:第1课时 金属矿物、海水资源的开发利用
22-23高一·全国·课时练习
6 . 从海水中可提取多种化工原料,下图是工业上对海水的几项综合利用的示意图。试回答下列问题:
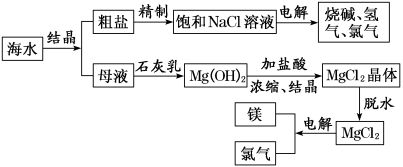
(1)写出用海滩上的贝壳制Ca(OH)2的化学方程式:_______ ;_______ 。
(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?_______ 。
(3)电解无水MgCl2可制取镁和氯气,其中副产品氯气和粉末状熟石灰可制得漂白粉,制漂白粉的化学方程式为_______ 。
(4)用海滩上的贝壳制Ca(OH)2,而不从异地山中开凿石灰石制取,主要考虑到_______ 问题。
(5)从经济效益角度看,该化工厂厂址应选在_______ 。

(1)写出用海滩上的贝壳制Ca(OH)2的化学方程式:
(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?
(3)电解无水MgCl2可制取镁和氯气,其中副产品氯气和粉末状熟石灰可制得漂白粉,制漂白粉的化学方程式为
(4)用海滩上的贝壳制Ca(OH)2,而不从异地山中开凿石灰石制取,主要考虑到
(5)从经济效益角度看,该化工厂厂址应选在
您最近一年使用:0次
22-23高一·全国·课后作业
7 . 下列有关海水综合利用的说法正确的是
| A.利用电解的方法可以从海水中获取淡水 |
| B.海水中含有钾元素,只需经过物理变化可以得到钾单质 |
| C.海水蒸发制海盐的过程只发生了化学变化 |
| D.从海水中可以得到NaCl, 电解熔融NaCl可制备Na |
您最近一年使用:0次
8 . 科学、可持续、合理利用资源是习近平建立新时代中国特色社会主义思想的重要组成部分。下列有关资源开发和利用的说法不正确的是
| A.煤的干馏,又称为煤的焦化,属于化学变化 |
| B.通过石油裂化和裂解可以得到乙烯等重要化工原料 |
| C.以石油、煤、天然气为原料,可获得性能优异的高分子材料 |
| D.从海水中提取粗盐、溴单质、镁及其化工产品的过程中均涉及氧化还原反应 |
您最近一年使用:0次
2023-01-15更新
|
236次组卷
|
5卷引用:第八章 化学与可持续发展 单元测试
9 . 海水中蕴藏着丰富的资源。下列不需要 通过化学反应就能从海水中获得的物质是
| A.粗盐 | B.金属镁 | C.烧碱 | D.氯气 |
您最近一年使用:0次
2023-01-05更新
|
133次组卷
|
2卷引用:第1课时 金属矿物、海水资源的开发利用1
解题方法
10 . 海水是一个巨大的化学资源宝库。下列有关海水综合利用的说法中,正确的是
| A.从海水中可以获得NaCl,电解NaCl溶液可制备金属钠 |
| B.从海水中提取碘的过程中利用了氧化还原反应原理 |
| C.海水中含有镁元素,只需经过物理变化就可以得到镁单质 |
| D.目前工业上可直接从海水中提取Br2 |
您最近一年使用:0次
2022-12-07更新
|
105次组卷
|
2卷引用:化学与可持续发展——课时1金属矿物和海水资源的开发利用



