解题方法
1 . 元素周期表和元素周期律对认识元素的结构与性质有着重要作用。结合Cl、S、Br等元素在周期表中的位置及其结构特点,请按要求回答下列问题。
(1)氯元素的原子结构示意图为______ ,在元素周期表中的位置为第三周期第______ 族。
(2)Cl、S的原子半径较大的是_______ (填元素符号);二者最高价氧化物对应的水化物酸性较强的是_______ (填化学式)。
(3)Cl2、Br2分别与H2反应生成的氢化物中稳定性较强的是_______ (填化学式)。
(4)使用点滴板进行同主族、同周期元素性质递变规律的实验,如下图所示。_______ (填编号)中溶液颜色变化,可得出氧化性:Cl2>Br2的结论。
②孔穴4中反应的离子方程式为_______ 。
③观察到孔穴6中溶液出现淡黄色浑浊,写出其中反应的化学方程式:_______ 。
(5)Cl2和CH4光照条件下反应的装置如图所示。_______ (任写一个)。
②写出其中生成CH3Cl的化学方程式:_______ ;其反应类型为_______ 反应。
(1)氯元素的原子结构示意图为
(2)Cl、S的原子半径较大的是
(3)Cl2、Br2分别与H2反应生成的氢化物中稳定性较强的是
(4)使用点滴板进行同主族、同周期元素性质递变规律的实验,如下图所示。
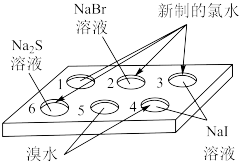
②孔穴4中反应的离子方程式为
③观察到孔穴6中溶液出现淡黄色浑浊,写出其中反应的化学方程式:
(5)Cl2和CH4光照条件下反应的装置如图所示。
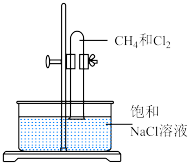
②写出其中生成CH3Cl的化学方程式:
您最近一年使用:0次
2 . 丙烯酸(CH2=CHCOOH)是一种重要的化工原料。用它合成的聚丙烯酸(PAA)对水中碳酸钙和氢氧化钙有优良的分解作用。它能发生如下转化:
(1)反应①的反应类型为_______ ; 物质B的官能团名称为_______ 。
(2)物质C的结构简式为_______ 。
(3)写出反应③的化学方程式_______ 。
(4)下列说法正确的是_______。
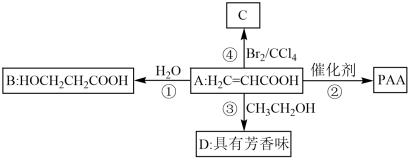
(1)反应①的反应类型为
(2)物质C的结构简式为
(3)写出反应③的化学方程式
(4)下列说法正确的是_______。
| A.物质A能使酸性高锰酸钾溶液褪色 |
| B.等物质的量的A与B在空气中完全燃烧;消耗氧气的量A小于B |
| C.可用NaOH溶液除去D中含有少量的A |
| D.PAA为高分子化合物 |
您最近一年使用:0次
3 . 某研究性学习小组制取 并探究
并探究 及铵盐的相关性质。反应的化学方程式为:
及铵盐的相关性质。反应的化学方程式为:
 。
。
查阅资料得知,铵盐通常是白色晶体,易溶于水,受热易分解,能与碱反应产生 ,浓氨水易挥发。
,浓氨水易挥发。
【制取 】
】
(1)按如图所示装置制取 ,生成的
,生成的 可用
可用_____ (填“浓硫酸”或“碱石灰”干燥)。_____ (填“向上”或“向下”)排气集气法。
(3)若生成标准状况下 ,至少需要
,至少需要 的质量为
的质量为_____ g( 的摩尔质量为
的摩尔质量为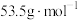 )。
)。
(4)某同学用刚清洗过、含有较多水分的集气瓶收集 ,结果收集不到气体,原因是
,结果收集不到气体,原因是_____ 。
(5)为确认某固体化肥样品中含有 ,不必用到的试纸或试剂是
,不必用到的试纸或试剂是_____ 。
① 溶液②红色石蕊试纸③稀硫酸
溶液②红色石蕊试纸③稀硫酸
 并探究
并探究 及铵盐的相关性质。反应的化学方程式为:
及铵盐的相关性质。反应的化学方程式为: 。
。查阅资料得知,铵盐通常是白色晶体,易溶于水,受热易分解,能与碱反应产生
 ,浓氨水易挥发。
,浓氨水易挥发。【制取
 】
】(1)按如图所示装置制取
 ,生成的
,生成的 可用
可用
(3)若生成标准状况下
 ,至少需要
,至少需要 的质量为
的质量为 的摩尔质量为
的摩尔质量为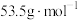 )。
)。(4)某同学用刚清洗过、含有较多水分的集气瓶收集
 ,结果收集不到气体,原因是
,结果收集不到气体,原因是(5)为确认某固体化肥样品中含有
 ,不必用到的试纸或试剂是
,不必用到的试纸或试剂是①
 溶液②红色石蕊试纸③稀硫酸
溶液②红色石蕊试纸③稀硫酸
您最近一年使用:0次
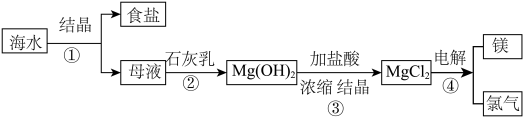
4 . 海水是重要资源,从海水中提取镁的流程如下图所示。_____ (填“降温”或“蒸发”)结晶法。
(2)步骤②分离 沉淀与溶液的实验操作名称为
沉淀与溶液的实验操作名称为_____ 。
(3)流程图的4个步骤中发生了氧化还原反应的是_____ 。(填序号)。
(4)步骤③发生反应的化学方程式为_____ 。
(2)步骤②分离
 沉淀与溶液的实验操作名称为
沉淀与溶液的实验操作名称为(3)流程图的4个步骤中发生了氧化还原反应的是
(4)步骤③发生反应的化学方程式为
您最近一年使用:0次
解题方法
5 . 下表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列各题。
(1)这10种元素中,化学性质最稳定的元素是_____ (写元素符号)。
(2)地壳中含量最丰富的元素是_____ (写元素名称)。
(3)元素①②③最高价氧化物对应的水化物,碱性最强的物质名称是_____
(4)元素⑥的氢化物的化学式是_____ (写一种)。
(5)④⑥⑦中原子半径由大到小的顺序是_____ (写元素名称)
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ④ | ⑥ | ⑦ | |||||
| 3 | ① | ② | ③ | ⑤ | ⑧ | ⑨ | ⑩ | |
(1)这10种元素中,化学性质最稳定的元素是
(2)地壳中含量最丰富的元素是
(3)元素①②③最高价氧化物对应的水化物,碱性最强的物质名称是
(4)元素⑥的氢化物的化学式是
(5)④⑥⑦中原子半径由大到小的顺序是
您最近一年使用:0次
解题方法
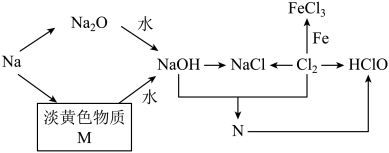
6 . 钠元素、氯元素及其它们对应的化合物有如下图转化关系。淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,物质N常被用来杀菌消毒。请按要求填空: ___________ 中;金属钠在空气中燃烧时火焰颜色呈___________ 色。
(2)写出物质M与水反应的化学方程式:___________ ,该反应中的氧化剂为___________ ;当生成标准状况下的氧气11.2 L时,转移电子数目为___________ (用NA表示阿伏加德罗常数的值)。
(3)新制的氯水呈___________ 色,放置一段时间后,溶液的pH___________ (填“增大”或“减小”)。
(4)物质N在空气中的CO2作用下,能产生有漂白、杀菌作用的次氯酸,该反应的化学方程式为NaClO+CO2+H2O=NaHCO3+HClO,该反应___________ (填“属于”或“不属于”)氧化还原反应。
(5)在酸性条件下,向铬废水中加入绿矾(FeSO4·7H2O),可将Cr2O 还原为Cr3+,该反应的离子方程式为
还原为Cr3+,该反应的离子方程式为___________ 。
(2)写出物质M与水反应的化学方程式:
(3)新制的氯水呈
(4)物质N在空气中的CO2作用下,能产生有漂白、杀菌作用的次氯酸,该反应的化学方程式为NaClO+CO2+H2O=NaHCO3+HClO,该反应
(5)在酸性条件下,向铬废水中加入绿矾(FeSO4·7H2O),可将Cr2O
 还原为Cr3+,该反应的离子方程式为
还原为Cr3+,该反应的离子方程式为
您最近一年使用:0次
解题方法
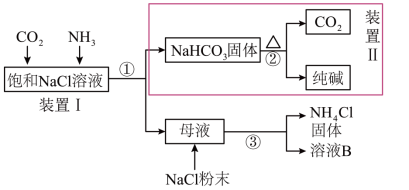
7 . 我国化学家侯德榜早在1929年改进了纯碱的生产技术,创立了“侯氏制碱法”,其产品获美国费城万国博览会金奖。某化学兴趣小组在实验室中模拟“侯氏制碱法”制备NaHCO3,进一步处理得到产品Na2CO3,和NH4Cl,实验流程如下所示。
(1)上述流程中,①②③所涉及的操作方法属于“过滤”的有___________ (填序号)。过滤时,所需要的玻璃仪器:烧杯、___________ 、___________ 。
(2)装置I中发生反应的化学方程式为CO2+NH3+NaCl+H2O=NaHCO3↓+NH4C1,向装置I的饱和NaCl溶液中通入足量的CO2,和NH3,应先通入___________ (填“CO2”或“NH3”)。
(3)检验装置Ⅱ中制备的纯碱含有Cl-的方法:取少量该纯碱样品溶于水,加入足量的稀硝酸,再加入硝酸银溶液,若出现___________ ,则说明含有Cl-。
(4)整个实验流程中,可循环利用的物质的化学式是___________ 。
(5)若装置Ⅱ中得到25.00 g的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了2.48g,则原混合物中碳酸钠的质量分数为___________ 。
(1)上述流程中,①②③所涉及的操作方法属于“过滤”的有
(2)装置I中发生反应的化学方程式为CO2+NH3+NaCl+H2O=NaHCO3↓+NH4C1,向装置I的饱和NaCl溶液中通入足量的CO2,和NH3,应先通入
(3)检验装置Ⅱ中制备的纯碱含有Cl-的方法:取少量该纯碱样品溶于水,加入足量的稀硝酸,再加入硝酸银溶液,若出现
(4)整个实验流程中,可循环利用的物质的化学式是
(5)若装置Ⅱ中得到25.00 g的碳酸钠和碳酸氢钠的固体混合物,加热至混合物质量不再变化,固体质量共减少了2.48g,则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
解题方法
8 . 表列出了①~⑨九种元素在周期表中的位置:
(1)①~⑨九种元素中原子半径最大的是__________ (填元素符号)。
(2)元素③的原子结构示意图为__________ ;元素①与⑨组成的化合物的电子式:___________ ;由⑤、⑥两种元素组成的化合物的化学键类型为__________ (“离子键”或“共价键”)。
(3)元素③、④的简单氢化物的稳定性较弱的是_____________ (填化学式);元素⑧、⑨的最高价氧化物对应的水化物中,酸性较强的是_____________ (填化学式)。
(4)元素①与②所形成的最简单有机物的空间结构是__________ ,该物质与⑨的单质在光照下发生反应,该反应的产物是__________ (填“纯净物”或“混合物”)。元素①与②所形成的最简单烯烃为M,写出M与元素⑨的单质在一定条件下反应的化学方程式:_____________ ,该反应类型为__________ 。
(5)元素⑥的单质在空气中燃烧生成__________ 色固体,此固体与二氧化碳反应的化学方程式为____________ 。
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(2)元素③的原子结构示意图为
(3)元素③、④的简单氢化物的稳定性较弱的是
(4)元素①与②所形成的最简单有机物的空间结构是
(5)元素⑥的单质在空气中燃烧生成
您最近一年使用:0次
解题方法
9 . 下图所示烧瓶中充满了 ,打开止水夹,挤压胶头滴管,使水进入烧瓶。烧瓶中出现红色喷泉。回答下列问题。
,打开止水夹,挤压胶头滴管,使水进入烧瓶。烧瓶中出现红色喷泉。回答下列问题。 为
为__________ 色气体,有__________ 气味。
(2)由压力传感器的数据图可知,b点压强最小,烧瓶中压强变小的原因是_____________ 。线段cd显示压强不再变化,说明_____________ 。
(3)下列方程式中,能解释喷泉呈红色的原因是____________ (填序号)。
A.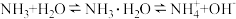
B.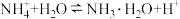
C.
(4)实验室常用加热 和
和 混合固体的方法制备
混合固体的方法制备 ,该反应的化学方程式为
,该反应的化学方程式为_____________ 。试管A管口略向下倾斜的原因是_____________ 。_____________ 。
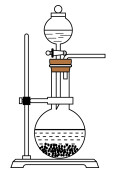
(6)实验室还可以用下边装置制取氨气,试剂可选用__________ (填字母)。
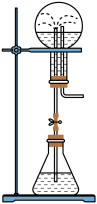
(7)某学生积极思考产生喷泉的其他方法,并设计了如图所示的装置。
①在如图所示的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是__________ (填字母)。 与稀盐酸 B.
与稀盐酸 B. 与
与 溶液C.
溶液C. 与稀硫酸 D.
与稀硫酸 D. 与稀盐酸
与稀盐酸
②在图示锥形瓶外放一水槽,瓶中加入酒精;水槽中加入水后,再加入足量的下列物质,结果也可产生喷泉。水槽中加入的物质可以是__________ (填字母)。
A.浓硫酸 B.食盐 C.硝酸钾 D.硫酸铜
 ,打开止水夹,挤压胶头滴管,使水进入烧瓶。烧瓶中出现红色喷泉。回答下列问题。
,打开止水夹,挤压胶头滴管,使水进入烧瓶。烧瓶中出现红色喷泉。回答下列问题。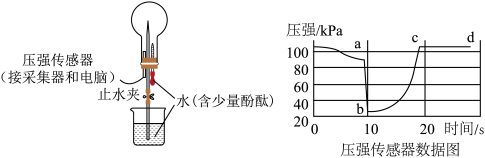
 为
为(2)由压力传感器的数据图可知,b点压强最小,烧瓶中压强变小的原因是
(3)下列方程式中,能解释喷泉呈红色的原因是
A.
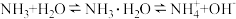
B.
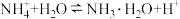
C.

(4)实验室常用加热
 和
和 混合固体的方法制备
混合固体的方法制备 ,该反应的化学方程式为
,该反应的化学方程式为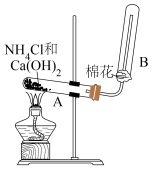
(6)实验室还可以用下边装置制取氨气,试剂可选用
(7)某学生积极思考产生喷泉的其他方法,并设计了如图所示的装置。
①在如图所示的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是
 与稀盐酸 B.
与稀盐酸 B. 与
与 溶液C.
溶液C. 与稀硫酸 D.
与稀硫酸 D. 与稀盐酸
与稀盐酸②在图示锥形瓶外放一水槽,瓶中加入酒精;水槽中加入水后,再加入足量的下列物质,结果也可产生喷泉。水槽中加入的物质可以是
A.浓硫酸 B.食盐 C.硝酸钾 D.硫酸铜
您最近一年使用:0次
解题方法
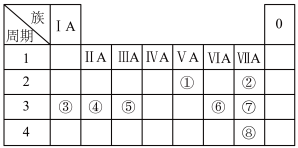
10 . 下表列出了①~⑧八种元素在周期表中的位置。
(1)元素①的原子结构示意图:________ 。
(2)元素③与⑥组成的化合物的电子式:_______ 。
(3)元素②、③的离子中,半径较大的是_______ (填化学式)。
(4)元素④的单质与盐酸反应的离子方程式:________ 。
(5)元素⑤的最高价氧化物是______ (填“酸性”“碱性”或“两性”)氧化物。
(6)元素⑦、⑧形成单质的氧化性较弱的是______ (填化学式),从实验证据的角度列举能证明其氧化性强弱关系的反应:_______ (填化学方程式)。
(7)已知硒(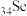 )与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:
)与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:_______ (填序号)。
a.Se的最低负化合价为-2价 b. 既有氧化性又有还原性
既有氧化性又有还原性
c.Se的气态氢化物的稳定性比⑥的强 d.最高价氧化物对应的水化物为
(1)元素①的原子结构示意图:
(2)元素③与⑥组成的化合物的电子式:
(3)元素②、③的离子中,半径较大的是
(4)元素④的单质与盐酸反应的离子方程式:
(5)元素⑤的最高价氧化物是
(6)元素⑦、⑧形成单质的氧化性较弱的是
(7)已知硒(
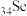 )与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:
)与⑥同主族,请根据硒元素在元素周期表中的位置,推测硒及其化合物可能具有的性质:a.Se的最低负化合价为-2价 b.
 既有氧化性又有还原性
既有氧化性又有还原性c.Se的气态氢化物的稳定性比⑥的强 d.最高价氧化物对应的水化物为

您最近一年使用:0次



