半胱氨酸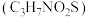 是人体细胞正常活动的必需氨基酸之一。
是人体细胞正常活动的必需氨基酸之一。
(1)组成半胱氨酸的元素中,位于元素周期表第三周期的是_______ 。
(2)非金属性N强于C。
①事实依据: 的酸性比
的酸性比
_______ (填“强”或“弱”)。
②从原子结构角度解释:N和C位于同一周期,原子核外电子层数相同,_______ ,原子半径N小于C,得电子能力N强于C。
(3)半胱氨酸分子中的硫原子被硒(Se)原子取代后称为硒代半胱氨酸,硒代半胱氨酸分子是潜在的抗癌分子药物。Se与O、S在元素周期表中位于同一主族。下列推测正确的是_______ (填字母)。
a.Se的最低化合价为 价
价
b.原子半径:
c.将 通入
通入 溶液中,可生成S
溶液中,可生成S
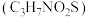 是人体细胞正常活动的必需氨基酸之一。
是人体细胞正常活动的必需氨基酸之一。(1)组成半胱氨酸的元素中,位于元素周期表第三周期的是
(2)非金属性N强于C。
①事实依据:
 的酸性比
的酸性比
②从原子结构角度解释:N和C位于同一周期,原子核外电子层数相同,
(3)半胱氨酸分子中的硫原子被硒(Se)原子取代后称为硒代半胱氨酸,硒代半胱氨酸分子是潜在的抗癌分子药物。Se与O、S在元素周期表中位于同一主族。下列推测正确的是
a.Se的最低化合价为
 价
价b.原子半径:

c.将
 通入
通入 溶液中,可生成S
溶液中,可生成S
更新时间:2024-05-22 18:02:19
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】比较下列粒子的半径大小
①Na Mg O F___________________
②Na+ Mg2+ O2- F-___________________
③ Na+ Mg2+ S2- Cl-___________________
①Na Mg O F
②Na+ Mg2+ O2- F-
③ Na+ Mg2+ S2- Cl-
您最近一年使用:0次
【推荐2】原子或离子半径的比较方法
(1)同种元素的离子半径:阴离子_______ 于原子,原子_______ 于阳离子,低价阳离子_______ 于高价阳离子。例如:r(Cl-)>r(Cl),r(Fe)>r(Fe2+)>r(Fe3+)。
(2)能层结构相同的离子:核电荷数越_______ ,半径越_______ 。例如:r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+)。
(3)带相同电荷的离子:能层数越_______ ,半径越_______ 。例如:r(Li+)<r(Na+)<r(K+)_______ r(Rb+)<r(Cs+),r(O2-)<r(S2-) _______ (Se2-)<r(Te2-)。
(4)核电荷数、能层数均不同的离子:可选一种离子参照比较。例如:比较r(K+)与r(Mg2+),可选r(Na+)为参照,r(K+)_______ r(Na+) _______ r(Mg2+)。
(1)同种元素的离子半径:阴离子
(2)能层结构相同的离子:核电荷数越
(3)带相同电荷的离子:能层数越
(4)核电荷数、能层数均不同的离子:可选一种离子参照比较。例如:比较r(K+)与r(Mg2+),可选r(Na+)为参照,r(K+)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】据《中国质量报》报道,我国首次将星载铷(Rb)钟应用于海洋二号卫星,已知 的原子序数为37。回答下列有关铷的问题:
的原子序数为37。回答下列有关铷的问题:
(1) Rb的原子结构示意图中共有______ 个电子层,最外层电子数为______ 。
(2) Rb在元素周期表中的位置是______ 。
(3)取少量铷单质加入水中,可观察到其剧烈反应,放出气体______ (写化学式),在反应后的溶液中滴加紫色石蕊试液,溶液显______ 色,因为___________ (用离子方程式表示)。
(4) Rb的还原性比K的还原性______ (填“弱”或“强”)。
 的原子序数为37。回答下列有关铷的问题:
的原子序数为37。回答下列有关铷的问题:(1) Rb的原子结构示意图中共有
(2) Rb在元素周期表中的位置是
(3)取少量铷单质加入水中,可观察到其剧烈反应,放出气体
(4) Rb的还原性比K的还原性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等;氮是地球上极为丰富的元素。
(1)在光照条件下,氯气和氢气反应过程如下:
①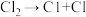 ②
②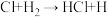 ③
③ ……
……
反应②中形成的化合物的电子式为___________ ;反应①中元素位于周期表中___________ 区
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是___________ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第___________ 周期___________ 族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是___________ 。
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—C1、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:
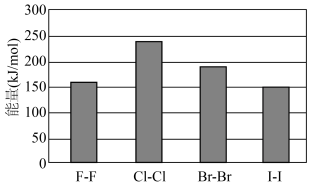
①非金属性强的卤素,其单质分子的化学键___________ 断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:___________ 。
(1)在光照条件下,氯气和氢气反应过程如下:
①
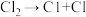 ②
②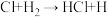 ③
③ ……
……反应②中形成的化合物的电子式为
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—C1、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:

①非金属性强的卤素,其单质分子的化学键
②卤素单质键能大小与键长的关系为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下元素及物质与人类的生产生活紧密相关。完成下列填空:
(1)氯元素原子结构示意图为_______ ,其与钠元素组成的化合物的电子式为_______ 。
(2)铝是地壳中含量最高的金属元素,其在周期表中位于第_______ 周期_______ 族。
(3)以下不是铝和铁的共同性质的是_______ 。
a.导电性 b.导热性 c.延展性 d.两性
(4)下列能说明氯元素的非金属性比硫元素强的事实是_______ 。
a.稳定性 b.氧化性
b.氧化性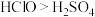
c.酸性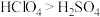 强 d.
强 d. 溶液是强酸,
溶液是强酸, 溶液是弱酸
溶液是弱酸
(1)氯元素原子结构示意图为
(2)铝是地壳中含量最高的金属元素,其在周期表中位于第
(3)以下不是铝和铁的共同性质的是
a.导电性 b.导热性 c.延展性 d.两性
(4)下列能说明氯元素的非金属性比硫元素强的事实是
a.稳定性
 b.氧化性
b.氧化性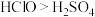
c.酸性
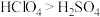 强 d.
强 d. 溶液是强酸,
溶液是强酸, 溶液是弱酸
溶液是弱酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是周期表中的一部分,根据①--⑩在周期表中的位置,用元素符号 或化学式 回答下列问题:
(1)表中元素,化学性质最不活泼的是______ ,还原性最强的单质是______ ,可用于制半导体材料的元素是______ ;
(2)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是______ ;
(3)比较⑥、⑦、⑨的氢化物的稳定性最弱的是______ ;
(4)铍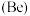 位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加______ (填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式__________ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ④ | ⑦ | ⑧ | ⑩ | ||||
| 3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(1)表中元素,化学性质最不活泼的是
(2)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是
(3)比较⑥、⑦、⑨的氢化物的稳定性最弱的是
(4)铍
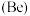 位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
您最近一年使用:0次



