按要求回答下列问题:
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有___________ (填字母,下同),属于酸性氧化物的有___________ 。
②Fe2(SO4)3溶于水的电离方程式为___________ 。
③写出实验室制取Fe(OH)3胶体的离子方程式:___________ 。
④写出H与足量A反应的离子方程式:___________ 。
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:___________ 。

②该反应中的还原剂为___________ (填化学式),被还原的物质与被氧化的物质的物质的量之比为___________ 。
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=___________ 。
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有
②Fe2(SO4)3溶于水的电离方程式为
③写出实验室制取Fe(OH)3胶体的离子方程式:
④写出H与足量A反应的离子方程式:
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:

②该反应中的还原剂为
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为
 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=
更新时间:2024/05/24 16:01:40
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.现有下列10种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤NaOH,⑥硫酸铜溶液,⑦HCl,⑧NaHSO4,⑨碳酸氢钠,⑩乙醇。
(1)上述物质中属于非电解质的有_______________ (填序号)。
(2)向⑥中加入过氧化钠固体,看到的现象是________________ 。
(3)⑧在水中的电离方程式为______________ 。
(4)②和⑤的溶液混合,反应的离子方程式为_____________ 。
(5)⑦的浓溶液与软锰矿反应制取氯气的离子方程式为______________ 。
Ⅱ.已知离子还原性BrFe2I,则氧化性Fe3+______ I2(填“>”“=”或“<”),有一混合溶液,其中只含有Fe2+、Br-、I-,其中Br-、I-的个数比为3:4,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是_______ 。如果要使溶液中Br-、I-的个数比为3:1,通入氯气与溶液中剩余Fe2+的物质的量之比为_______ 。
(1)上述物质中属于非电解质的有
(2)向⑥中加入过氧化钠固体,看到的现象是
(3)⑧在水中的电离方程式为
(4)②和⑤的溶液混合,反应的离子方程式为
(5)⑦的浓溶液与软锰矿反应制取氯气的离子方程式为
Ⅱ.已知离子还原性BrFe2I,则氧化性Fe3+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室有如下物质:
①乙醇;②氨水;③熔融的 ;④
;④ ;⑤饱和氯化铁溶液;⑥氢氧化铁胶体;⑦纯
;⑤饱和氯化铁溶液;⑥氢氧化铁胶体;⑦纯 ;⑧
;⑧ 溶液;⑨
溶液;⑨ 固体
固体
回答下列问题:
(1)以上物质属于非电解质的有___________ (填编号,下同),属于电解质的有___________ 。
(2)⑨在水中的电离方程式为___________ 。
(3)区分物质⑤和⑥的实验方法是___________ 。
A.能否透过滤纸 B.丁达尔效应 C.观察颗粒大小
(4)⑥的颜色为___________ ,用⑤制备⑥的离子方程式___________ 。
(5)向⑦的水溶液中加入⑧,反应的离子方程式为___________ 。
①乙醇;②氨水;③熔融的
 ;④
;④ ;⑤饱和氯化铁溶液;⑥氢氧化铁胶体;⑦纯
;⑤饱和氯化铁溶液;⑥氢氧化铁胶体;⑦纯 ;⑧
;⑧ 溶液;⑨
溶液;⑨ 固体
固体回答下列问题:
(1)以上物质属于非电解质的有
(2)⑨在水中的电离方程式为
(3)区分物质⑤和⑥的实验方法是
A.能否透过滤纸 B.丁达尔效应 C.观察颗粒大小
(4)⑥的颜色为
(5)向⑦的水溶液中加入⑧,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有下列物质:①Ba(OH)2固体;②熔融的KHSO4;③HNO3;④稀硫酸;⑤CO2;⑥铜;⑦氨水;⑧蔗糖晶体;⑨FeCl3固体;⑩CH3COOH。请用序号填空
(1)上述状态下的物质可导电的是____ (请用序号填空)。
(2)属于电解质的是____ (请用序号填空)。
(3)属于非电解质的是____ (请用序号填空)。
(4)写出⑩的电离方程式____ 。写出KHSO4水溶液中的电离方程式____ 。
(5)请书写氢氧化钡和稀硫酸反应的离子方程式____ 。
(1)上述状态下的物质可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)写出⑩的电离方程式
(5)请书写氢氧化钡和稀硫酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号。请回答下列问题:

(1)两种物质都是电解质的是_______ (填分类标准代号)。
(2)分类标准代号A表示_______
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,该反应的离子方程式为:_______ 。

(1)两种物质都是电解质的是
(2)分类标准代号A表示
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,该反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】用一种试剂除去下列物质中的杂质(括号内物质为杂质,所用试剂均为适量),写出所加的试剂(写化学式)及有关反应的离子方程式。
(1)FeSO4溶液(CuSO4):所加试剂:_______ ,离子方程式: _______ 。
(2)Cu(Mg):所加试剂:_______ ,离子方程式: _______ 。
(3)CO(CO2):所加试剂:_______ ,离子方程式:_______ 。
(4)BaCl2(HCl):试剂_______ ,离子方程式为:_______ 。
(1)FeSO4溶液(CuSO4):所加试剂:
(2)Cu(Mg):所加试剂:
(3)CO(CO2):所加试剂:
(4)BaCl2(HCl):试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】中华民族为人类文明进步做出了巨大贡献,中国传统文化中包含许多科技知识。
I.在西汉刘安组织编撰的《淮南万毕术》中,有“曾青得铁则化为铜”记载。这说明早在西汉时期,我国劳动人民就已经发现铁能从某些含铜(+2价)化合物的溶液中置换出铜。
(1)请写出该反应的离子方程式:___________ 。
II.在明代宋应星所著的《天工开物》中,有关于石灰石的使用记载:“凡石灰(CaCO3)经火焚炼为用。”
(2)请写出石灰石CaCO3高温分解的化学方程式:___________ 。
III.在《天工开物》中,关于火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。冷定毁罐取出……即倭铅也……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
(3)请完成上述火法炼锌反应的化学方程式:ZnCO3+______ C
______ +3CO↑
(4)在该反应中,还原剂是_________ (填化学式。下同),氧化产物是___________ 。
I.在西汉刘安组织编撰的《淮南万毕术》中,有“曾青得铁则化为铜”记载。这说明早在西汉时期,我国劳动人民就已经发现铁能从某些含铜(+2价)化合物的溶液中置换出铜。
(1)请写出该反应的离子方程式:
II.在明代宋应星所著的《天工开物》中,有关于石灰石的使用记载:“凡石灰(CaCO3)经火焚炼为用。”
(2)请写出石灰石CaCO3高温分解的化学方程式:
III.在《天工开物》中,关于火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团。冷定毁罐取出……即倭铅也……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
(3)请完成上述火法炼锌反应的化学方程式:ZnCO3+

(4)在该反应中,还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生___________ 反应,说明亚硝酸钠具有___________ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有___________ 性。
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=6CeF3+16NH3↑+12H2O+N2↑,该反应中氧化剂是___________ ,还原剂是___________ ,反应中被氧化的氮原子与未被氧化的氮原子物质的量之比为___________ 。
(3)近年来,锂的含氢化合物作为氢源受到广泛关注。化合物LiNH2和LiH都是具有潜在应用价值的释氢材料。将LiNH2和LiH按一定比例混合,在催化剂作用下,所含氢全部以氢气形式放出同时生成Li3N,反应的化学方程式为___________ 。
(1)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生
(2)稀土氟化物是金属热还原法制取单一稀土金属的重要原料。微波法合成CeF3的化学方程式为6CeO2+18NH4F=6CeF3+16NH3↑+12H2O+N2↑,该反应中氧化剂是
(3)近年来,锂的含氢化合物作为氢源受到广泛关注。化合物LiNH2和LiH都是具有潜在应用价值的释氢材料。将LiNH2和LiH按一定比例混合,在催化剂作用下,所含氢全部以氢气形式放出同时生成Li3N,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.中国传统文化是人类文明的瑰宝,古代文献中记载了大量古代化学的研究成果。回答下面问题:
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭士,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为______________ 。
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C K2S+N2↑+3CO2↑,该反应的氧化剂是
K2S+N2↑+3CO2↑,该反应的氧化剂是____ ,反应转移4mol电子时,被S氧化的C有____ mol。
(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式_________________ 。
Ⅱ.“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。
(4)请写出金属钒与浓硝酸反应的离子方程式:_______________________________ 。
(5)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:_____________ 、 _____________ 。
(1)我国最原始的陶瓷约出现在距今12000年前,制作瓷器所用的原料是高岭士,其晶体化学式是Al4[Si4O10](OH)8,用氧化物表示其组成为
(2)《本草纲目》中记载:“(火药)乃焰消( KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者。”反应原理为:S+2KNO3+3C
 K2S+N2↑+3CO2↑,该反应的氧化剂是
K2S+N2↑+3CO2↑,该反应的氧化剂是(3)我国古代中药学著作《新修本草》记载的药物有844种,其中有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如瑁璃…烧之赤色…。”我国早期科技丛书《物理小适-金石类》 记载有加热青矾时的景象:“青矾厂气熏人,衣服当之易烂,载木不盛。”青矾就是绿矾( FeSO4·7H2O)。根据以上信息,写出“青矾”受热分解的化学方程式
Ⅱ.“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成VO2+。
(4)请写出金属钒与浓硝酸反应的离子方程式:
(5)V2O5是两性氧化物,与强碱反应生成钒酸盐(阴离子为VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出V2O5分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
您最近一年使用:0次
【推荐3】第ⅢA元素也称为硼族元素,除硼外其余均为金属元素。硼的应用非常广泛,可用于原子反应堆和高温技术,甚至可用来制作火箭中所用的某些结构材料。
(1)硼元素位于元素周期表第__________ 周期。铝与氢氧化钠溶液反应的离子方程式为_________________________ 。
(2)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂(主要成分为Na2B4O7·10H2O)为起始物,经过一系列反应可以得到BN、B和BF3等。

①反应a的化学方程式为________ ,为了加快反应a的化学反应速率可采取的措施有_____________ (回答一条即可)。
②生成BN的化学反应_________ (填“是”或“不是”)氧化还原反应。
③由B2O3制硼时所得到的产品不纯,主要含有的杂质为____________ 。
(3)有一类硼烷形似鸟巢,故称为巢式硼烷,如下有三种巢式硼烷的结构:
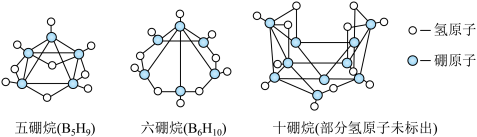
①根据五硼烷和六硼烷的化学式,推测十硼烷的化学式为_____________ 。
②已知:B6H10+O2→B2O3+H2O(未配平),每1 mol B6H10完全燃烧时转移__________ mol电子。
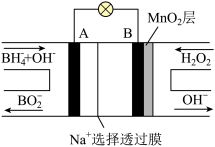
(4)NaBH4被称为“万能还原剂”,近年来常用NaBH4与过氧化氢构建一种新型碱性电池,如图所示;则该电池放电时的负极反应式为___________ ,正极附近溶液的pH会___________ 。(填“增大”、“减小”或“不变”)。
(1)硼元素位于元素周期表第
(2)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂(主要成分为Na2B4O7·10H2O)为起始物,经过一系列反应可以得到BN、B和BF3等。

①反应a的化学方程式为
②生成BN的化学反应
③由B2O3制硼时所得到的产品不纯,主要含有的杂质为
(3)有一类硼烷形似鸟巢,故称为巢式硼烷,如下有三种巢式硼烷的结构:

①根据五硼烷和六硼烷的化学式,推测十硼烷的化学式为
②已知:B6H10+O2→B2O3+H2O(未配平),每1 mol B6H10完全燃烧时转移
(4)NaBH4被称为“万能还原剂”,近年来常用NaBH4与过氧化氢构建一种新型碱性电池,如图所示;则该电池放电时的负极反应式为

您最近一年使用:0次
【推荐1】化学对生产、生活有重要的价值。
(1)工业上利用氨制备硝酸,写出氨被催化氧化生成NO的化学方程式:___ 。
(2)汽车尾气是城市空气的污染源之一。
①汽车的“催化转换器”能使尾气中的NO与CO发生反应,生成可参与大气循环的物质,写出该反应的化学方程式:___ 。
②用甲醇(CH3OH)作汽车燃料,可以降低汽车尾气对大气的污染。若80g甲醇完全燃烧转化为CO2,转移的电子数为____ 。
(3)水污染是常见的环境问题。某工业废水中可能含有大量Na+、Cl-、Cu2+和SO ,需净化后排放。
,需净化后排放。
①写出检验废水中含有SO 的实验操作、现象及结论。
的实验操作、现象及结论。___ 。
②现需将废水中Cu2+除去,且回收金属Cu。请设计处理方案并用流程图表示____ 。
(流程图示例:
 ……)
……)
(1)工业上利用氨制备硝酸,写出氨被催化氧化生成NO的化学方程式:
(2)汽车尾气是城市空气的污染源之一。
①汽车的“催化转换器”能使尾气中的NO与CO发生反应,生成可参与大气循环的物质,写出该反应的化学方程式:
②用甲醇(CH3OH)作汽车燃料,可以降低汽车尾气对大气的污染。若80g甲醇完全燃烧转化为CO2,转移的电子数为
(3)水污染是常见的环境问题。某工业废水中可能含有大量Na+、Cl-、Cu2+和SO
 ,需净化后排放。
,需净化后排放。①写出检验废水中含有SO
 的实验操作、现象及结论。
的实验操作、现象及结论。②现需将废水中Cu2+除去,且回收金属Cu。请设计处理方案并用流程图表示
(流程图示例:
 ……)
……)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属材料在生活生产中应用极其广泛,回答下列问题。
(1)过氧化钠可在呼吸面具或潜水艇中作为氧气的来源,请写出Na2O2的电子式_________ ,_________ (填“是”或“不是”)碱性氧化物。
(2)工业上,粗盐需精制,为除去Ca2+需要加入的试剂名称为_________ 。食盐中含有KIO3,可加入稀硫酸酸化的淀粉碘化钾溶液检测,若变蓝,则说明含有KIO3,写出相应反应的离子方程式____________________________________ 。等物质的量Cl2、H2O2、ClO2(还原产物为Cl-)消毒效率最高的是_________ 。
(3)已知硼酸可治疗湿疹,是一元弱酸,存在电离方程式H3BO3+H2O B(OH)
B(OH) +H+,其与过量NaOH反应得到的盐的化学式为
+H+,其与过量NaOH反应得到的盐的化学式为___________ 。
(4)含重金属离子Cu2+的废水中,可加入Na2S溶液除去,写出Na2S溶液与Cu2+发生反应的离子方程式____________________________________ ;某温度条件下,CuSO4·xH2O失掉0.5个结晶水,失重3.88%,则x=_________ 。
(1)过氧化钠可在呼吸面具或潜水艇中作为氧气的来源,请写出Na2O2的电子式
(2)工业上,粗盐需精制,为除去Ca2+需要加入的试剂名称为
(3)已知硼酸可治疗湿疹,是一元弱酸,存在电离方程式H3BO3+H2O
 B(OH)
B(OH) +H+,其与过量NaOH反应得到的盐的化学式为
+H+,其与过量NaOH反应得到的盐的化学式为(4)含重金属离子Cu2+的废水中,可加入Na2S溶液除去,写出Na2S溶液与Cu2+发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】乙二酸俗称草酸,草酸和草酸盐在化学实验中有比较重要的应用。
(1)已知草酸氢钠溶液呈酸性,请做出合理解释(结合离子方程式)______ 。
(2)已知草酸的Ka2>碳酸的Ka1,则相同浓度的Na2C2O4和碳酸钠溶液中,水的电离更强的是______ 。
(3)20.00mL 0.100mol/L VO2+离子恰好将20.00mL 0.050mol/L H2C2O4完全氧化成CO2,VO2+被还原为VOn+离子,则VOn+中的n值为______ 。
(4)草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,进行下列实验:①称取Wg草酸晶体配成100.0mL水溶液;②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L的KMnO4的溶液滴定,滴定时,所发生的反应为:______ KMnO4+______ H2C2O4+______ H2SO4=______ K2SO4+______ CO2↑______ MnSO4+______ H2O
试回答下列问题:①配平上述化学方程式。
②该实验滴定时,指示剂应该______ (填“加”或“不加”)。
③若滴定时,反应前后的两次读数分别为a mL和b mL,则实验测得的所配草酸溶液的物质的量浓度为______ ;由此计算出草酸晶体的x值是______ 。
(1)已知草酸氢钠溶液呈酸性,请做出合理解释(结合离子方程式)
(2)已知草酸的Ka2>碳酸的Ka1,则相同浓度的Na2C2O4和碳酸钠溶液中,水的电离更强的是
(3)20.00mL 0.100mol/L VO2+离子恰好将20.00mL 0.050mol/L H2C2O4完全氧化成CO2,VO2+被还原为VOn+离子,则VOn+中的n值为
(4)草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,进行下列实验:①称取Wg草酸晶体配成100.0mL水溶液;②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L的KMnO4的溶液滴定,滴定时,所发生的反应为:
试回答下列问题:①配平上述化学方程式。
②该实验滴定时,指示剂应该
③若滴定时,反应前后的两次读数分别为a mL和b mL,则实验测得的所配草酸溶液的物质的量浓度为
您最近一年使用:0次



