名校
解题方法
1 . 4种短周期主族元素X、Y、Z和Q的原子序数依次增大,相关信息如下表:
下列说法正确的是
| 元素 | 相关信息 |
| X | 最外层电子数等于次外层电子数 |
| Y | 与X在同一主族 |
| Z | 单质为淡黄色固体,难溶于水,微溶于酒精,易溶于二硫化碳 |
| Q | 同周期主族元素中原子半径最小 |
| A.X的金属性比Y强 |
| B.Y的原子半径是同周期中最大的 |
| C.Z的单质在空气燃烧和在充满氧气的集气瓶中燃烧产物相同 |
| D.Q的含氧酸与Z的含氧酸都可以混合,不发生反应 |
您最近一年使用:0次
名校
2 . 下列叙述错误的是
| A.1 mol SO2中含有2 mol氧原子和1 mol硫原子 |
| B.1 mol N2的质量为28g |
| C.0.1 mol H2O中含有的电子数目约为6.02×1023 |
| D.3.01×1023个CO2分子所占的体积约为11.2升 |
您最近一年使用:0次
名校
3 . 某实验小组通过下图所示实验,探究Na2O2与水的反应:
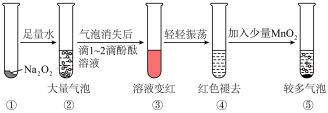
| A.②⑤中的气泡的主要成分相同,生成等物质的量的该气体转移电子的数目不同 |
| B.③中溶液变红,说明有碱性物质生成 |
| C.④中现象可能是由于溶液中含有漂白性物质造成的 |
| D.⑤中MnO2的主要作用是作催化剂 |
您最近一年使用:0次
名校
解题方法
4 . 下列关于二氧化硫性质的说法正确的是
| A.氯水中通入一定量二氧化硫气体可增强氯水的漂白性 |
| B.二氧化硫的水溶液能导电,二氧化硫是电解质 |
| C.除去二氧化碳中的二氧化硫可以用足量的酸性高锰酸钾溶液 |
| D.红酒中添加少量的二氧化硫抑菌,说明二氧化硫即无毒也无漂白性 |
您最近一年使用:0次
名校
解题方法
5 . 下列关于碳酸钠和碳酸氢钠的叙述正确的是
| A.相同条件下,在水中的溶解性:碳酸钠<碳酸氢钠 |
| B.相同条件下,溶液的碱性:碳酸钠>碳酸氢钠 |
| C.相同条件下,与酸反应产生二氧化碳气体的速率:碳酸钠>碳酸氢钠 |
| D.碳酸钠溶液和碳酸氢钠溶液可以用澄清石灰水来区别 |
您最近一年使用:0次
名校
解题方法
6 . 有关Cl2的性质,下列说法不正确的是
| A.Cl2有毒但可用于自来水消毒 |
| B.能与Ca(OH)2溶液反应生成两种正盐 |
| C.过量的Fe在氯气中燃烧生成FeCl3 |
| D.将氯气和二氧化硫分别通入到紫色石蕊溶液中现象相同 |
您最近一年使用:0次
名校
解题方法
7 . 将下列物质按酸、碱、盐、氧化物分类排列,正确的是
| A.硫酸、纯碱、生石灰、氧气 | B.醋酸、烧碱、硝酸钾、干冰 |
| C.H2SO4、甲醇(CH3OH)、CaCO3、水 | D.硝酸、熟石灰、苛性钠、甲烷 |
您最近一年使用:0次
解题方法
8 . 下列选项关于一定物质的量浓度溶液的配制说法正确的是
A.用托盘天平称量 固体的质量 固体的质量 |
B.将 胆矾溶于 胆矾溶于 水中,所得溶质物质的量浓度为 水中,所得溶质物质的量浓度为 |
| C.固体溶解放热,溶液未冷却至室温立即转移至容量瓶中完成之后操作,所配溶液浓度偏高 |
| D.定容后摇匀,发现液面低于刻度线,即加水至刻度线 |
您最近一年使用:0次
名校
解题方法
9 . 五水硫酸铜在化工、农业、医药、食品等方面均有广泛的用途,实验室制备方法如下:
(1)制备硫酸铜溶液
称取3.0g铜粉放入双颈烧瓶中,加入11.0mL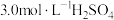 ,再分批缓慢加入5.0mL
,再分批缓慢加入5.0mL 浓
浓 ,待反应缓和后水浴加热。在加热过程中补加6.0mL
,待反应缓和后水浴加热。在加热过程中补加6.0mL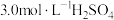 和1.0mL浓硝酸。
和1.0mL浓硝酸。
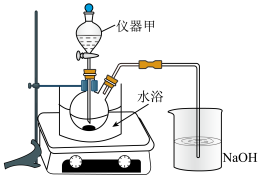
①仪器甲的名称是______ ,硝酸的主要作用是______ 。
②分批加入硝酸的主要原因是______ 。
③实验过程中,观察到有气体生成,NaOH溶液的作用是吸收______ 和______ 。
(2)制得五水硫酸铜粗品
待Cu接近于全部溶解后,趁热用倾析法将溶液转至小烧杯中,然后通过“相关操作”得到粗五水硫酸铜晶体。
①趁热用倾析法转液的目的是______ 、______ 。
②通过“相关操作”得到粗五水硫酸铜晶体,其“相关操作”是指将溶液转至蒸发皿中,水浴加热,______ 。
③如果蒸发水时温度过高,得到的晶体会偏白色,则原因是______ 。(用化学反应方程式表示)
(1)制备硫酸铜溶液
称取3.0g铜粉放入双颈烧瓶中,加入11.0mL
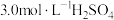 ,再分批缓慢加入5.0mL
,再分批缓慢加入5.0mL 浓
浓 ,待反应缓和后水浴加热。在加热过程中补加6.0mL
,待反应缓和后水浴加热。在加热过程中补加6.0mL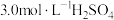 和1.0mL浓硝酸。
和1.0mL浓硝酸。
①仪器甲的名称是
②分批加入硝酸的主要原因是
③实验过程中,观察到有气体生成,NaOH溶液的作用是吸收
(2)制得五水硫酸铜粗品
待Cu接近于全部溶解后,趁热用倾析法将溶液转至小烧杯中,然后通过“相关操作”得到粗五水硫酸铜晶体。
①趁热用倾析法转液的目的是
②通过“相关操作”得到粗五水硫酸铜晶体,其“相关操作”是指将溶液转至蒸发皿中,水浴加热,
③如果蒸发水时温度过高,得到的晶体会偏白色,则原因是
您最近一年使用:0次
2024-04-04更新
|
256次组卷
|
3卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题
名校
解题方法
10 . 资源化利用CO2,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
(1)CO2的捕集:
①CO2属于___________ 分子(填“极性”或“非极性”),其晶体(干冰)属于__________ 晶体。
②用饱和 溶液做吸收剂可“捕集”CO2。若所得溶液
溶液做吸收剂可“捕集”CO2。若所得溶液 ,溶液中c(HCO
,溶液中c(HCO ):c(CO
):c(CO )=
)=_______ ;(室温下, 的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式
的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式_____ 。
③聚合离子液体是目前广泛研究的CO2吸附剂。结合下图 分析聚合离子液体吸附CO2的有利条件是____________ 。
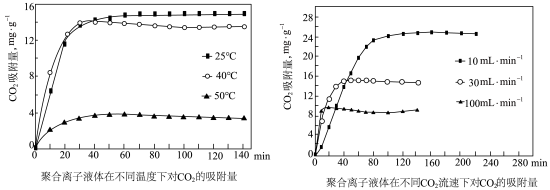
(2)生产尿素:工业上以CO2、 为原料生产尿素[CO(NH2)2],该反应分为二步进行:
为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步: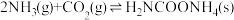
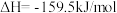
第二步:
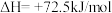
写出上述合成尿素的热化学方程式_______ 。
(3)合成乙酸:中国科学家首次以 、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
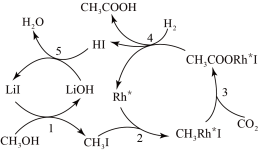
①原料中的 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:____________ 。
②根据图示 ,写出总反应的化学方程式:_______ 。
(1)CO2的捕集:
①CO2属于
②用饱和
 溶液做吸收剂可“捕集”CO2。若所得溶液
溶液做吸收剂可“捕集”CO2。若所得溶液 ,溶液中c(HCO
,溶液中c(HCO ):c(CO
):c(CO )=
)= 的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式
的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式③聚合离子液体是目前广泛研究的CO2吸附剂。

(2)生产尿素:工业上以CO2、
 为原料生产尿素[CO(NH2)2],该反应分为二步进行:
为原料生产尿素[CO(NH2)2],该反应分为二步进行:第一步:
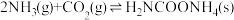
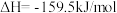
第二步:

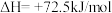
写出上述合成尿素的热化学方程式
(3)合成乙酸:中国科学家首次以
 、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
①原料中的
 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:②
您最近一年使用:0次
2024-04-04更新
|
362次组卷
|
3卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题



