湖南省2024届普通高中高三下学期学业水平选择性考试临考预测押题密卷化学试题(B卷)
湖南
高三
模拟预测
2024-05-27
291次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、化学实验基础、常见无机物及其应用、物质结构与性质
一、单选题 添加题型下试题
A.利用葡萄糖酸- -内酯使豆浆凝固 -内酯使豆浆凝固 | B.使用含氟牙膏预防龋齿 |
| C.将植物油氢化以便于运输和储存 | D.利用明矾溶液清除铜镜表面的铜锈 |
|
|
|
|
| A | B | C | D |
| A.向容量瓶中转移溶液 |
B.观察 的焰色试验 的焰色试验 |
C.测定某 溶液的浓度 溶液的浓度 |
D.证明 的酸性强于HClO 的酸性强于HClO |
A.向硫化钠溶液中通入足量二氧化硫: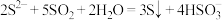 |
B.向 溶液中加入足量烧碱溶液: 溶液中加入足量烧碱溶液: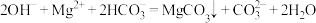 |
C.向次氯酸钙溶液中通入过量二氧化碳: |
D.向 溶液中通入少量 溶液中通入少量 : :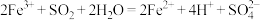 |

| A.具有热固性 | B.可通过加聚反应制得 |
C.酸性条件下水解的产物之一为 | D.所有碳原子均为 杂化 杂化 |
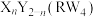 。已知:W、X、R、Y是原子序数依次增大的前四周期元素,基态W、X原子s轨道上的电子数和p轨道上的电子数都相等,基态R原子核外有14种不同运动状态的电子,Y的原子序数为X与R的原子序数之和。下列说法错误的是
。已知:W、X、R、Y是原子序数依次增大的前四周期元素,基态W、X原子s轨道上的电子数和p轨道上的电子数都相等,基态R原子核外有14种不同运动状态的电子,Y的原子序数为X与R的原子序数之和。下列说法错误的是A.第一电离能: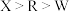 | B.简单氢化物的键角: |
| C.工业上冶炼X、Y单质的方法不同 | D.该橄榄石晶体中存在R、W形成的四面体结构 |
| 选项 | 试剂① | 试剂② |
| A |  溶液 溶液 | HCl溶液 |
| B |  溶液 溶液 | 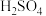 溶液 溶液 |
| C | 氨水 |  溶液 溶液 |
| D |  溶液 溶液 |  溶液 溶液 |
| A.A | B.B | C.C | D.D |
 为催化剂,利用
为催化剂,利用 、
、 制甲醇,反应机理如图所示,
制甲醇,反应机理如图所示, 表示阿伏加德罗常数的值,下列说法错误的是
表示阿伏加德罗常数的值,下列说法错误的是
A. 的电子式为 的电子式为 |
B.100g质量分数为64%的 水溶液中 水溶液中 键的数目为 键的数目为 |
| C.反应④是吸热反应 |
| D.增大催化剂的表面积可以提高反应速率 |
| 选项 | 事实 | 结论 |
| A | 热稳定性: | 热稳定性: |
| B | NaCl晶胞中 的配位数为6 的配位数为6 | CsCl晶胞中 的配位数也为6 的配位数也为6 |
| C | 电负性: | 氧化性: 单斜硫 单斜硫 |
| D | 沸点: | 沸点: |
| A.A | B.B | C.C | D.D |
【知识点】 氢键对物质性质的影响解读 常见离子晶体的结构解读
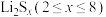 会穿梭至负极进而缩短电池寿命。科学家研制的HMSC材料(
会穿梭至负极进而缩短电池寿命。科学家研制的HMSC材料(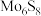 与
与 的结合体)可使
的结合体)可使 快速嵌入,并有效吸附
快速嵌入,并有效吸附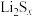 从而抑制穿梭效应。以HMSC作为电极材料的锂硫电池的结构示意图如图所示,下列说法正确的是
从而抑制穿梭效应。以HMSC作为电极材料的锂硫电池的结构示意图如图所示,下列说法正确的是
| A.乙醇可作该电池电解液的溶剂 |
B.放电时, 从HMSC中脱嵌 从HMSC中脱嵌 |
C.放电时,主要的电池反应为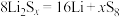 |
D.充电时,阳极的电极反应式为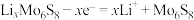 |
【知识点】 新型电池解读 原电池、电解池综合考查解读
 可发生如下转化:
可发生如下转化: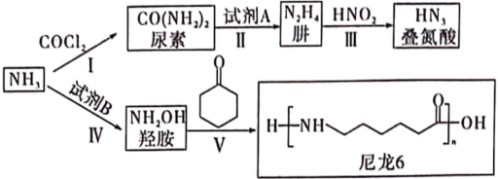
| A.基态N原子的空间运动状态有7种 |
| B.试剂A和试剂B可能为同一种物质 |
C.过程Ⅲ中若有 生成,则转移20mol电子 生成,则转移20mol电子 |
| D.过程V的原子利用率为100% |
【知识点】 基态核外电子排布规律 电子排布式解读 电子转移计算
 可用作理离子电池的电解质。以LiF、HF和
可用作理离子电池的电解质。以LiF、HF和 为原料制备
为原料制备 的某工艺流程如图所示:
的某工艺流程如图所示: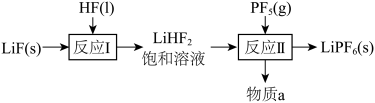
 极易水解。下列说法错误的是
极易水解。下列说法错误的是| A.“反应I”中HF既作反应物又作溶剂 | B.“反应Ⅱ”结束后,可使用玻璃漏斗过滤得到 |
| C.物质a可在该流程中循环使用 | D.整个制备过程需要在低温、干燥条件下进行 |
【知识点】 二氧化硅的化学性质解读 盐类水解在生活、生产中的应用解读
 处理NO的反应历程如图所示。下列关于该历程的说法错误的是
处理NO的反应历程如图所示。下列关于该历程的说法错误的是
A. 能降低该反应的活化能 能降低该反应的活化能 |
| B.该历程中存在Fe与O之间的电子转移 |
| C.该历程中有极性键和非极性键的断裂与形成 |
D.总反应的化学方程式为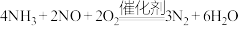 |
13. 工业中采用双环戊二烯解聚法合成环伐二烯,反应方程式为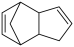 (g)
(g) 2
2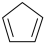 (g)
(g)  。将3mol双环戊二烯通入恒温、恒容密闭容器中,分别在
。将3mol双环戊二烯通入恒温、恒容密闭容器中,分别在 和
和 温度下进行反应,起始压强分别为
温度下进行反应,起始压强分别为 和
和 ,n(双环戊二烯)、n(环戊二烯)随时间t的变化关系如图所示。下列说法错误的是
,n(双环戊二烯)、n(环戊二烯)随时间t的变化关系如图所示。下列说法错误的是
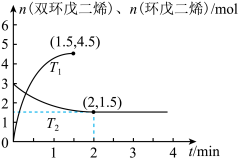
A. |
B. |
C. 温度下,当容器总压强 温度下,当容器总压强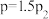 时 时 |
| D.与恒温相比,绝热条件下的平衡常数小 |
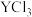 (可溶性盐)和
(可溶性盐)和 (可溶性盐)三种溶液。
(可溶性盐)三种溶液。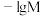 [M表示
[M表示 、
、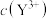 、
、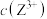 ]随溶液pH的变化如图所示。已知:
]随溶液pH的变化如图所示。已知: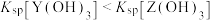 。下列说法错误的是
。下列说法错误的是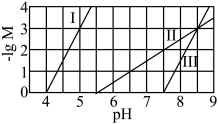
A.曲线I代表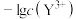 随溶液pH的变化关系 随溶液pH的变化关系 |
B. 的数量级是 的数量级是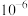 |
C. 固体能完全溶解在 固体能完全溶解在 溶液中 溶液中 |
D.滴定HX溶液至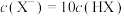 时,溶液中: 时,溶液中: |
二、解答题 添加题型下试题
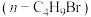 、金属镁、乙醚和丙酮为主要原料制备2-甲基-2-已醇的反应原理及主要制取装置如下:
、金属镁、乙醚和丙酮为主要原料制备2-甲基-2-已醇的反应原理及主要制取装置如下:
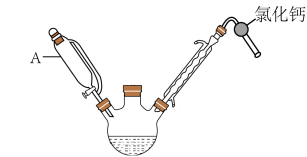
 (偶联反应,R、R′代表烃基)
(偶联反应,R、R′代表烃基)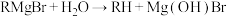
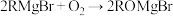
已知:
①实验中相关物质的部分性质如表所示。
| 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度 |
| 乙醚 | 74 | -116.2 | 34.5 | 0.714 |
| 丙酮 | 58 | -94.9 | 56.5 | 0.790 |
| 正溴丁烷 | 137 | -112.4 | 101.6 | 1.270 |
| 2-甲基-2-己醇 | 116 | -30.45 | 141 | 0.812 |
实验步骤:
I.制备格氏试剂:向三颈烧瓶中加入2.4g镁屑和15.00mL无水乙醚,向仪器A中加入10.80mL正溴丁烷和15.00mL无水乙醚的混合液。通入冷却水,向三颈烧瓶中滴加4.00mL混合液,引发反应。一段时间后搅拌,并缓慢滴加剩余混合液,保持微沸状态。滴加完成后,由冷凝管上口补加25.00mL无水乙醚,继续反应15分钟,使镁屑反应完全。
II.合成2-甲基-2-己醇:向三颈烧瓶中加入7.40mL丙酮和10.00mL无水乙醚的混合液,维持微沸状态,继续搅拌15分钟。向三颈烧瓶中分批加入50.00mL20%的硫酸溶液,充分反应。
III.产物的分离提纯:用分液漏斗分出醚层,水层用少许乙醚萃取,将萃取液与醚层合并、洗涤、干燥、蒸馏,得到产品5.6g。
回答下列问题:
(1)仪器A的名称是
(2)该实验中所使用的仪器和试剂都需要进行干燥处理,原因是
(3)根据上述实验药品的用量,三颈烧瓶最适宜的规格为___________(填标号)。
| A.50mL | B.100mL | C.250mL | D.500mL |
(4)步骤I中,滴加试剂后一段时间才搅拌的原因是
(5)步骤II中,为防止反应过于剧烈,需控制反应速率,可采取的措施有
(6)该实验中,乙醚除作溶剂和萃取剂外,另一个作用是
(7)下列关于步骤III的说法正确的是___________(填标号)。
| A.可用碳酸钠溶液进行洗涤 |
| B.可用无水碳酸钾或浓硫酸作干燥剂 |
| C.蒸馏时,可在陶土网上直接加热蒸出乙醚,再换接收器,继续加热蒸出产品 |
| D.得到的产品可以用重结晶法继续提纯 |
(8)产品的产率为
 受热会发生一系列的分解反应。回答下列问题:
受热会发生一系列的分解反应。回答下列问题:向容器中加入1mol乙酸钙晶体,通入一定量的Ar,加热容器开始反应。反应过程中始终保持气体总压强为p。
I.加热体系至160℃时,乙酸钙晶体先完全脱水,吸收akJ热量,再发生反应(i):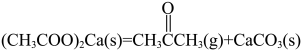 ,吸收bkJ热量。
,吸收bkJ热量。
Ⅱ.继续加热体系至500℃,发生反应(ii): 
 反应(iii):
反应(iii):
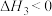 。
。
 、反应温度T的变化如图所示:
、反应温度T的变化如图所示: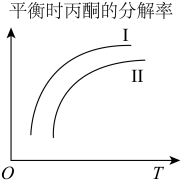
 较大的曲线为
较大的曲线为②反应(ii)可在
(3)此条件下,若
 ,平衡时丙酮的分解率为90%、
,平衡时丙酮的分解率为90%、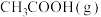 的体积分数为
的体积分数为 ,则
,则 的体积分数为
的体积分数为
Ⅲ.继续加热体系至900℃,丙酮完全分解,体系中发生如下反应(不考虑其他副反应):
(iv)

(v)
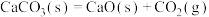
(vi)

(4)工业生产中常在镍基催化剂表面发生反应(ⅵ),其机理如图所示。步骤(d)中间体的氧化和分解涉及的主要反应有
 ,
, 以及
以及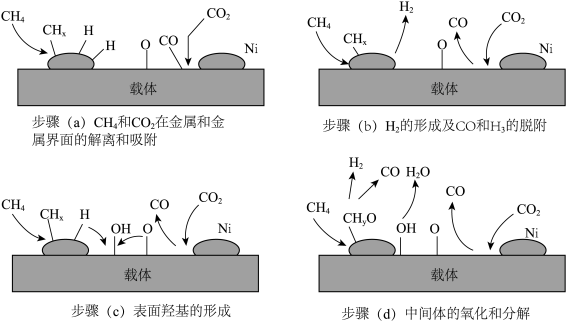
 。常温下,
。常温下,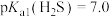 ,
, 。一些难溶电解质的
。一些难溶电解质的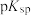 如表所示:
如表所示:| 难溶电解质 | NiS | CuS | ZnS |
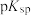 | 18.8 | 35.2 | 21.7 |
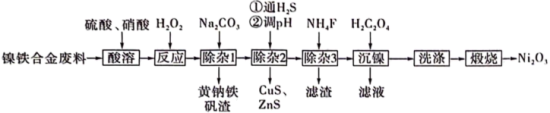
(1)“酸溶”过程中可以加快反应速率和提高浸出率的方法有
(2)“除杂1”步骤中,加入
 将溶液的pH调至1.6~1.8,得到黄钠铁矾
将溶液的pH调至1.6~1.8,得到黄钠铁矾 ,该反应的离子方程式为
,该反应的离子方程式为(3)“除杂2”步骤中,常温下,始终保持溶液中
 的浓度为
的浓度为 。为将预除杂质完全除去,应保持溶液的pH不小于
。为将预除杂质完全除去,应保持溶液的pH不小于 的浓度为
的浓度为 ,则
,则
 时,可认为该离子完全除去)。
时,可认为该离子完全除去)。(4)“沉镍”步骤中,得到的滤液中所含的阳离子主要有
(5)在空气中“煅烧”发生反应的化学方程式为
(6)Ni、Fe、O三种元素形成的某化合物可以用作催化剂,其晶胞结构如图所示。该化合物晶体的密度为
 (设
(设 为阿伏加德罗常数的值,列出计算表达式)。
为阿伏加德罗常数的值,列出计算表达式)。
18. 根据我国农药毒性分级标准,精喹禾灵(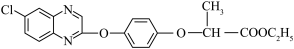 )属于低毒除草剂,作用速度快,药效稳定,不易受温度及湿度等环境条件的影响。其合成路线之一如下:
)属于低毒除草剂,作用速度快,药效稳定,不易受温度及湿度等环境条件的影响。其合成路线之一如下:
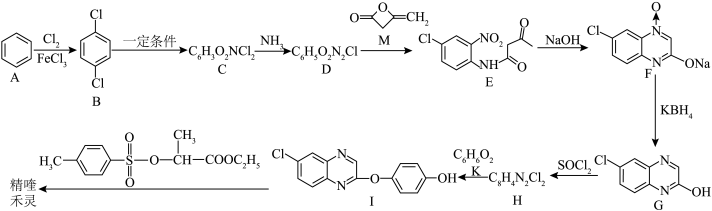
 属于间位定位基,
属于间位定位基,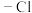 属于邻、对位定位基。
属于邻、对位定位基。回答下列问题:
(1)B→C的反应试剂及条件是
(2)D中含氧官能团的名称为
(3)K的结构简式为
(4)H→I的反应过程中,当H过量时可能会得到某一副产物,生成该副产物的化学方程式为
(5)化合物X的相对分子质量比D大14,则满足下列条件的X有
①含有
 和
和 ,且
,且 直接连在苯环上;②苯环上侧链数目小于4。
直接连在苯环上;②苯环上侧链数目小于4。其中核磁共振氢谱有4组吸收峰的X的结构简式为
(6)参考上述合成路线,设计以
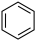 和M为原料,合成
和M为原料,合成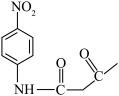 的路线
的路线试卷分析
试卷题型(共 18题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 氧化还原反应定义、本质及特征 盐类水解在生活、生产中的应用 油脂的氢化 | |
| 2 | 0.85 | 酸碱中和滴定实验基本操作及步骤 配制一定物质的量浓度的溶液的步骤、操作 物质性质实验方案的设计 | |
| 3 | 0.65 | 离子方程式的书写 离子方程式的正误判断 硝酸的强氧化性 | |
| 4 | 0.65 | 缩聚物的单体、链节及聚合度的确定 利用杂化轨道理论判断化学键杂化类型 | |
| 5 | 0.65 | 根据原子结构进行元素种类推断 电离能的概念及变化规律 价层电子对互斥理论的应用 | |
| 6 | 0.65 | 氨水的性质 碳酸钠与盐酸的反应 偏铝酸钠与盐酸的反应 | |
| 7 | 0.65 | 共价化合物的结构及形成过程 吸热反应和放热反应 催化剂对化学反应速率的影响 | |
| 8 | 0.65 | 氢键对物质性质的影响 常见离子晶体的结构 | |
| 9 | 0.65 | 新型电池 原电池、电解池综合考查 | |
| 10 | 0.65 | 基态核外电子排布规律 电子排布式 电子转移计算 | |
| 11 | 0.65 | 二氧化硅的化学性质 盐类水解在生活、生产中的应用 | |
| 12 | 0.4 | 氧化还原反应的规律 碰撞理论及活化能 活化能及其对反应速率的影响 共价键的形成及主要类型 | |
| 13 | 0.4 | 化学平衡的移动及其影响因素 化学平衡图像分析 化学平衡状态的判断方法 化学平衡常数的有关计算 | |
| 14 | 0.15 | 水的离子积常数 弱电解质在水溶液中的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 溶度积常数相关计算 | |
| 二、解答题 | |||
| 15 | 0.65 | 影响化学反应速率的外因 几种常见的酮 常见有机物的制备 物质制备的探究 | 实验探究题 |
| 16 | 0.4 | 盖斯定律与热化学方程式 化学平衡的移动及其影响因素 化学平衡图像分析 化学平衡常数的有关计算 | 原理综合题 |
| 17 | 0.4 | 溶度积常数相关计算 晶胞的有关计算 物质分离、提纯综合应用 | 工业流程题 |
| 18 | 0.4 | 根据要求书写同分异构体 同分异构体的数目的确定 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |