解题方法
1 . 下列关于肼的说法正确的是
A.电子式为 | B.既含极性键,又含非极性键 |
| C.属于极性分子 | D.N原子为sp2杂化 |
您最近一年使用:0次
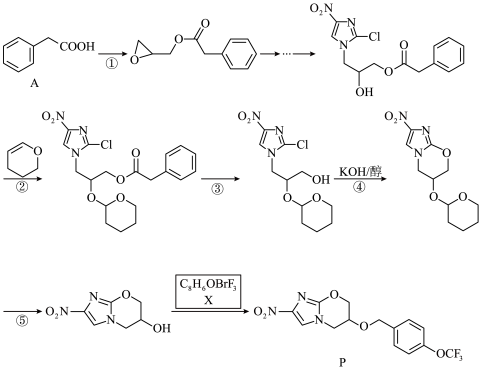
2 . 普托马尼(P)为口服的抗分枝杆菌药物,用于结核病的治疗。P的某种合成路线如下所示(部分反应条件已省略):
(2)②的反应类型是____________。
(3)③所需的反应试剂与条件为____________ 。
(4)④中生成的无机产物为____________ 。
(5)写出①的反应式:___________ 。
(6)X的结构简式为____________ 。
(7)反应②、⑤的目的是___________ 。
(8)M与X互为同分异构体,且具有如下性质,写出M的结构简式___________ 。
ⅰ.属于芳香族化合物,核磁共振氢谱有四组峰,峰面积比为1:1:2:2;
ⅱ.能与FeCl3溶液发生显色反应;
ⅲ.分子中含有一个氟甲基(-CF3)。
(9)结合题示信息,设计以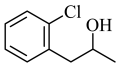 为有机原料合成
为有机原料合成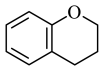 的合成路线
的合成路线___________ (其他无机试剂与溶剂任选)。
| A.0个 | B.1个 | C.2个 | D.3个 |
(2)②的反应类型是____________。
| A.加成反应 | B.取代反应 | C.消去反应 | D.氧化反应 |
(3)③所需的反应试剂与条件为
(4)④中生成的无机产物为
(5)写出①的反应式:
(6)X的结构简式为
(7)反应②、⑤的目的是
(8)M与X互为同分异构体,且具有如下性质,写出M的结构简式
ⅰ.属于芳香族化合物,核磁共振氢谱有四组峰,峰面积比为1:1:2:2;
ⅱ.能与FeCl3溶液发生显色反应;
ⅲ.分子中含有一个氟甲基(-CF3)。
(9)结合题示信息,设计以
 为有机原料合成
为有机原料合成 的合成路线
的合成路线
您最近一年使用:0次
解题方法
3 . 写出基态B原子的轨道表示式__________ ;BF3的分子构型为___________ 。
您最近一年使用:0次
4 . LiF晶胞结构如图所示。
(2)LiF晶胞中,Li+位于F-围成的________空隙中。
(3)已知该晶胞棱长为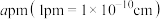 ,
, 表示阿伏加德罗常数,则LiF晶体的密度为
表示阿伏加德罗常数,则LiF晶体的密度为________ g·cm-3。
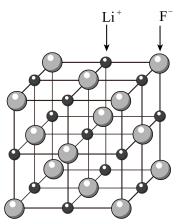
| A.氯化钠 | B.氟化钙 | C.金刚石 | D.二氧化碳 |
(2)LiF晶胞中,Li+位于F-围成的________空隙中。
| A.正四面体 | B.正八面体 |
| C.立方体 | D.平面正方形 |
(3)已知该晶胞棱长为
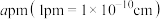 ,
, 表示阿伏加德罗常数,则LiF晶体的密度为
表示阿伏加德罗常数,则LiF晶体的密度为
您最近一年使用:0次
5 . FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下方法来制备无水FeCl2。有关物质的性质如下:
方法一:用H2还原无水FeCl3制取FeCl2。有关装置如下:____________ 。
(2)按气流由左到右的方向,上述仪器的连接顺序为____________。
(3)该制备装置的缺点为____________ 。
方法二:利用反应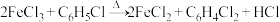 制取无水FeCl2,并通过测定HCl的量来计算FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N2一段时间,分离提纯得到粗产品。
制取无水FeCl2,并通过测定HCl的量来计算FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N2一段时间,分离提纯得到粗产品。_____________ 。
(5)仪器b中干燥剂可以选择_____________。
(6)反应结束后恢复至室温,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用最佳试剂是___________ 。
(7)回收滤液中C6H6Cl的操作方法是_____________。
(8)反应后将c中溶液稀释至250mL。量取25.00mL所配溶液,用0.400mol·L-1标准NaOH溶液滴定,终点时消耗标准液19.60mL。则氯化铁的转化率为___________ 。
(9)若反应后通入N2时间不足,则测得氯化铁的转化率______________ 。
A.偏低 B.偏高 C.不影响
(10)制备无水FeCl2需要用到无水FeCl3,某同学提出利用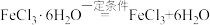 制备无水FeCl3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方
制备无水FeCl3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方_______________ 。
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯;易溶于乙醇,易吸水 | ||
| 熔点/℃ | -45 | 53 | 100℃时升华 | 672 |
| 沸点/℃ | 132 | 173 | >1000 | |
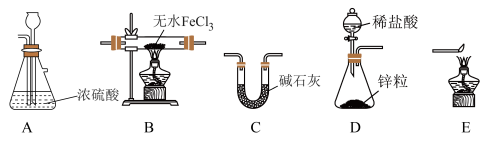
(2)按气流由左到右的方向,上述仪器的连接顺序为____________。
| A.D→C→B→A→E | B.D→A→B→C→E |
| C.D→B→A→C→E | D.D→C→A→B→E |
(3)该制备装置的缺点为
方法二:利用反应
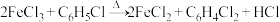 制取无水FeCl2,并通过测定HCl的量来计算FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N2一段时间,分离提纯得到粗产品。
制取无水FeCl2,并通过测定HCl的量来计算FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N2一段时间,分离提纯得到粗产品。
(5)仪器b中干燥剂可以选择_____________。
| A.碱石灰 | B.无水硫酸铜 | C.无水氯化钙 | D.浓硫酸 |
(6)反应结束后恢复至室温,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用最佳试剂是
(7)回收滤液中C6H6Cl的操作方法是_____________。
| A.萃取 | B.分液 | C.过滤 | D.蒸馏 |
(8)反应后将c中溶液稀释至250mL。量取25.00mL所配溶液,用0.400mol·L-1标准NaOH溶液滴定,终点时消耗标准液19.60mL。则氯化铁的转化率为
(9)若反应后通入N2时间不足,则测得氯化铁的转化率
A.偏低 B.偏高 C.不影响
(10)制备无水FeCl2需要用到无水FeCl3,某同学提出利用
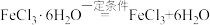 制备无水FeCl3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方
制备无水FeCl3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方
您最近一年使用:0次
6 . 肼在水溶液中为二元弱碱,在水中的电离方式与氨相似。常温下,向0.1mol·L-1肼溶液中,滴加稀盐酸调节pH。溶液中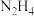 、
、 、
、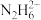 占含氮物种的物质的量分数为
占含氮物种的物质的量分数为 (如
(如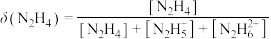 ),
), 随溶液pH变化的曲线如下图所示:
随溶液pH变化的曲线如下图所示:
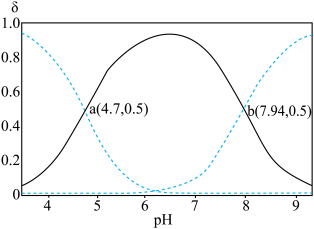
(1)常温下中性溶液中,各含氮物种的浓度大小关系为______________。
(2)室温时,反应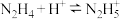 平衡常数K的数值为_____________。
平衡常数K的数值为_____________。
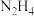 、
、 、
、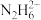 占含氮物种的物质的量分数为
占含氮物种的物质的量分数为 (如
(如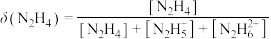 ),
), 随溶液pH变化的曲线如下图所示:
随溶液pH变化的曲线如下图所示:
(1)常温下中性溶液中,各含氮物种的浓度大小关系为______________。
A.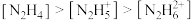 | B.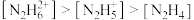 |
C.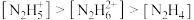 | D.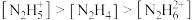 |
(2)室温时,反应
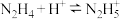 平衡常数K的数值为_____________。
平衡常数K的数值为_____________。A.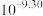 | B.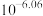 | C. | D.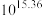 |
您最近一年使用:0次
7 . 肼能除去锅炉用水中的溶解氧(即溶解的氧气),以减缓锅炉锈蚀。已知某锅炉用水中的溶解氧的浓度为8.0mg·L-1,若反应过程中肼全部转化为氮气,则每处理1m3该锅炉用水,需要消耗肼的质量为多少?______ (写出计算过程)。
您最近一年使用:0次
8 . 一定条件下,Co2+与肼在碱性环境中反应制得高纯度纳米钴。请完成相应的离子方程式_______ :
N2H4+Co2++ Co+N2↑+
Co+N2↑+
检验产品的颗粒尺寸是否为纳米级的简易方案是:_____________ 。
N2H4+Co2++
 Co+N2↑+
Co+N2↑+ 检验产品的颗粒尺寸是否为纳米级的简易方案是:
您最近一年使用:0次
解题方法
9 . 在催化剂作用下,肼蒸气受热可分解生成N2和一种能使湿润红色石蕊试纸变蓝的气体。写出该反应的化学方程式:_____________ 。
您最近一年使用:0次
10 . N2H4的沸点(113.5℃)比NH3的沸点(-33.4℃)高,原因是_____________ 。
您最近一年使用:0次



