1 . 氮及其化合物在工农业生产、生活中有着重要作用。
1.下列元素中电负性最大的是____。
2.NH3和PH3都具有四面体结构,NH3比PH3的分解温度高的原因是____。
3.配合物Ni(CO)4也具有四面体结构,常温下Ni(CO)4为液态,易溶于CCl4、苯等有机溶剂。写出基态Ni的电子排布式____ ;Ni(CO)4属于____ 晶体。
4.Zn(NH3)42+离子也具有四面体结构,Zn2+可提供4个能量最低的空轨道与NH3参与形成配位键,这4个空轨道是____。
氨在某催化剂作用下只发生如下反应:
主反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H =-905kJ/mol
4NO(g)+6H2O(g) △H =-905kJ/mol
副反应:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H =-1268kJ/mol
2N2(g)+6H2O(g) △H =-1268kJ/mol
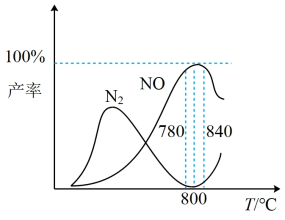
有关物质产率与温度的关系如图。_________ 。
6.工业上采用物料比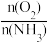 在1.7~2.0,主要目的是:
在1.7~2.0,主要目的是:______________ 。
7.下列说法正确的是______________ 。
A. 工业上进行氨催化氧化生成NO时,温度应控制在780~840℃之间
B. 在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
C. 选择合适的催化剂,可以大幅度提高NO在最终产物中的比率
8.一定温度下,在3.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应,CH4(g)+2NO2(g) CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
表中数据计算0~4min内υ(NO2)=_________ 。
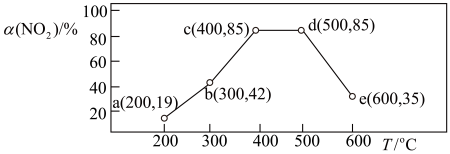
9.在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率 [α(NO2)/%] 如下图;c点___ (填“是”或“不是”)反应达平衡的点。d点之后,转化率随温度升高而降低的原因是___ 。
1.下列元素中电负性最大的是____。
| A.N | B.P | C.Si | D.C |
| A.NH3分子间有氢键 | B.NH3分子极性强 |
| C.N-H键键能大于P-H键 | D.氨极易液化 |
4.Zn(NH3)42+离子也具有四面体结构,Zn2+可提供4个能量最低的空轨道与NH3参与形成配位键,这4个空轨道是____。
| A.3p | B.3d | C.4s | D.4p |
氨在某催化剂作用下只发生如下反应:
主反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H =-905kJ/mol
4NO(g)+6H2O(g) △H =-905kJ/mol副反应:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H =-1268kJ/mol
2N2(g)+6H2O(g) △H =-1268kJ/mol有关物质产率与温度的关系如图。
6.工业上采用物料比
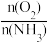 在1.7~2.0,主要目的是:
在1.7~2.0,主要目的是:7.下列说法正确的是
A. 工业上进行氨催化氧化生成NO时,温度应控制在780~840℃之间
B. 在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
C. 选择合适的催化剂,可以大幅度提高NO在最终产物中的比率
8.一定温度下,在3.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应,CH4(g)+2NO2(g)
 CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:| 时间(t/min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 总压强(p/100kPa) | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
9.在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率 [α(NO2)/%] 如下图;c点
您最近一年使用:0次
解题方法
2 . 1.丁苯酞(NBP)是我国拥有完全自主知识产权的化学药物,临床上用于治疗缺血性脑卒中等疾病。ZJM-289是一种NBP开环体(HPBA)衍生物,其合成路线如下:

已知: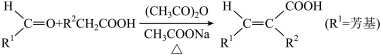
1.A的化学名称为_________ ,NBP中官能团的化学式为:____________ 。
2.关于化合物B叙述正确的是_______。
3.D有多种同分异构体, 其中能同时满足下列条件的芳香族化合物的结构简式为______ 、________
①可发生银镜反应,也能与FeCl3溶液发生显色反应
②核磁共振氢谱有四组峰,峰面积比为1:2:2:3
4.E→F中步骤1的化学方程式为________ 。
5.G→H的反应类型为____________ 。若以NaNO3代替AgNO3,则该反应难以进行,AgNO3对该反应的促进作用主要是因为______________ 。
6.HPBA的结构简式为__________ 。
7.W是合成某种抗疟疾药物的中间体类似物。参照题干中流程图的表达方式,写出设计由2,4-二氯甲苯(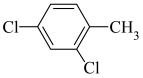 )和对三氟甲基苯乙酸 (
)和对三氟甲基苯乙酸 (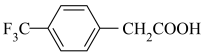 )制备W的合成路线
)制备W的合成路线__________ (无机试剂和四个碳以下的有机试剂任选)。
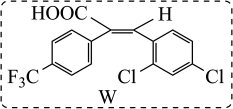

已知:
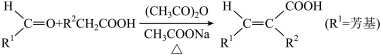
1.A的化学名称为
2.关于化合物B叙述正确的是_______。
| A.二氯代物有3种 |
| B.所有的原子可能共平面 |
| C.能发生加成、取代、消去反应 |
| D.1molB最多可与含2molNaOH的溶液反应 |
①可发生银镜反应,也能与FeCl3溶液发生显色反应
②核磁共振氢谱有四组峰,峰面积比为1:2:2:3
4.E→F中步骤1的化学方程式为
5.G→H的反应类型为
6.HPBA的结构简式为
7.W是合成某种抗疟疾药物的中间体类似物。参照题干中流程图的表达方式,写出设计由2,4-二氯甲苯(
 )和对三氟甲基苯乙酸 (
)和对三氟甲基苯乙酸 ( )制备W的合成路线
)制备W的合成路线
您最近一年使用:0次
3 . 氧化二氯是一种广谱、高效的灭菌剂,可由氯气与氧化汞反应制得。
1.实验室以MnO2为氧化剂制取Cl2的化学方程式为___________ 。
2.由该原理生成Cl2后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是__________ 。
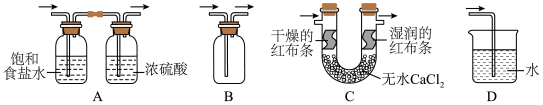
3.某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中,不合理的是__________ (已知:饱和NaClO溶液的pH约为11)
A. 该消毒液的pH约为12:ClO-+ H2O HClO + OH-
HClO + OH-
B. 该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2: 2H+ + Cl-+ClO-=Cl2↑+ H2O
C. 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH + ClO-=HClO + CH3COO-
已知:HgO+2Cl2 HgCl2+Cl2O,合适反应温度为18~25℃;副反应:2HgO+2Cl2
HgCl2+Cl2O,合适反应温度为18~25℃;副反应:2HgO+2Cl2 2HgCl2 + O2;常压下, Cl2沸点-34.0℃,熔点-101.0℃;Cl2O沸点2.0℃,熔点-120.6℃;Cl2O+H2O
2HgCl2 + O2;常压下, Cl2沸点-34.0℃,熔点-101.0℃;Cl2O沸点2.0℃,熔点-120.6℃;Cl2O+H2O 2HClO,Cl2O在CCl4中的溶解度远大于其在水中的溶解度。
2HClO,Cl2O在CCl4中的溶解度远大于其在水中的溶解度。__________ 。
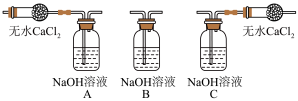
5.有关反应柱B,无需进行的操作是__________。
6.氧化二氯制备出之后,要冷却为固态才便于操作和贮存,则C中保温瓶内盛有冷却液应是__________。
产品分析:取一定量Cl2O浓溶液的稀释液,加入适量CCl4、过量KI溶液及一定量的稀H2SO4,充分反应。用标准Na2S2O3溶液滴定(滴定Ⅰ):I2+2S2O =S4O
=S4O +2I-;再以酚酞为指示剂,用标准NaOH溶液滴定(滴定Ⅱ)。已知产生I2的反应(不考虑Cl2与水反应):
+2I-;再以酚酞为指示剂,用标准NaOH溶液滴定(滴定Ⅱ)。已知产生I2的反应(不考虑Cl2与水反应):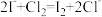 ,
,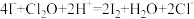 ,
, 。实验数据如下表:
。实验数据如下表:
7.用标准Na2S2O3溶液滴定时,无需另加指示剂。判断滴定Ⅰ到达终点的实验现象是_______ 。
8.高纯度Cl2O浓溶液中,要求n(Cl2O)/n( Cl2)≥99(Cl2O和HClO均以Cl2O计)。由已知数据可知:n(Cl2O)=___________ , n(Cl2O)/n( Cl2) =__________ , 所制备的Cl2O浓溶液______ (选填“是”或“否”)符合要求。
1.实验室以MnO2为氧化剂制取Cl2的化学方程式为
2.由该原理生成Cl2后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是

3.某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中,不合理的是
A. 该消毒液的pH约为12:ClO-+ H2O
 HClO + OH-
HClO + OH-B. 该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2: 2H+ + Cl-+ClO-=Cl2↑+ H2O
C. 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH + ClO-=HClO + CH3COO-
已知:HgO+2Cl2
 HgCl2+Cl2O,合适反应温度为18~25℃;副反应:2HgO+2Cl2
HgCl2+Cl2O,合适反应温度为18~25℃;副反应:2HgO+2Cl2 2HgCl2 + O2;常压下, Cl2沸点-34.0℃,熔点-101.0℃;Cl2O沸点2.0℃,熔点-120.6℃;Cl2O+H2O
2HgCl2 + O2;常压下, Cl2沸点-34.0℃,熔点-101.0℃;Cl2O沸点2.0℃,熔点-120.6℃;Cl2O+H2O 2HClO,Cl2O在CCl4中的溶解度远大于其在水中的溶解度。
2HClO,Cl2O在CCl4中的溶解度远大于其在水中的溶解度。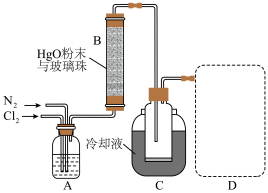

5.有关反应柱B,无需进行的操作是__________。
| A.将HgO粉末热处理除水分、增加表面积后填入反应柱 |
| B.调控进入反应柱的混合气中Cl2和N2的比例 |
| C.调控混合气从下口进入反应柱的流速 |
| D.将加热带缠绕于反应柱并加热 |
| A.干冰 | B.冰水 | C.液态空气 | D.液氨 |
 =S4O
=S4O +2I-;再以酚酞为指示剂,用标准NaOH溶液滴定(滴定Ⅱ)。已知产生I2的反应(不考虑Cl2与水反应):
+2I-;再以酚酞为指示剂,用标准NaOH溶液滴定(滴定Ⅱ)。已知产生I2的反应(不考虑Cl2与水反应):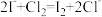 ,
,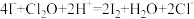 ,
, 。实验数据如下表:
。实验数据如下表:| 加入量n(H2SO4)/mol | 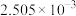 |
| 滴定Ⅰ测出量n(I2)/mol | 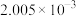 |
| 滴定Ⅱ测出量n(H2SO4)/mol | 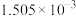 |
8.高纯度Cl2O浓溶液中,要求n(Cl2O)/n( Cl2)≥99(Cl2O和HClO均以Cl2O计)。由已知数据可知:n(Cl2O)=
您最近一年使用:0次
4 . 纳米硫化亚铁是一种很有潜在价值的新材料,值得深入研究。
1.关于铁元素的认识正确的是_________。
2.可用于检验FeSO4溶液是否变质的是_________。
3.高铁酸钠( Na2FeO4) 可用作净水剂,其原因是_________。
4.Fe、Co、Ni三种元素二价氧化物的晶胞类型相同,其熔点最高的是____ 。
A. FeO B. CoO C. NiO
纳米FeS可去除水中微量六价铬[Cr(Ⅵ)]。在pH=4~7的水溶液中,纳米FeS颗粒表面带正电荷,Cr(Ⅵ)主要以CrO 等形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。已知: Ksp(FeS)=6.5×10-18,Ksp[Fe(OH)2]=5.0×10-17;H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。
等形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。已知: Ksp(FeS)=6.5×10-18,Ksp[Fe(OH)2]=5.0×10-17;H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。
5.在弱酸性溶液中,反应FeS+H+ Fe2++HS-的平衡常数K的数值为
Fe2++HS-的平衡常数K的数值为____ 。
在pH=4~7溶液中,pH越大,FeS去除水中Cr(Ⅵ)的速率越慢,原因是____________ 。
6.FeS2的一种晶体与NaCl晶体的结构相似,该FeS2晶体的一个晶胞中S 的数目为_________。
的数目为_________。
7.在FeS2晶体中,每个S原子与三个Fe2+紧邻,且Fe—S间距相等,如图给出了FeS2晶胞中的Fe2+和位于晶胞体心的S (S
(S 中的S—S键位于晶胞体对角线上,晶胞中的其他S
中的S—S键位于晶胞体对角线上,晶胞中的其他S 已省略)。图1中用“—”将其中一个S原子与紧邻的Fe2+连接起来
已省略)。图1中用“—”将其中一个S原子与紧邻的Fe2+连接起来_________ 。

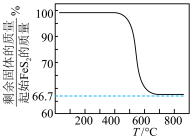
8.FeS2、FeS在空气中易被氧化。将FeS2在空气中氧化,测得氧化过程中剩余固体的质量与起始FeS2的质量的比值随温度变化的曲线如图所示。800℃时,FeS2氧化成含有两种元素的固体产物_______ 。
1.关于铁元素的认识正确的是_________。
| A.能存在于人体的血红蛋白中 | B.是地壳中含量最多的金属元素 |
| C.单质是人类最早使用的金属 | D.铁的氧化物都具有致密的结构 |
| A.稀盐酸 | B.酚酞试液 | C.KSCN溶液 | D.苯酚 |
| A.能吸附水中杂质,氧化产物能消毒杀菌 |
| B.可消毒杀菌,氧化产物能吸附水中杂质 |
| C.能吸附水中杂质,还原产物能消毒杀菌 |
| D.可消毒杀菌,还原产物能吸附水中杂质 |
A. FeO B. CoO C. NiO
纳米FeS可去除水中微量六价铬[Cr(Ⅵ)]。在pH=4~7的水溶液中,纳米FeS颗粒表面带正电荷,Cr(Ⅵ)主要以CrO
 等形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。已知: Ksp(FeS)=6.5×10-18,Ksp[Fe(OH)2]=5.0×10-17;H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。
等形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。已知: Ksp(FeS)=6.5×10-18,Ksp[Fe(OH)2]=5.0×10-17;H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。5.在弱酸性溶液中,反应FeS+H+
 Fe2++HS-的平衡常数K的数值为
Fe2++HS-的平衡常数K的数值为在pH=4~7溶液中,pH越大,FeS去除水中Cr(Ⅵ)的速率越慢,原因是
6.FeS2的一种晶体与NaCl晶体的结构相似,该FeS2晶体的一个晶胞中S
 的数目为_________。
的数目为_________。| A.2 | B.4 | C.6 | D.8 |
 (S
(S 中的S—S键位于晶胞体对角线上,晶胞中的其他S
中的S—S键位于晶胞体对角线上,晶胞中的其他S 已省略)。图1中用“—”将其中一个S原子与紧邻的Fe2+连接起来
已省略)。图1中用“—”将其中一个S原子与紧邻的Fe2+连接起来
8.FeS2、FeS在空气中易被氧化。将FeS2在空气中氧化,测得氧化过程中剩余固体的质量与起始FeS2的质量的比值随温度变化的曲线如图所示。800℃时,FeS2氧化成含有两种元素的固体产物

您最近一年使用:0次
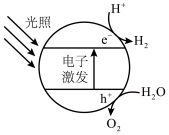
5 . 利用太阳能光解水时,将半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物。下图为该催化剂在水中发生光催化反应的原理示意图。_________ 。
A. 离子键 B. 极性共价键 C. 非极性共价键
2.硫的非金属性比氧弱,但从以下的事实不能做出判断的是________。
3.在相同条件下,同时存在如下两个过程:
ⅰ.2H(g) + O(g) = H2O(g)
ⅱ.H2(g) + O2(g) = H2O(g)
O2(g) = H2O(g)
则放出热量______ 。
A. ⅰ>ⅱ B. ⅰ=ⅱ C. ⅰ<ⅱ
4.光解水能量转化形式是__________ 。若将该催化剂置于Na2SO3溶液中,产物之一为SO ,另一产物为
,另一产物为__________ 。
储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
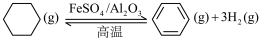
一定条件下,下图所示装置可实现有机物的电化学储氢(忽略其它有机物)。

5.导线中电子转移方向为____ 。(用A、D表示),生成目标产物的电极反应为____ 。
6.由数据分析可知,D电极上除了环己烷,还有另一产物,该产物属于_______ 。
7.阳极产物的电子式为__________ ,转移的电子的物质的量是_______ 。
8.含碳的微粒种类繁多,结构各异。其中CO 的立体构型为
的立体构型为_______ 。
A. 离子键 B. 极性共价键 C. 非极性共价键
2.硫的非金属性比氧弱,但从以下的事实不能做出判断的是________。
| A.硫化氢不如水稳定 |
| B.硫跟氢气反应比氧气跟氢气反应更困难 |
| C.硫化氢的水溶液露置在空气中变浑浊 |
| D.硫是固体,氧气在常温下是气体 |
ⅰ.2H(g) + O(g) = H2O(g)
ⅱ.H2(g) +
 O2(g) = H2O(g)
O2(g) = H2O(g)则放出热量
A. ⅰ>ⅱ B. ⅰ=ⅱ C. ⅰ<ⅱ
4.光解水能量转化形式是
 ,另一产物为
,另一产物为储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
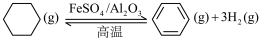
一定条件下,下图所示装置可实现有机物的电化学储氢(忽略其它有机物)。

5.导线中电子转移方向为
6.由数据分析可知,D电极上除了环己烷,还有另一产物,该产物属于
| A.氧化产物 | B.还原产物 | C.极性分子 | D.非极性分子 |
8.含碳的微粒种类繁多,结构各异。其中CO
 的立体构型为
的立体构型为| A.平面正三角形 | B.正四面体型 | C.三角锥型 | D.直线型 |
您最近一年使用:0次
名校
6 . 在密闭容器中,反应2X(g)+Y(g) 3Z(g)达到平衡后,若将容器体积缩小一半,对反应产生的影响是
3Z(g)达到平衡后,若将容器体积缩小一半,对反应产生的影响是
 3Z(g)达到平衡后,若将容器体积缩小一半,对反应产生的影响是
3Z(g)达到平衡后,若将容器体积缩小一半,对反应产生的影响是| A.v(正)减小,v (逆)增大 | B.v (正)增大,v (逆)减小 |
| C.v (正),v (逆)都减小 | D.v (正),v (逆)都增大 |
您最近一年使用:0次
2023-10-31更新
|
117次组卷
|
10卷引用:上海市长宁、金山、青浦区2017届高三4月教学质量检测(二模)化学试题
上海市长宁、金山、青浦区2017届高三4月教学质量检测(二模)化学试题(已下线)上海市宝山区2017年高考化学二模试卷2017届上海市宝山区高三下学期期中教学质量监测化学试卷上海市金山中学2018届高三上学期期中考试化学试题上海市文绮中学2019届高三期中考试卷化学试题上海市扬子中学2017-2018学年高三上学期期中考试化学试题课前-2.2.3 影响化学平衡的因素-课前、课中、课后(人教版2019选择性必修1)海南省三亚华侨学校(南新校区)2021-2022学年高二上学期期中考试化学试题陕西西安市第八十三中学2023-2024学年高二上学期10月月考化学试题江西省赣州市全南中学2023-2024学年高二上学期11月期中考试化学试题
7 . CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g),回答下列问题:
CS2(g)+2H2S(g),回答下列问题:
(1)CH4的立体构型为_______ ,CS2分子的电子式为_______ 。
(2)某温度下若S8完全分解成气态S2。在恒温恒容密闭容器中S2与CH4物质的量比为2∶1时开始反应。
①当CS2的体积分数为10%时,CH4的转化率为_______ 。
②当以下数值不变时,能说明该反应达到平衡的是_______ (填序号)。
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
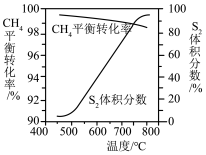
(3)一定条件下,CH4与S2反应中CH4的平衡转化率、S8分解产生S2的体积分数随温度的变化曲线如图所示。据图分析,生成CS2的反应为_______ (填“放热”或“吸热”)反应。工业上通常采用在600~650℃的条件下进行此反应,不采用低于600℃可能的原因是:_______ 。
(4)用燃煤废气(含N2、O2、SO2、CO2、H2O等)使尾气中的H2S转化为单质硫S,可实现废物利用,保护环境,写出其中一个反应的化学方程式_______ 。燃煤废气中常含有的NOx也能使H2S转化为单质硫S,完成其化学方程式,并标出电子转移的方向和数目(用含X的代数式表示)_______ 。
_______H2S+_______NOx=_______S+_______+_______N2
 CS2(g)+2H2S(g),回答下列问题:
CS2(g)+2H2S(g),回答下列问题:(1)CH4的立体构型为
(2)某温度下若S8完全分解成气态S2。在恒温恒容密闭容器中S2与CH4物质的量比为2∶1时开始反应。
①当CS2的体积分数为10%时,CH4的转化率为
②当以下数值不变时,能说明该反应达到平衡的是
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
(3)一定条件下,CH4与S2反应中CH4的平衡转化率、S8分解产生S2的体积分数随温度的变化曲线如图所示。据图分析,生成CS2的反应为

(4)用燃煤废气(含N2、O2、SO2、CO2、H2O等)使尾气中的H2S转化为单质硫S,可实现废物利用,保护环境,写出其中一个反应的化学方程式
_______H2S+_______NOx=_______S+_______+_______N2
您最近一年使用:0次
解题方法
8 . 溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末,常用作有机反应的催化剂。实验室制备CuBr的实验步骤和装置如图。

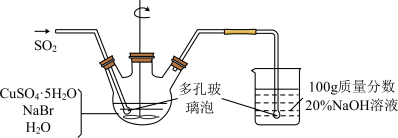
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去蒸馏水中的_______ (写化学式); 三颈烧瓶中反应生成CuBr的离子方程式为_______ ;控制反应在60℃进行,实验中可采取的措施是 _______ ;说明反应已完成的现象是 _______ 。
(2)步骤②抽滤需要避光的原因是_______ ,步骤③依次用溶有少量SO2的水、溶有少量SO2的乙醇、极易挥发的乙醚洗涤,洗涤剂需“溶有SO2”的原因是_______ ;最后用乙醚的目的可能是_______ 。
(3)将产品在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,得到产品21.6g。本实验产品的产率是_______ (保留小数点后1位)。
(4)欲利用上述装置烧杯中的吸收液(经检测主要含有Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。完善下列步骤:①在烧杯中继续通入SO2至恰好反应完全;②向烧杯中加入_______ g 20% NaOH;③加入少量维生素C溶液作抗氧化剂;④通过蒸发浓缩、_______ 、过滤、用乙醇洗涤2~3次;⑤置于真空干燥箱中干燥。


(1)实验所用蒸馏水需经煮沸,煮沸目的是除去蒸馏水中的
(2)步骤②抽滤需要避光的原因是
(3)将产品在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,得到产品21.6g。本实验产品的产率是
(4)欲利用上述装置烧杯中的吸收液(经检测主要含有Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。完善下列步骤:①在烧杯中继续通入SO2至恰好反应完全;②向烧杯中加入
您最近一年使用:0次
2023-04-14更新
|
539次组卷
|
5卷引用:上海市长宁区2022-2023学年高三下学期二模测试化学试题
上海市长宁区2022-2023学年高三下学期二模测试化学试题(已下线)化学-2023年高考押题预测卷01(辽宁卷)(含考试版、全解全析、参考答案、答题卡)四川省绵阳市2024届高三上学期一诊模拟考试理科综合化学试题(已下线)专题22 实验探究题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
解题方法
9 . 1962年首个稀有气体化合物XePtF6问世,目前已知的稀有气体化合物中,含氙(54Xe)的最多,氪(36Kr)次之,氩(18Ar)化合物极少。[BrOF2][AsF6]•xKrF2是[BrOF2]+、[AsF6]-与KrF2分子形成的加合物,回答下列问题:
(1)As元素原子序数为33,在周期表中的位置是_______ 。As原子的价电子排布式为_______ 。与磷酸相比,最高价氧化物的水化物酸性强弱的顺序是:_______ 。
(2)Ar、Kr、Xe原子半径大小顺序为_______ 。Ar、Kr、Xe原子的活泼性依序增强,原因是________ 。
(3)晶体熔点:KrF2_______ XeF2(填“>”“<”或“=”),判断依据是______________ 。
(4)试猜想:[BrOF2][AsF6]•xKrF2晶体中的化学键类型有_______ 。
(1)As元素原子序数为33,在周期表中的位置是
(2)Ar、Kr、Xe原子半径大小顺序为
(3)晶体熔点:KrF2
(4)试猜想:[BrOF2][AsF6]•xKrF2晶体中的化学键类型有
您最近一年使用:0次
解题方法
10 . 下列离子方程式正确的是
A.足量的CO2通入饱和碳酸钠溶液中:CO2+CO +H2O=2HCO +H2O=2HCO |
B.酸性条件下KIO3溶液与KI溶液反应生成I2:5I-+IO +3H2O=3I2+6OH- +3H2O=3I2+6OH- |
C.向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO 恰好完全反应:2Ba2++4OH-+Al3++2SO 恰好完全反应:2Ba2++4OH-+Al3++2SO =BaSO4↓+AlO =BaSO4↓+AlO +2H2O +2H2O |
D.NH4HSO3溶液中逐滴加入足量的Ba(OH)2溶液:NH +HSO +HSO +Ba2++2OH-=BaSO3↓+NH3·H2O+H2O +Ba2++2OH-=BaSO3↓+NH3·H2O+H2O |
您最近一年使用:0次



