一定条件下,Co2+与肼在碱性环境中反应制得高纯度纳米钴。请完成相应的离子方程式_______ :
N2H4+Co2++ Co+N2↑+
Co+N2↑+
检验产品的颗粒尺寸是否为纳米级的简易方案是:_____________ 。
N2H4+Co2++
 Co+N2↑+
Co+N2↑+ 检验产品的颗粒尺寸是否为纳米级的简易方案是:
更新时间:2024-04-18 21:47:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有以下物质:①CaO固体 ②NaOH溶液 ③液氨 ④NaHSO4固体 ⑤铁 ⑥ 胶体 ⑦
胶体 ⑦ 固体 ⑧
固体 ⑧ 固体 ⑨
固体 ⑨ ⑩硫酸溶液
⑩硫酸溶液
(1)以上物质中属于非电解质的是_______ (填序号,下同),上述物质在所处的状态下,可以导电的有_______ 。
(2)写出④在水溶液中电离方程式_______ 。
(3)在足量④的水溶液中加入少量⑦的水溶液,发生反应的离子方程式为_______ 。
(4)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体。制取
胶体。制取 胶体的离子方程式为:
胶体的离子方程式为:_______ 。
(5)下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔效应
区分胶体和溶液的方法是_______ (填字母,下同);“卤水点豆腐”,利用的性质是_______ (填字母,下同);工厂采用高压静电除尘,利用的胶体性质是_______ 。
 胶体 ⑦
胶体 ⑦ 固体 ⑧
固体 ⑧ 固体 ⑨
固体 ⑨ ⑩硫酸溶液
⑩硫酸溶液(1)以上物质中属于非电解质的是
(2)写出④在水溶液中电离方程式
(3)在足量④的水溶液中加入少量⑦的水溶液,发生反应的离子方程式为
(4)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
 胶体。制取
胶体。制取 胶体的离子方程式为:
胶体的离子方程式为:(5)下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔效应
区分胶体和溶液的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列10种物质:
① ②
② 溶液 ③液态
溶液 ③液态 ④
④ ⑤
⑤ ⑥
⑥ 固体 ⑦纯醋酸 ⑧氢氧化铁胶体 ⑨乙醇 ⑩
固体 ⑦纯醋酸 ⑧氢氧化铁胶体 ⑨乙醇 ⑩ 溶液
溶液

(1)上述物质中能导电的有___________ (填序号,下同),属于电解质的有___________ 。
(2)向⑧中逐滴加入③的水溶液,该过程中可观察到的现象为___________ 。
(3)向一定浓度的②中滴加⑩,溶液的电导率随滴入溶液体积变化的曲线如图所示。则ab段发生反应的离子方程式为___________ ,c点溶液中大量存在的离子是___________ 。
(4)⑤与⑥在高温下反应生成一种高效绿色消毒剂高铁酸钠,反应方程式为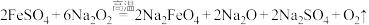 ,若每生成
,若每生成 ,理论上被还原的
,理论上被还原的 的物质的量为
的物质的量为___________ mol。
①
 ②
② 溶液 ③液态
溶液 ③液态 ④
④ ⑤
⑤ ⑥
⑥ 固体 ⑦纯醋酸 ⑧氢氧化铁胶体 ⑨乙醇 ⑩
固体 ⑦纯醋酸 ⑧氢氧化铁胶体 ⑨乙醇 ⑩ 溶液
溶液
(1)上述物质中能导电的有
(2)向⑧中逐滴加入③的水溶液,该过程中可观察到的现象为
(3)向一定浓度的②中滴加⑩,溶液的电导率随滴入溶液体积变化的曲线如图所示。则ab段发生反应的离子方程式为
(4)⑤与⑥在高温下反应生成一种高效绿色消毒剂高铁酸钠,反应方程式为
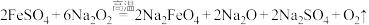 ,若每生成
,若每生成 ,理论上被还原的
,理论上被还原的 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列八种物质:①盐酸;②小苏打;③FeSO4•7H2O;④二氧化碳;⑤蔗糖;⑥氢氧化铁胶体;⑦氨水;⑧NaHSO4固体。
(1)上述八种物质中,属于电解质的是_____ (填序号,下同);属于非电解质的是_____ 。
(2)向⑥中滴加①产生的现象为______ 。
(3)将少量②的溶液与澄清石灰水混合,发生反应的离子方程式为_____ 。
(4)FeSO4•7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式表示铁粉的作用_____ 。
(1)上述八种物质中,属于电解质的是
(2)向⑥中滴加①产生的现象为
(3)将少量②的溶液与澄清石灰水混合,发生反应的离子方程式为
(4)FeSO4•7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式表示铁粉的作用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,Z原子序数大于X,其中Z的简单离子半径在同周期中最小,X单质极易与常见无色无味液态物质发生置换反应且做氧化剂,在短周期中Y的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1)Y在周期表中的位置是_______ ,写出YM的电子式:_______ 。
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):_______ 。
(3)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是_______ 。
a.Ga位于元素周期表第四周期ⅣA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d.酸性:
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为_______ 。
(4) 是有机合成的重要还原剂,其合成路线如图所示。
是有机合成的重要还原剂,其合成路线如图所示。
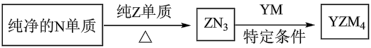
利用 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。
①其反应的化学方程式为_______ 。
②取样品a g,若实验测得氢气的体积为V mL(标准状态),则 样品纯度为
样品纯度为_______ (用代数式表示)。
(1)Y在周期表中的位置是
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):
(3)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是
a.Ga位于元素周期表第四周期ⅣA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d.酸性:

②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出
 气体,同时生成
气体,同时生成 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为(4)
 是有机合成的重要还原剂,其合成路线如图所示。
是有机合成的重要还原剂,其合成路线如图所示。
利用
 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。①其反应的化学方程式为
②取样品a g,若实验测得氢气的体积为V mL(标准状态),则
 样品纯度为
样品纯度为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】(1)在Cl2、NO、SO2、NO2、NH3五种气体中,与空气相遇立即变色的是______ ,常用于自来水杀菌、消毒的是________ ,能用向下排空气法收集的是________ ,溶于水后能生成强酸的是_____________ 。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒消毒剂。
①工业上通过下列方法制取ClO2,完成该反应的化学方程式:2KClO3 + SO2 =2C1O2+___
②配平下列化学方程式:KClO3+__ H2C2O4+__ H2SO4=__ ClO2↑+__ K2SO4+ CO2↑+__ H2O
下列有关上述反应的说法正确的是_______ 。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒消毒剂。
①工业上通过下列方法制取ClO2,完成该反应的化学方程式:2KClO3 + SO2 =2C1O2+
②配平下列化学方程式:KClO3+
下列有关上述反应的说法正确的是
| A.H2C2O4在反应中被还原 | B.KClO3是氧化剂 |
| C.ClO2是还原剂 | D.生成1molClO2有2mol电子转移 |
您最近一年使用:0次
【推荐3】(1)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该有害物质。例如:在如图有编号的步骤中,发生氧化反应的是_____________ (填编号,下同),发生还原反应的是_____________ 。(提示:铬元素化合价有+6、+3价)。
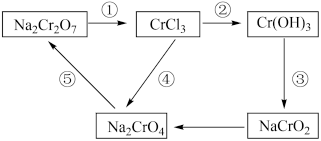
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原N2,其化学方程式为:Al+NaNO3 +NaOH=NaAlO2+N2↑+H2O(未配平)
还原N2,其化学方程式为:Al+NaNO3 +NaOH=NaAlO2+N2↑+H2O(未配平)
请回答下列问题:
①氧化剂是_______________ ;氧化产物是________________ 。
②配平反应的方程式,并用单线桥表示反应中电子转移的方向和数目:
Al+ NaNO3 + NaOH= NaAlO2+ N2↑+ H2O
___
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2+ +Cu2+的拆写结果是:
氧化反应:Cu-2e- =Cu2+ 还原反应: 2Fe3++2e- =2Fe2+。
请据此将反应: Fe+2H+ =Fe2+ +H2↑拆写成两个“半反应式”;
氧化反应为______________________________________________________ ;
还原反应为_____________________________________________________ 。

(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原N2,其化学方程式为:Al+NaNO3 +NaOH=NaAlO2+N2↑+H2O(未配平)
还原N2,其化学方程式为:Al+NaNO3 +NaOH=NaAlO2+N2↑+H2O(未配平)请回答下列问题:
①氧化剂是
②配平反应的方程式,并用单线桥表示反应中电子转移的方向和数目:
Al+ NaNO3 + NaOH= NaAlO2+ N2↑+ H2O
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu=2Fe2+ +Cu2+的拆写结果是:
氧化反应:Cu-2e- =Cu2+ 还原反应: 2Fe3++2e- =2Fe2+。
请据此将反应: Fe+2H+ =Fe2+ +H2↑拆写成两个“半反应式”;
氧化反应为
还原反应为
您最近一年使用:0次



