2022高三·全国·专题练习
真题
解题方法
1 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列判断正确的是
A.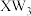 是非极性分子 是非极性分子 |
B.简单氢化物沸点: |
| C.Y与Z形成的化合物是离子化合物 |
| D.X、Y、Z三种元素组成的化合物水溶液呈酸性 |
您最近一年使用:0次
2022-07-04更新
|
8386次组卷
|
19卷引用:上海市虹口区2022-2023学年高三上学期一模统考化学试题
上海市虹口区2022-2023学年高三上学期一模统考化学试题(已下线)专题06 物质结构元素周期律-2022年高考真题模拟题分项汇编2022年海南省高考真题化学试题(已下线)2022年海南省高考真题变式题1-14(已下线)第14讲 元素周期律和元素周期表(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第16讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)易错点14 元素周期表和元素周期律-备战2023年高考化学考试易错题海南省华东师范大学第二附属中学乐东黄流中学2022-2023学年高二上学期期中检测化学试题(已下线)专题07 元素周期律与元素周期表(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题卷09 根据原子结构和物质结构特点叙述型元素推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题07 突破原子结构和元素周期表(律)(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)题型9 元素“位—构-性”关系的综合应用-高考必备50个题型(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)热点题型训练 元素“位—构—性”的综合推断题
2 . 重晶石( )作为原料制备金属钡及其他含钡化合物的方法如下图:
)作为原料制备金属钡及其他含钡化合物的方法如下图:
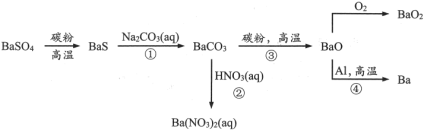
完成下列填空:
(1)Ba在元素周期表中位于第_______ 族,最外层电子的电子云形状是_______ 。图中涉及的第二周期元素原子半径由大到小的顺序是_______ ,可以判断其中两种元素非金属性强弱的反应是_______ (选填流程中的反应编号)。
(2)配平BaS与稀硝酸反应的化学方程式:_______ 。
_______ _______
_______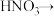 _______
_______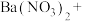 _______
_______ _______
_______ _______
_______
检验溶液中BaS是否完全反应的方法是:取少量反应液,加入_______ (填试剂),有黑色沉淀生成,则BaS未反应完全。
(3)工业上,利用反应①②而不用BaS直接与稀硝酸反应制 的原因是
的原因是_______ 。
(4)元素的金属性:Al_______ Ba(选填“>”或“<”);已知:沸点Al>Ba,反应④在真空容器中可以发生的理由是_______ 。
 )作为原料制备金属钡及其他含钡化合物的方法如下图:
)作为原料制备金属钡及其他含钡化合物的方法如下图:
完成下列填空:
(1)Ba在元素周期表中位于第
(2)配平BaS与稀硝酸反应的化学方程式:
_______
 _______
_______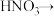 _______
_______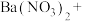 _______
_______ _______
_______ _______
_______
检验溶液中BaS是否完全反应的方法是:取少量反应液,加入
(3)工业上,利用反应①②而不用BaS直接与稀硝酸反应制
 的原因是
的原因是(4)元素的金属性:Al
您最近一年使用:0次
解题方法
3 . 回答下列问题:
(1)将0.050mol SO2(g)和0.030mol O2(g)充入一个2L的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g) 2SO3(g)+Q。写出该反应的逆反应化学平衡常数表达式
2SO3(g)+Q。写出该反应的逆反应化学平衡常数表达式_______ ;经2分钟反应达到平衡,测得n(SO3)=0.040mol,则这个时间段O2的平均反应速率为_______ 。
(2)在容积不变时,下列措施中有利于提高SO2平衡转化率的有_______ (选填编号)。
a. 移出氧气 b. 降低温度 c. 减小压强 d. 再充入0.050mol SO2(g)和0.030mol O2(g)
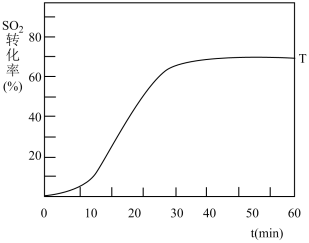
(3)在起始温度T1(673K)时SO2的转化率随反应时间(t)的变化如图。请在图中画出其他条件不变情况下,起始温度为T2(723K)时SO2的转化率随反应时间变化的示意图_______ 。
常温下,向1L pH=10的NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离产生的OH-离子浓度(c)的关系如图所示。
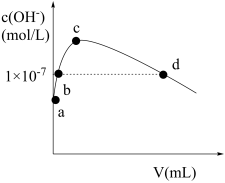
(4)c点溶液中离子浓度由大至小的关系是:_______ 。a点溶液中由水电离产生的c(H+)=_______ 。b点溶液中c(H+)_______ 1×10-7mol/L(填写“等于”、“大于”或“小于”)。
(5)写出c点到d点化学反应方程式_______ 。
(1)将0.050mol SO2(g)和0.030mol O2(g)充入一个2L的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)
 2SO3(g)+Q。写出该反应的逆反应化学平衡常数表达式
2SO3(g)+Q。写出该反应的逆反应化学平衡常数表达式(2)在容积不变时,下列措施中有利于提高SO2平衡转化率的有
a. 移出氧气 b. 降低温度 c. 减小压强 d. 再充入0.050mol SO2(g)和0.030mol O2(g)
(3)在起始温度T1(673K)时SO2的转化率随反应时间(t)的变化如图。请在图中画出其他条件不变情况下,起始温度为T2(723K)时SO2的转化率随反应时间变化的示意图

常温下,向1L pH=10的NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离产生的OH-离子浓度(c)的关系如图所示。

(4)c点溶液中离子浓度由大至小的关系是:
(5)写出c点到d点化学反应方程式
您最近一年使用:0次
解题方法
4 . 以盐湖锂精矿(主要成分:Li2CO3,杂质:CaCO3)和盐湖卤水(含一定浓度LiCl和MgCl2)为原料均能制备碳酸锂(Li2CO3)。
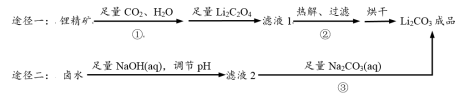
部分溶解度(g/100gH2O)数据见下表:
完成下列填空:
(1)步骤①主要反应的化学方程式为_______ ,反应在常温下进行,温度越高,锂精矿转化率越低的原因可能是_______ 。
(2)步骤②热解、过滤获得的沉淀表面有少量Li2C2O4,不经洗涤也不会影响Li2CO3纯度的原因用化学方程式表示为_______ 。
(3)步骤③的操作是过滤、_______ 洗涤(选填“冷水”或“热水”)、干燥;判断滤液2中Li+是否沉淀完全的方法是_______ 。
(4)Li2CO3(M=74g·mol-1)样品的纯度可用滴定法测定(杂质不参与反应)。反应原理:Li2CO3+2HCl→2LiCl+CO2↑+H2O,用盐酸标准液滴定Li2CO3样品的操作步骤顺序为c、a_______ 。
a.加入0.1~0.2mL甲基红-溴甲粉绿作指示剂;
b.煮沸去除CO2,再冷却到室温;
c.将样品置于锥形瓶中,加水溶解;
d.用盐酸标准液滴定至溶液由绿色变成酒红色;
e.继续滴定至酒红色(滴定突跃区域)即为终点。
(5)用含以下物理量的数学表达式表示Li2CO3的纯度ω=_______ 。
m-Li2CO3样品的质量(g);c-盐酸标准液的浓度(mol·L-1);V1-样品滴定时消耗盐酸的体积(mL);V0-滴定空白溶液(指不加样品进行滴定)时消耗盐酸的体积(mL)。
上述滴定操作中,若缺少步骤b,测定结果将_______ (选填“偏大”或“偏小”)。

部分溶解度(g/100gH2O)数据见下表:
| 温度(℃) | 0 | 20 | 80 |
| LiOH | - | 12.8 | - |
| Li2CO3 | 1.54 | 1.33 | 0.85 |
完成下列填空:
(1)步骤①主要反应的化学方程式为
(2)步骤②热解、过滤获得的沉淀表面有少量Li2C2O4,不经洗涤也不会影响Li2CO3纯度的原因用化学方程式表示为
(3)步骤③的操作是过滤、
(4)Li2CO3(M=74g·mol-1)样品的纯度可用滴定法测定(杂质不参与反应)。反应原理:Li2CO3+2HCl→2LiCl+CO2↑+H2O,用盐酸标准液滴定Li2CO3样品的操作步骤顺序为c、a
a.加入0.1~0.2mL甲基红-溴甲粉绿作指示剂;
b.煮沸去除CO2,再冷却到室温;
c.将样品置于锥形瓶中,加水溶解;
d.用盐酸标准液滴定至溶液由绿色变成酒红色;
e.继续滴定至酒红色(滴定突跃区域)即为终点。
(5)用含以下物理量的数学表达式表示Li2CO3的纯度ω=
m-Li2CO3样品的质量(g);c-盐酸标准液的浓度(mol·L-1);V1-样品滴定时消耗盐酸的体积(mL);V0-滴定空白溶液(指不加样品进行滴定)时消耗盐酸的体积(mL)。
上述滴定操作中,若缺少步骤b,测定结果将
您最近一年使用:0次
解题方法
5 . ZnO是一种难溶于水的白色固体,在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上可由菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Mn等元素)制备。工艺如图所示:

相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
已知:
①“溶浸”后的溶液pH=1,所含金属离子主要有:Zn2+、Fe2+、Cd2+、Mn2+、Ni2+;
②弱酸性溶液中KMnO4氧化Mn2+时,产物中含Mn元素物质只有MnO2;
③氧化性顺序:Ni2+>Cd2+>Zn2+。
回答下列问题:
(1)①“溶浸”过程中,为了提高浸出率,可采取的措施是_______ 。(写一条即可)
②“调pH”是向“溶浸”后的溶液中加入少量_______ (填化学式)调节至弱酸性(pH约为5),“调pH”的目的是_______ 。
(2)“滤渣2”的化学成分为_______ (写化学式);用离子方程式表示“氧化除杂”时KMnO4溶液与Mn2+的反应原理_______ 。
(3)“还原除杂”除去的离子是_______ ;加入的还原剂是_______ 。
(4)“沉锌”时生成碱式碳酸锌[ZnCO3·2Zn(OH)2·2H2O]沉淀,分析测得1kg该沉淀“高温灼烧”后获得ZnO0.670kg。则“高温灼烧”过程中原料的转化率为_______ 。

相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ | Mn2+ | Ni2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 | 8.1 | 6.9 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 | 10.1 | 8.9 |
已知:
①“溶浸”后的溶液pH=1,所含金属离子主要有:Zn2+、Fe2+、Cd2+、Mn2+、Ni2+;
②弱酸性溶液中KMnO4氧化Mn2+时,产物中含Mn元素物质只有MnO2;
③氧化性顺序:Ni2+>Cd2+>Zn2+。
回答下列问题:
(1)①“溶浸”过程中,为了提高浸出率,可采取的措施是
②“调pH”是向“溶浸”后的溶液中加入少量
(2)“滤渣2”的化学成分为
(3)“还原除杂”除去的离子是
(4)“沉锌”时生成碱式碳酸锌[ZnCO3·2Zn(OH)2·2H2O]沉淀,分析测得1kg该沉淀“高温灼烧”后获得ZnO0.670kg。则“高温灼烧”过程中原料的转化率为
您最近一年使用:0次
2022-07-03更新
|
346次组卷
|
2卷引用:上海市崇明区2022届高三等级考 二模化学试题
6 . 二甲醚(CH3OCH3)的合成方法主要有两种:方法一:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)
(1)恒温恒容下进行上述反应,能说明反应已达平衡状态的是_______ 。
a.混合气体密度不变
b.混合气体的平均相对分子质量不变
c.3v(CO2)正=v(H2)逆
d. 不变
不变
反应达到平衡,其他条件不变,向容器中再加入等物质的量的H2(g)和H2O(g),平衡向_______ (选填“正”或“逆”)反应方向移动,理由是_______ 。
(2)方法一是CO2高值化利用的途径之一、已知CO2溶于水的过程可表示为:CO2(g)+H2O(l)⇌H2CO3(aq); ,p(CO2)表示CO2的平衡压强。将CO2(g)通入NaClO(aq)中,当n(CO2)∶n(NaClO)=1恰好反应,离子方程式为
,p(CO2)表示CO2的平衡压强。将CO2(g)通入NaClO(aq)中,当n(CO2)∶n(NaClO)=1恰好反应,离子方程式为_______ ,该反应的平衡常数表达式K=_______ 。向反应后的溶液中加过量NaOH(aq),c( )
)_______ c(ClO-)(选填“>”“<”或“=”)。
方法二:CO(g)+2H2(g)⇌CH3OH(g) ①
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ②
(3)T℃,在2L的密闭容器中充入4molCO和8molH2合成二甲醚,4min达到平衡,平衡时CO的转化率为0.8,且2c(CH3OH)=c(CH3OCH3)。0~4min内,v(CH3OCH3)=_______ 。
(4)300℃和500℃时,反应①的平衡常数分别为K1、K2,且K1>K2,则反应①正反应为_______ 反应(选填“吸热”或“放热”)。
(1)恒温恒容下进行上述反应,能说明反应已达平衡状态的是
a.混合气体密度不变
b.混合气体的平均相对分子质量不变
c.3v(CO2)正=v(H2)逆
d.
 不变
不变反应达到平衡,其他条件不变,向容器中再加入等物质的量的H2(g)和H2O(g),平衡向
(2)方法一是CO2高值化利用的途径之一、已知CO2溶于水的过程可表示为:CO2(g)+H2O(l)⇌H2CO3(aq);
 ,p(CO2)表示CO2的平衡压强。将CO2(g)通入NaClO(aq)中,当n(CO2)∶n(NaClO)=1恰好反应,离子方程式为
,p(CO2)表示CO2的平衡压强。将CO2(g)通入NaClO(aq)中,当n(CO2)∶n(NaClO)=1恰好反应,离子方程式为 )
)方法二:CO(g)+2H2(g)⇌CH3OH(g) ①
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ②
(3)T℃,在2L的密闭容器中充入4molCO和8molH2合成二甲醚,4min达到平衡,平衡时CO的转化率为0.8,且2c(CH3OH)=c(CH3OCH3)。0~4min内,v(CH3OCH3)=
(4)300℃和500℃时,反应①的平衡常数分别为K1、K2,且K1>K2,则反应①正反应为
您最近一年使用:0次
7 . 氮及其化合物在自然界中存在循环,请回答下列问题:
(1)氮元素在周期表中的位置是_______ ,氮原子核外电子共占据_______ 个轨道,最外层有_______ 种不同能量的电子。
(2)氨气分子的空间构型为_______ ,氮的最高价氧化物对应水化物的酸性比磷酸的酸性_______ (填“强”或者“弱”)。
(3)工业合成氨反应的化学平衡常数表达式为_______ 。一定条件下,在容积为2L的密闭容器中模拟该反应,测得10min时氮气为0.195mol,请计算0 ~ 10min的氨气的化学反应速率为_______ 。据图判断,反应进行至20 min时,曲线发生变化的原因是_______ (用文字表达)。

(4)工业上用氨水吸收SO2尾气,若最终得到(NH4)2SO4,则该溶液中c(NH )与c(SO
)与c(SO )之比
)之比_______ 2:1(选填“>”、“<”、“=”),请结合离子方程式解释其原因_______ 。
(1)氮元素在周期表中的位置是
(2)氨气分子的空间构型为
(3)工业合成氨反应的化学平衡常数表达式为

(4)工业上用氨水吸收SO2尾气,若最终得到(NH4)2SO4,则该溶液中c(NH
 )与c(SO
)与c(SO )之比
)之比
您最近一年使用:0次
2022-07-03更新
|
256次组卷
|
2卷引用:上海市奉贤区2022届高三下学期等级考二模化学试题
解题方法
8 . 高温下,活性炭可用来处理NOx废气。某研究小组向体积固定的密闭容器加入一定量的活性炭和NO,发生反应C(s)+ 2NO(g) N2(g)+CO2(g)。T1℃时,测得反应进行到不同时刻各物质的浓度如下表:
N2(g)+CO2(g)。T1℃时,测得反应进行到不同时刻各物质的浓度如下表:
回答下列问题:
(1)碳原子核外有_______ 个未成对的电子,N2分子的电子式是_______ ,氧原子2p亚层的轨道表示式为_______ 。
(2)T1 ℃时,在0~10 min内的平均反应速率v(N2)=_______ mol·L-1·min-1。
(3)该反应的平衡常数表达式为_______ 。第30min 时,仅改变了某一条件,请根据表中数据判断可能改变的条件是_______ (填字母编号)。
a. 加入合适的催化剂 b. 适当缩小容器的体积
c. 再通入一定量的NO d. 再加入一定量的活性炭
(4)若第30 min时,将温度升高至T2℃,重新达新平衡时K为2.25,则正反应为_______ 反应(填“放热”或“吸热”),NO的平衡转化率_______ (填“升高”或“降低”)。
 N2(g)+CO2(g)。T1℃时,测得反应进行到不同时刻各物质的浓度如下表:
N2(g)+CO2(g)。T1℃时,测得反应进行到不同时刻各物质的浓度如下表:| 时间(min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 2.0 | 1.16 | 0.40 | 0.40 | 0.6 | 0.6 |
| N2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 | 1.2 |
| CO2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 | 1.2 |
回答下列问题:
(1)碳原子核外有
(2)T1 ℃时,在0~10 min内的平均反应速率v(N2)=
(3)该反应的平衡常数表达式为
a. 加入合适的催化剂 b. 适当缩小容器的体积
c. 再通入一定量的NO d. 再加入一定量的活性炭
(4)若第30 min时,将温度升高至T2℃,重新达新平衡时K为2.25,则正反应为
您最近一年使用:0次
9 . 冰壶比赛称为“冰上的国际象棋”,制作冰壶用的标准砥石的化学成分为石英碱长正长岩,常见的组分有钾长石K[AlSi3O8]和钠长石Na[AlSi3O8]等。完成下列填空:
(1)上述所涉及的元素中,具有相同电子数的简单离子半径由大到小的顺序是_______ ,原子核外有两个未成对电子的元素有_______ 。
(2)用一个化学方程式比较钠和铝的金属性的强弱_______ ,并用原子结构知识的观点解释原因_______ 。
(3)我国科学家发展了一种在200℃熔盐体系中,采用金属Al还原二氧化硅或硅酸盐、钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能,配平下列方程式_______ 。
______Al+_______K[AlSi3O8]+_______AlCl3→_______Si+_______AlOCl+_______KAlO2;
上述反应中若产生14g硅,转移的电子数为_______ 。
(4)KAlO2溶液中,n(K+)_______ n(AlO )(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
)(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因_______ 。
(1)上述所涉及的元素中,具有相同电子数的简单离子半径由大到小的顺序是
(2)用一个化学方程式比较钠和铝的金属性的强弱
(3)我国科学家发展了一种在200℃熔盐体系中,采用金属Al还原二氧化硅或硅酸盐、钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能,配平下列方程式
______Al+_______K[AlSi3O8]+_______AlCl3→_______Si+_______AlOCl+_______KAlO2;
上述反应中若产生14g硅,转移的电子数为
(4)KAlO2溶液中,n(K+)
 )(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
)(选填“>”或“<”),加入KHCO3溶液后,出现白色沉淀,请解释原因
您最近一年使用:0次
10 . 五氧化二氮(N2O5)是一种绿色硝化剂,在军用炸药、火箭推进剂、医药等工业中得到广泛应用。常温下N2O5为白色固体,可溶于二氯甲烷等氯代烃溶剂,微溶于水且与水反应生成硝酸,高于室温时不稳定。回答下列问题:
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体N2O5。该反应的氧化产物为空气中的主要成分之一,写出反应的化学方程式:_______ 。
(2)某化学兴趣小组设计用臭氧(O3)氧化法制备N2O5,反应原理为 N2O4+O3→N2O5+O2。实验装置如下图:
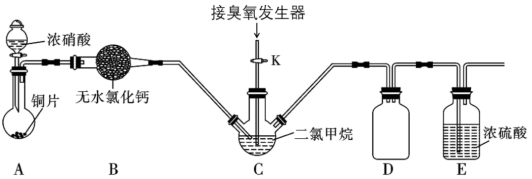
装置B的仪器名称是_______ ;装置E的作用是_______ 。实验时,先将三口烧瓶C浸入_______ (填字母编号)中,打开装置A中分液漏斗的活塞,随即关闭。一段时间后C中液体变为红棕色。然后打开活塞K,通过臭氧发生器向三口烧瓶中通入含有臭氧的氧气。
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CH2Cl2)的作用是_______ (填字母编号)。判断C中反应已结束的简单方法是_______ 。
a.溶解反应物NO2 b.充分混合反应物使其反应更加充分 c.控制O3的通入速度 d.溶解生成物N2O5
(4)该装置存在一处明显缺陷,请指出_______ 。
(5)N2O5粗产品中常含有N2O4。该兴趣小组用滴定法测定N2O5粗产品的纯度。取2.0g粗产品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。已知:N2O4与KMnO4发生反应的离子方程式为5N2O4+2MnO +2H2O→Mn2++10NO
+2H2O→Mn2++10NO +4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO
+4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO +6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
+6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是_______ 。粗产品的纯度为_______ (结果保留三位有效数字)。
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体N2O5。该反应的氧化产物为空气中的主要成分之一,写出反应的化学方程式:
(2)某化学兴趣小组设计用臭氧(O3)氧化法制备N2O5,反应原理为 N2O4+O3→N2O5+O2。实验装置如下图:

装置B的仪器名称是
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CH2Cl2)的作用是
a.溶解反应物NO2 b.充分混合反应物使其反应更加充分 c.控制O3的通入速度 d.溶解生成物N2O5
(4)该装置存在一处明显缺陷,请指出
(5)N2O5粗产品中常含有N2O4。该兴趣小组用滴定法测定N2O5粗产品的纯度。取2.0g粗产品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。已知:N2O4与KMnO4发生反应的离子方程式为5N2O4+2MnO
 +2H2O→Mn2++10NO
+2H2O→Mn2++10NO +4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO
+4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO +6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
+6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
您最近一年使用:0次



