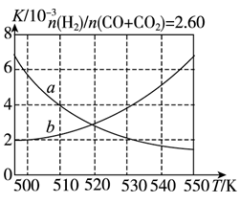
氮及其化合物在自然界中存在循环,请回答下列问题:
(1)氮元素在周期表中的位置是_______ ,氮原子核外电子共占据_______ 个轨道,最外层有_______ 种不同能量的电子。
(2)氨气分子的空间构型为_______ ,氮的最高价氧化物对应水化物的酸性比磷酸的酸性_______ (填“强”或者“弱”)。
(3)工业合成氨反应的化学平衡常数表达式为_______ 。一定条件下,在容积为2L的密闭容器中模拟该反应,测得10min时氮气为0.195mol,请计算0 ~ 10min的氨气的化学反应速率为_______ 。据图判断,反应进行至20 min时,曲线发生变化的原因是_______ (用文字表达)。

(4)工业上用氨水吸收SO2尾气,若最终得到(NH4)2SO4,则该溶液中c(NH )与c(SO
)与c(SO )之比
)之比_______ 2:1(选填“>”、“<”、“=”),请结合离子方程式解释其原因_______ 。
(1)氮元素在周期表中的位置是
(2)氨气分子的空间构型为
(3)工业合成氨反应的化学平衡常数表达式为

(4)工业上用氨水吸收SO2尾气,若最终得到(NH4)2SO4,则该溶液中c(NH
 )与c(SO
)与c(SO )之比
)之比
更新时间:2022/07/03 21:41:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知化学反应
①:Fe(s)+CO2(g) FeO(s)+CO(g),其化学平衡常数为K1
FeO(s)+CO(g),其化学平衡常数为K1
②:Fe(s)+H2O(g) FeO(s)+H2(g),其化学平衡常数为K2
FeO(s)+H2(g),其化学平衡常数为K2
在温度973 K和1173 K的情况下,K1、K2的值分别如下:
请填空:
(1)通过表格中的数值可以推断:反应①是_______ (填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g) CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=
CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=_______ 。推断出反应③是_______ (填“吸热”或“放热”)反应。
(3)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有_______ (填写字母序号)。
A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(4)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:
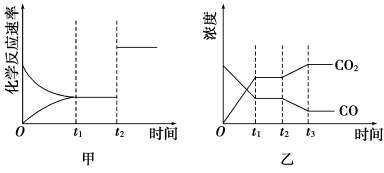
①图甲中t2时刻发生改变的条件是_______ 。
②图乙中t2时刻发生改变的条件是_______ 。
①:Fe(s)+CO2(g)
 FeO(s)+CO(g),其化学平衡常数为K1
FeO(s)+CO(g),其化学平衡常数为K1②:Fe(s)+H2O(g)
 FeO(s)+H2(g),其化学平衡常数为K2
FeO(s)+H2(g),其化学平衡常数为K2在温度973 K和1173 K的情况下,K1、K2的值分别如下:
K 温度 | K1 | K2 |
| 973 K | 1.47 | 2.38 |
| 1173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是
(2)现有反应③:CO2(g)+H2(g)
 CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=
CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=(3)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有
A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(4)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲中t2时刻发生改变的条件是
②图乙中t2时刻发生改变的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 高炉炼铁过程中发生的主要反应为 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)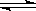
 Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0,(填>、<或 =);
(2)欲提高反应中CO的平衡转化率,可采取的措施是 ;
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.加入合适的催化剂
E.增大容器的容积
F.提高反应温度
(3)在一个容积为1L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各2.0mol,此时V(正) V(逆)(填“>”“<”或“=”),若反应经过5min后达到平衡.求该时间范围内反应的平均反应速率:v (CO2)= CO的平衡转化率= .
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)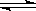
 Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0,(填>、<或 =);
(2)欲提高反应中CO的平衡转化率,可采取的措施是 ;
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.加入合适的催化剂
E.增大容器的容积
F.提高反应温度
(3)在一个容积为1L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各2.0mol,此时V(正) V(逆)(填“>”“<”或“=”),若反应经过5min后达到平衡.求该时间范围内反应的平均反应速率:v (CO2)= CO的平衡转化率= .
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)常温下,浓度均为 的8种溶液:①
的8种溶液:① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液;④
溶液;④ 溶液;⑤NaOH溶液;⑥
溶液;⑤NaOH溶液;⑥ 溶液;⑦KCl溶液;⑧
溶液;⑦KCl溶液;⑧ 溶液。这些溶液的pH由小到大的顺序是
溶液。这些溶液的pH由小到大的顺序是________ (填序号)。
(2)常温下, 的盐酸和
的盐酸和 的
的 溶液中,水电离出的
溶液中,水电离出的 分别为
分别为 和
和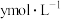 二者的关系正确的是
二者的关系正确的是________ (填字母)。
a.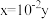 b.
b.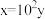 c.
c. d.
d.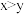
(3)常温下, HA溶液中
HA溶液中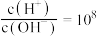 。现取
。现取 HA溶液与
HA溶液与 的NaOH溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题
的NaOH溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题
①混合溶液呈________ (填“酸”“中”或“碱”)性理由是__________ (用离子方程式表示)
②混合溶液中由水电离出的
________  ;NaOH溶液中由水电离出的
;NaOH溶液中由水电离出的
_______  。(填“大于”“小于”或“等于”)
。(填“大于”“小于”或“等于”)
 的8种溶液:①
的8种溶液:① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液;④
溶液;④ 溶液;⑤NaOH溶液;⑥
溶液;⑤NaOH溶液;⑥ 溶液;⑦KCl溶液;⑧
溶液;⑦KCl溶液;⑧ 溶液。这些溶液的pH由小到大的顺序是
溶液。这些溶液的pH由小到大的顺序是(2)常温下,
 的盐酸和
的盐酸和 的
的 溶液中,水电离出的
溶液中,水电离出的 分别为
分别为 和
和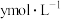 二者的关系正确的是
二者的关系正确的是a.
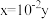 b.
b.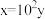 c.
c. d.
d.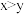
(3)常温下,
 HA溶液中
HA溶液中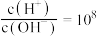 。现取
。现取 HA溶液与
HA溶液与 的NaOH溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题
的NaOH溶液等体积混合(忽略混合后溶液体积的变化)。试回答下列问题①混合溶液呈
②混合溶液中由水电离出的

 ;NaOH溶液中由水电离出的
;NaOH溶液中由水电离出的
 。(填“大于”“小于”或“等于”)
。(填“大于”“小于”或“等于”)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用0.01mol/L的NaOH溶液滴定 溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

(1)c点时溶液中各离子浓度由大到小的顺序为___________ 。
(2)b点时溶液显___________ 性,(填“酸”“碱”“中”性)原因是:___________ (用离子方程式解释);此时溶液中的质子守恒式为:___________ 。
(3)a点时溶液中电荷守恒式为:___________ 。
(4)硝酸银溶液和硫酸钠溶液混合,可以得到白色的硫酸银沉淀,向该分散系中滴加铬酸钠溶液,当白色沉淀和红色沉淀(铬酸银为红色沉淀)共存时,分散系中 =
=___________ [已知 ,
, ]。
]。
 溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
(1)c点时溶液中各离子浓度由大到小的顺序为
(2)b点时溶液显
(3)a点时溶液中电荷守恒式为:
(4)硝酸银溶液和硫酸钠溶液混合,可以得到白色的硫酸银沉淀,向该分散系中滴加铬酸钠溶液,当白色沉淀和红色沉淀(铬酸银为红色沉淀)共存时,分散系中
 =
= ,
, ]。
]。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,用0.1000mol/LNaOH溶液分别滴定20.00mL0.1000mol/LHCl溶液和20.00mL0.1000mol/LCH3COOH溶液,得到2条滴定曲线,如图所示:

(1)判断滴定HCl溶液的曲线是________ (填“图1”或“图2”);
(2)a=________ mL;
(3)c(Na+)=c(CH3COO-)的点是________ ;
(4)E点对应离子浓度由大到小的顺序为__________________________________ 。
(5)图1中,从A点到B点,溶液中水的电离程度逐渐________ (填“增大”或“减小”或“不变”);
(6)氢氧化钠溶液滴定盐酸溶液过程中,用酚酞作指示剂,请描述滴定终点的判断____________________________ 。

(1)判断滴定HCl溶液的曲线是
(2)a=
(3)c(Na+)=c(CH3COO-)的点是
(4)E点对应离子浓度由大到小的顺序为
(5)图1中,从A点到B点,溶液中水的电离程度逐渐
(6)氢氧化钠溶液滴定盐酸溶液过程中,用酚酞作指示剂,请描述滴定终点的判断
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为__________ 。
②NO3-的空间构型是____________________________________________ (用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O。
①根据等电子原理,CO分子的结构式为________ 。
②1 mol CO2中含有的σ键数目为____________ 。
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为______________ 。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为
②NO3-的空间构型是
(2)在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O。
①根据等电子原理,CO分子的结构式为
②1 mol CO2中含有的σ键数目为
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
您最近一年使用:0次
【推荐2】磷是人体所必需的重要矿物质元素,磷的化合物在生产和生活中应用广泛。
反应:P4+ NaOH+H2O→ NaH2PO2 +PH3(未配平)制得的次磷酸钠(NaH2PO2)可作食品防腐剂,也可用于化学镀镍。
请回答下列问题:
(1)磷原子的核外电子排布式:___________ ;磷原子核外有_____ 种能量不同的电子。
(2)上述反应的反应物和生成物中含有非极性键的分子是______ 。(写出物质的化学式)
(3)将Na、O、P三种原子的原子半径大小按由大到小的顺序排列___________________ 。
(4)NH3的稳定性比PH3的(填“强”或“弱”)_________ ,判断理由是____________ 。
(5)A、配平上述反应,并标出电子转移方向与数目_________
P4+ NaOH+ H2O→ NaH2PO2 + PH3
B、上述反应中每生成1 mol 氧化产物,转移电子的数目为___________ 。
反应:P4+ NaOH+H2O→ NaH2PO2 +PH3(未配平)制得的次磷酸钠(NaH2PO2)可作食品防腐剂,也可用于化学镀镍。
请回答下列问题:
(1)磷原子的核外电子排布式:
(2)上述反应的反应物和生成物中含有非极性键的分子是
(3)将Na、O、P三种原子的原子半径大小按由大到小的顺序排列
(4)NH3的稳定性比PH3的(填“强”或“弱”)
(5)A、配平上述反应,并标出电子转移方向与数目
P4+ NaOH+ H2O→ NaH2PO2 + PH3
B、上述反应中每生成1 mol 氧化产物,转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐3】Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+的核外电子排布式是_________________ 。
(2)在[Z(NH3)4]2+离子中,Z2+的空间轨道受NH3分子提供的_________ 形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是________ 。
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为____________ (用元素符号作答)
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为___________ 。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于___________ 。
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+的核外电子排布式是
(2)在[Z(NH3)4]2+离子中,Z2+的空间轨道受NH3分子提供的
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮是地球上极为丰富的元素。回答下列问题:
(1)氮化锂( )晶体中氮以
)晶体中氮以 存在,基态
存在,基态 核外电子排布式为
核外电子排布式为______ ,基态 核外电子占据的最高能级电子的电子云轮廓图形状为
核外电子占据的最高能级电子的电子云轮廓图形状为______ 。
(2)胸腺嘧啶是构成DNA的一种含氮碱基,结构简式如图所示。______ 。
②其分子中σ键和π键的数目之比为______ 。
③该胸腺嘧啶中含有官能团的名称______ 。
(3)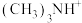 和
和 可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂
可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂______ (填“大”或“小”), 的空间结构为
的空间结构为______ 。
(4) 与
与 形成化合物的晶胞如图所示,与同一个
形成化合物的晶胞如图所示,与同一个 最近且等距的
最近且等距的 有
有______ 个。
(1)氮化锂(
 )晶体中氮以
)晶体中氮以 存在,基态
存在,基态 核外电子排布式为
核外电子排布式为 核外电子占据的最高能级电子的电子云轮廓图形状为
核外电子占据的最高能级电子的电子云轮廓图形状为(2)胸腺嘧啶是构成DNA的一种含氮碱基,结构简式如图所示。
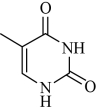
②其分子中σ键和π键的数目之比为
③该胸腺嘧啶中含有官能团的名称
(3)
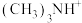 和
和 可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂
可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂 的空间结构为
的空间结构为(4)
 与
与 形成化合物的晶胞如图所示,与同一个
形成化合物的晶胞如图所示,与同一个 最近且等距的
最近且等距的 有
有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请根据以下转换填空:

(1)
(2)分子A中有_______ 个一级碳原子,有_______ 个二级碳原子,有_______ 个三级碳原子,有_______ 个
四级碳原子,至少有_______ 个氢原子共平面。
(3)B的同分异构体D的结构简式是:_______
(4)E是A的一种同分异构体,E含有sp、sp2、sp3杂化的碳原子,分子中没有甲基,E的结构简式是:_______

(1)
| (1)的反应条件 | (1)的反应类别 | (2)的反应类别 |
(2)分子A中有
四级碳原子,至少有
(3)B的同分异构体D的结构简式是:
(4)E是A的一种同分异构体,E含有sp、sp2、sp3杂化的碳原子,分子中没有甲基,E的结构简式是:
您最近一年使用:0次

 CH3OH(g) ΔH1=-99 kJ/mol,反应的化学平衡常数K表达式为
CH3OH(g) ΔH1=-99 kJ/mol,反应的化学平衡常数K表达式为