磷是人体所必需的重要矿物质元素,磷的化合物在生产和生活中应用广泛。
反应:P4+ NaOH+H2O→ NaH2PO2 +PH3(未配平)制得的次磷酸钠(NaH2PO2)可作食品防腐剂,也可用于化学镀镍。
请回答下列问题:
(1)磷原子的核外电子排布式:___________ ;磷原子核外有_____ 种能量不同的电子。
(2)上述反应的反应物和生成物中含有非极性键的分子是______ 。(写出物质的化学式)
(3)将Na、O、P三种原子的原子半径大小按由大到小的顺序排列___________________ 。
(4)NH3的稳定性比PH3的(填“强”或“弱”)_________ ,判断理由是____________ 。
(5)A、配平上述反应,并标出电子转移方向与数目_________
P4+ NaOH+ H2O→ NaH2PO2 + PH3
B、上述反应中每生成1 mol 氧化产物,转移电子的数目为___________ 。
反应:P4+ NaOH+H2O→ NaH2PO2 +PH3(未配平)制得的次磷酸钠(NaH2PO2)可作食品防腐剂,也可用于化学镀镍。
请回答下列问题:
(1)磷原子的核外电子排布式:
(2)上述反应的反应物和生成物中含有非极性键的分子是
(3)将Na、O、P三种原子的原子半径大小按由大到小的顺序排列
(4)NH3的稳定性比PH3的(填“强”或“弱”)
(5)A、配平上述反应,并标出电子转移方向与数目
P4+ NaOH+ H2O→ NaH2PO2 + PH3
B、上述反应中每生成1 mol 氧化产物,转移电子的数目为
更新时间:2020-05-26 19:06:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】Ⅰ、
(1)配平此反应的方程式:_____ 。
_____Zn+_____HNO3(稀)=_____Zn(NO3)2+_____NO↑+_____H2O。
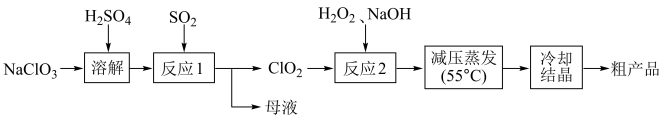
Ⅱ、亚氯酸钠(NaClO2)主要用于棉纺、造纸业,也用于食品消毒、水处理等,以氯酸钠(NaClO3)等为原料制备亚氯酸钠(NaClO2)的工艺流程如图。
(2)NaClO2中Cl的化合价为_____ 。
(3)写出反应1的化学方程式_____ 。
(4)反应2中的还原剂是_____ 。
(1)配平此反应的方程式:
_____Zn+_____HNO3(稀)=_____Zn(NO3)2+_____NO↑+_____H2O。
Ⅱ、亚氯酸钠(NaClO2)主要用于棉纺、造纸业,也用于食品消毒、水处理等,以氯酸钠(NaClO3)等为原料制备亚氯酸钠(NaClO2)的工艺流程如图。

(2)NaClO2中Cl的化合价为
(3)写出反应1的化学方程式
(4)反应2中的还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】配平下列氧化还原反应方程式:
(1)Mn2++O2+OH-→MnO(OH)2↓___
(2)MnO(OH)2+I-+H+→Mn2++I2+H2O___
(1)Mn2++O2+OH-→MnO(OH)2↓
(2)MnO(OH)2+I-+H+→Mn2++I2+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求回答下列问题
(1)在无色透明的强酸性溶液中能大量共存的离子组是_______ 。
①.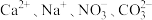
②.
③.
④.
⑤.Fe3+、K+、Cl-、S2-
⑥.Ag+、Na+、 、
、
⑦.Na+、Al3+、 、Cl-
、Cl-
⑧.Ba2+、 、C1-、CH3COO-
、C1-、CH3COO-
(2)①用单线桥表示反应电子转移的方向和数目: ,被氧化和被还原元素的物质的个数比
,被氧化和被还原元素的物质的个数比_______ 。
②用双线桥表示反应电子转移的方向和数目_______ 。
2Na2O2+2H2O=4NaOH+O2↑
反应每生成1个O2转移的电子数目为_______ 。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个配平 的化学方程式:_______ 。
_______+_______+H2SO4→_______+_______+_______(填化学式)
(1)在无色透明的强酸性溶液中能大量共存的离子组是
①.
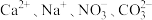
②.

③.

④.

⑤.Fe3+、K+、Cl-、S2-
⑥.Ag+、Na+、
 、
、
⑦.Na+、Al3+、
 、Cl-
、Cl-⑧.Ba2+、
 、C1-、CH3COO-
、C1-、CH3COO-(2)①用单线桥表示反应电子转移的方向和数目:
 ,被氧化和被还原元素的物质的个数比
,被氧化和被还原元素的物质的个数比②用双线桥表示反应电子转移的方向和数目
2Na2O2+2H2O=4NaOH+O2↑
反应每生成1个O2转移的电子数目为
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个
_______+_______+H2SO4→_______+_______+_______(填化学式)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下面是18×7的格子,按要求作答。

(1)用实线绘出过渡元素的边框____ (注意:不得使用铅笔作图)。
(2)Fe元素在周期表中的位置是____ ;只由元素②形成的18电子微粒为____ 。
(3)②、③、⑤、⑥、⑦的简单离子半径由大到小顺序是____ (填写离子符号)。请用电子式表示④和⑦形成的化合物的过程____ 。
(4)写出③的单质与H2O反应的化学方程式____ 。
(5)请从两个不同的角度预测SeO2可能具有的性质____ 和____ (表述示例:HNO3具有酸的通性和氧化性)。
(6)FeO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是____ 。

(1)用实线绘出过渡元素的边框
(2)Fe元素在周期表中的位置是
(3)②、③、⑤、⑥、⑦的简单离子半径由大到小顺序是
(4)写出③的单质与H2O反应的化学方程式
(5)请从两个不同的角度预测SeO2可能具有的性质
(6)FeO
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硒( )是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取而得。
)是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取而得。
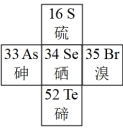
(1)硒在元素周期表中的位置如图所示:
① 在元素周期表中位置表示为
在元素周期表中位置表示为_______ ;
②用电子式表示 的形成过程:
的形成过程:_______ 。
(2)阳极泥中的硒主要以 和
和 的形式存在,工业上提取硒的流程如下:
的形式存在,工业上提取硒的流程如下:
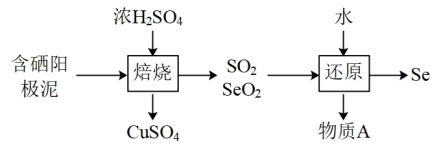
①请写出 与浓
与浓 反应的化学方程式:
反应的化学方程式:_______ 。
②写出“还原”步骤对应的化学方程式,并用单线桥标出电子转移情况:_______ 。
(3)下列说法正确的是_______。
 )是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取而得。
)是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取而得。
(1)硒在元素周期表中的位置如图所示:
①
 在元素周期表中位置表示为
在元素周期表中位置表示为②用电子式表示
 的形成过程:
的形成过程:(2)阳极泥中的硒主要以
 和
和 的形式存在,工业上提取硒的流程如下:
的形式存在,工业上提取硒的流程如下:
①请写出
 与浓
与浓 反应的化学方程式:
反应的化学方程式:②写出“还原”步骤对应的化学方程式,并用单线桥标出电子转移情况:
(3)下列说法正确的是_______。
A. 既有氧化性又有还原性 既有氧化性又有还原性 | B.原子半径由大到小顺序: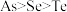 |
C.热稳定性: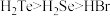 | D.酸性: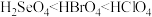 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表列出了a~m 13种元素在周期表(已省略了过渡元素 )中的位置:
(1)元素b为________ (填名称);画出g的原子结构示意图__________ 。
(2)元素f、i、j的原子半径从大到小的顺序是____________ (用元素符号表示);这三种原子分别形成简单离子后,离子半径从大到小的顺序是_____________ (用离子符号表示)。
(3)h和k的原子序数相差___________ (填数字)。
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为___________ ,该化合物中化学键有____________ ,该化合物与c的最高价氧化物反应的化学方程式为_________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | a | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h | i | |||
| 4 | j | k | l | |||||
| 5 | m |
(1)元素b为
(2)元素f、i、j的原子半径从大到小的顺序是
(3)h和k的原子序数相差
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,通常水加热至100℃时变为水蒸气,加热至2000℃会缓慢分解为 和
和 ,从粒子间的相互作用角度进行分析,这两种变化有所不同。
,从粒子间的相互作用角度进行分析,这两种变化有所不同。
(1)水加热至100℃变为水蒸气时,破坏的粒子间的相互作用包含_______ ,加热至2000℃分解为 和
和 时破坏的粒子间的相互作用是
时破坏的粒子间的相互作用是_______ 。
(2)以上三种作用力由大到小的顺序是_______ 。
(3)H、 、
、 半径由大到小的顺序是
半径由大到小的顺序是_______ 。
 和
和 ,从粒子间的相互作用角度进行分析,这两种变化有所不同。
,从粒子间的相互作用角度进行分析,这两种变化有所不同。(1)水加热至100℃变为水蒸气时,破坏的粒子间的相互作用包含
 和
和 时破坏的粒子间的相互作用是
时破坏的粒子间的相互作用是(2)以上三种作用力由大到小的顺序是
(3)H、
 、
、 半径由大到小的顺序是
半径由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】D、E、X、Y、Z是元素周期表中的前20号元素,且原子序数逐渐增大。它们的最简氢化物分子的立体构型依次是正四面体、三角锥形、正四面体、V形、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为________ 。
(2)上述五种元素中,能形成酸性最强的含氧酸的元素是________ ,写出该元素的任意三种含氧酸的化学式:________________________________ 。
(3)D和Y形成的化合物,其分子的空间构型为________ 。
(4)D和X形成的化合物,其化学键类型属于________ 。
(5)金属镁和E的单质在高温下反应得到的产物是________ ,此产物与水反应生成两种碱,该反应的化学方程式是____________________________________________ 。
(1)Y的最高价氧化物的化学式为
(2)上述五种元素中,能形成酸性最强的含氧酸的元素是
(3)D和Y形成的化合物,其分子的空间构型为
(4)D和X形成的化合物,其化学键类型属于
(5)金属镁和E的单质在高温下反应得到的产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】胃舒平主要成分是氢氧化铝,同时含有三硅镁(Mg2Si3O8·H2O)等化合物。
(1)比较铝离子和镁离子半径大小______________ (用离子符号表示)。
(2)比较铝和镁的第一电离能大小____________ (用元素符号表示);
(3)下列事实不能说明镁比铝的金属性强的是____________ ;
A.Al(OH)3可溶于强碱溶液中,Mg(OH)2不能
B.Mg能从铝盐溶液中置换出铝
C.Mg 原子最外层只有2个电子,而Al原子最外层有3个电子
D.Mg与盐酸反应比铝与盐酸反应更剧烈
(4)已知电负性:Mg- 1.2,Al- 1.5,Cl-3.0 。则MgCl2晶体中存在的作用力是__________ ;AlBr3属于_________ (填“离子”或“共价”)化合物;
(5)某元素与镁元素不同周期但在相邻主族,且性质和镁元素性质十分相似,该元素符号是_______ ,原子核外电子排布式为________________ 。
(6) Al2O3、MgO都有很高的熔点,都可以制耐火材料,其原因是________________ 。
(1)比较铝离子和镁离子半径大小
(2)比较铝和镁的第一电离能大小
(3)下列事实不能说明镁比铝的金属性强的是
A.Al(OH)3可溶于强碱溶液中,Mg(OH)2不能
B.Mg能从铝盐溶液中置换出铝
C.Mg 原子最外层只有2个电子,而Al原子最外层有3个电子
D.Mg与盐酸反应比铝与盐酸反应更剧烈
(4)已知电负性:Mg- 1.2,Al- 1.5,Cl-3.0 。则MgCl2晶体中存在的作用力是
(5)某元素与镁元素不同周期但在相邻主族,且性质和镁元素性质十分相似,该元素符号是
(6) Al2O3、MgO都有很高的熔点,都可以制耐火材料,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇及其化合物可制成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的烯丙醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
①基态镍原子的价电子排布式为___________________ 。
②1 mol CH2=CH-CH2OH含____ molσ键,烯丙醇分子中碳原子的杂化类型为________ 。
③ Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2- 和[Ni(SCN)2]- 等,与CN-互为等电子体的分子为____________ 。
(2)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
①CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为_____________ ; lmol O22+中含有的π键数目为_______________ 。
②将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为____________ 。
③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是_______________ ;分子中处于同一直线上的原子数目最多为_______________ 。
①基态镍原子的价电子排布式为
②1 mol CH2=CH-CH2OH含
③ Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2- 和[Ni(SCN)2]- 等,与CN-互为等电子体的分子为
(2)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
①CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为
②将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)N的核外电子排布式为____ ,Cu的外围电子排布式为 _____ ,CO2的其中一种等电子体的化学式或符号是____ ,[Co(NH3)4 Cl2] Cl中,中心原子的配位数是__________ 。
(2)SO3 2-离子中,孤对电子数是____ ,价层电子对数是 ____ ,VSEPR构型是 _____ ,立体构型是_____ ,S采取的杂化方式是_____ 。
(3)乙炔与氢氰酸反应可得丙烯腈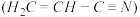 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是______ 、_____ ;分子中处于同一平面上的原子数目最多为_________ 。
(4)丙烯(CH3—CH =CH2)分子中,官能团上的碳原子采取的是____ 杂化方式,分子中有____ 个s-sp3 键,
键,____ 个sp2 -sp3 键和
键和___ 个p-p 键。
键。
(2)SO3 2-离子中,孤对电子数是
(3)乙炔与氢氰酸反应可得丙烯腈
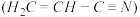 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是(4)丙烯(CH3—CH =CH2)分子中,官能团上的碳原子采取的是
 键,
键, 键和
键和 键。
键。
您最近一年使用:0次

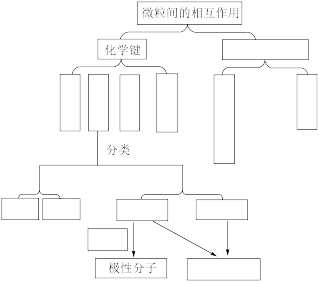
 键、极性键、非极性键、离子键、配位键、金属键、范德华力、氢键、分子空间结构、极性分子、非极性分子等,请通过图示的方式表示它们之间的相互关系,以加深对所学内容的理解
键、极性键、非极性键、离子键、配位键、金属键、范德华力、氢键、分子空间结构、极性分子、非极性分子等,请通过图示的方式表示它们之间的相互关系,以加深对所学内容的理解