名校
解题方法
1 . 从化学键的角度解释石墨的熔点高于金刚石的原因_______ 。
您最近一年使用:0次
名校
2 . 甲乙酮肟(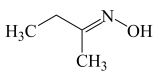 )中同周期三种元素电负性由大到小的顺序为
)中同周期三种元素电负性由大到小的顺序为
您最近一年使用:0次
名校
解题方法
3 .  与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为_______ ,其空间构型为_______ 。
 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为
您最近一年使用:0次
4 . 碳的多种同素异形体及一系列化合物广泛应用于科研、医疗、工农业生产等领域。
(1)写出基态C原子核外电子排布的轨道表示式_______ 。
(2)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成负离子的是_______。
(1)写出基态C原子核外电子排布的轨道表示式
(2)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成负离子的是_______。
A. | B. | C. | D.苯 |
您最近一年使用:0次
名校
解题方法
5 . 密闭容器中,加入足量的焦炭(沸点4827℃)和1mol 反应,生成
反应,生成 和硫蒸气(
和硫蒸气( ):
): 。反应在某温度达到平衡时,
。反应在某温度达到平衡时, 和
和 的体积分数都等于40%。
的体积分数都等于40%。
(1) 中
中
_______ 。
(2)按相同投料方式发生上述反应,相同时间内测得 与
与 的生成速率随温度变化的关系如图1所示。其他条件相同时,在不同催化剂作用下,
的生成速率随温度变化的关系如图1所示。其他条件相同时,在不同催化剂作用下, 转化率与温度关系如图2所示。
转化率与温度关系如图2所示。_______ (填“甲”或“乙”)活性更高,理由是_______ 。
②由图中信息可知,A、B、C三点对应的反应状态中,达到平衡状态的是_______ (填字母),原因是_______ 。
 反应,生成
反应,生成 和硫蒸气(
和硫蒸气( ):
): 。反应在某温度达到平衡时,
。反应在某温度达到平衡时, 和
和 的体积分数都等于40%。
的体积分数都等于40%。(1)
 中
中
(2)按相同投料方式发生上述反应,相同时间内测得
 与
与 的生成速率随温度变化的关系如图1所示。其他条件相同时,在不同催化剂作用下,
的生成速率随温度变化的关系如图1所示。其他条件相同时,在不同催化剂作用下, 转化率与温度关系如图2所示。
转化率与温度关系如图2所示。
②由图中信息可知,A、B、C三点对应的反应状态中,达到平衡状态的是
您最近一年使用:0次
名校
解题方法
6 . T℃时,向2.0L的恒容密闭容器中充入1.0mol 和0.6mol
和0.6mol ,发生如下反应:
,发生如下反应: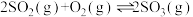 。20s时反应达到平衡,
。20s时反应达到平衡,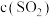 和
和 相等。
相等。
(1)0~20s内,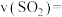
_______  。
。
(2)平衡后向容器中再充入0.4mol 和0.3mol
和0.3mol ,此时,
,此时, _______
_______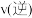 。
。
(3)相同温度下,起始投料变为0.5mol 和0.3mol
和0.3mol ,
, 的平衡转化率_______。
的平衡转化率_______。
 和0.6mol
和0.6mol ,发生如下反应:
,发生如下反应: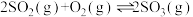 。20s时反应达到平衡,
。20s时反应达到平衡,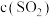 和
和 相等。
相等。(1)0~20s内,
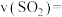
 。
。(2)平衡后向容器中再充入0.4mol
 和0.3mol
和0.3mol ,此时,
,此时, _______
_______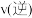 。
。| A.大于 | B.小于 | C.等于 | D.无法判断 |
(3)相同温度下,起始投料变为0.5mol
 和0.3mol
和0.3mol ,
, 的平衡转化率_______。
的平衡转化率_______。| A.增大 | B.不变 | C.减小 | D.无法判断 |
您最近一年使用:0次
名校
7 . 硫元素在周期表中位于
| A.s区 | B.p区 | C.第三周期第ⅣA族 | D.第3周期第16族 |
您最近一年使用:0次
解题方法
8 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe,还有少量其他不溶性物质。采用如图工艺流程回收其中的镍并制备硫酸镍晶体:
(1)“碱浸”中NaOH的作用有 ___________ 、___________ 。
(2)滤液②中含有的金属离子是 ___________。
(3)“转化”步骤中H2O2的作用是 ___________ ,c(H2O2)随时间t的变化关系如图所示,反应开始10~20min内c(H2O2)迅速减小,原因可能是 ___________ 。(不考虑温度变化)
资料显示,硫酸镍结晶水合物的形态与温度有如表的关系:
(5)从滤液③中获得NiSO4•6H2O晶体的操作依次是 ___________ 、___________ 、过滤、洗涤、干燥。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其目的是___________ 。
实验室有一份NiSO4•xH2O样品,为测定其结晶水数目x,将4.188g样品加热至300℃充分反应,最终残留固体质量为2.328g。
(7)该样品中结晶水数目x为多少?___________ (结果精确至0.1,写出计算过程)
(8)再设计一种实验方案测定样品结晶水数目x(简述实验过程)。___________ 。

| 金属离子 | 开始沉淀时的pH | 沉淀完全时的pH |
| Ni2+ | 7.2 | 8.7 |
| Al3+ | 3.7 | 4.7 |
| Fe3+ | 2.2 | 3.2 |
| Fe2+ | 7.5 | 9.5 |
(2)滤液②中含有的金属离子是 ___________。
| A.Ni2+ | B.Al3+ | C.Fe3+ | D.Fe2+ |
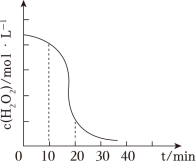
| A.2.2 | B.3.2 | C.3.7 | D.4.7 |
资料显示,硫酸镍结晶水合物的形态与温度有如表的关系:
| 温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
| 晶体形态 | NiSO4•7H2O | NiSO4•6H2O | 多种结晶水合物 | NiSO4 |
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其目的是
实验室有一份NiSO4•xH2O样品,为测定其结晶水数目x,将4.188g样品加热至300℃充分反应,最终残留固体质量为2.328g。
(7)该样品中结晶水数目x为多少?
(8)再设计一种实验方案测定样品结晶水数目x(简述实验过程)。
您最近一年使用:0次
9 . 大气中 能通过高温下与
能通过高温下与 反应进行协同转化处理。反应原理为:
反应进行协同转化处理。反应原理为: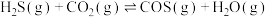 ,工业中测得的产物中有
,工业中测得的产物中有 、
、 、CO等副产物。
、CO等副产物。
(1)一定温度下,在恒容密闭容器中发生以上反应,下列条件能判断反应达到平衡状态的是___________。
(2)在573K下,向2L恒容密闭容器中通入2mol 和1mol
和1mol  ,反应达到平衡后水蒸气的物质的量分数为0.2。
,反应达到平衡后水蒸气的物质的量分数为0.2。
①上述条件下 的平衡转化率
的平衡转化率
___________ %。
②在上述平衡体系中再加2mol 和2mol
和2mol  ,通过数据说明平衡移动的方向
,通过数据说明平衡移动的方向___________ 。
(3)在不同温度下,向密闭容器甲、乙中分别充入2mol 和1mol
和1mol  ,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下反应,测得的
,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下反应,测得的 平衡转化率随温度变化关系如图所示。
平衡转化率随温度变化关系如图所示。___________ 。
A.甲 B.乙 C.甲、乙中任一个
②1173K以后平衡转化率变化的原因可能是___________ 。
 能通过高温下与
能通过高温下与 反应进行协同转化处理。反应原理为:
反应进行协同转化处理。反应原理为: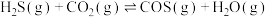 ,工业中测得的产物中有
,工业中测得的产物中有 、
、 、CO等副产物。
、CO等副产物。(1)一定温度下,在恒容密闭容器中发生以上反应,下列条件能判断反应达到平衡状态的是___________。
A.容器内 不再生成 不再生成 | B.容器内压强不再发生变化 |
| C.容器内气体密度不再发生变化 | D. |
(2)在573K下,向2L恒容密闭容器中通入2mol
 和1mol
和1mol  ,反应达到平衡后水蒸气的物质的量分数为0.2。
,反应达到平衡后水蒸气的物质的量分数为0.2。①上述条件下
 的平衡转化率
的平衡转化率
②在上述平衡体系中再加2mol
 和2mol
和2mol  ,通过数据说明平衡移动的方向
,通过数据说明平衡移动的方向(3)在不同温度下,向密闭容器甲、乙中分别充入2mol
 和1mol
和1mol  ,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下反应,测得的
,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下反应,测得的 平衡转化率随温度变化关系如图所示。
平衡转化率随温度变化关系如图所示。
A.甲 B.乙 C.甲、乙中任一个
②1173K以后平衡转化率变化的原因可能是
您最近一年使用:0次
名校
10 . 缓释布洛芬具有解热、镇痛、抗炎等功效,一种合成缓释布洛芬的路线如下:
(1)化合物Ⅰ的分子式为___________ ,缓释布洛芬的结构简式为___________ 。
(2)化合物Ⅱ易溶于水的原因是___________ ,化合物Ⅳ+Ⅴ→Ⅵ的反应类型是___________ 。
(3)根据化合物Ⅲ的结构特征,分析预测其可能的化学性质,完成下表。
(4)写出Ⅲ→Ⅳ的化学方程式:___________ 。
(5)同时满足下列条件的化合物Ⅴ的同分异构体共有___________ 种(不考虑立体异构),其中核磁共振氢谱中峰面积比为6∶3∶2∶2∶1的结构简式为___________ 。
①属于芳香族化合物;②苯环上含有两个取代基。
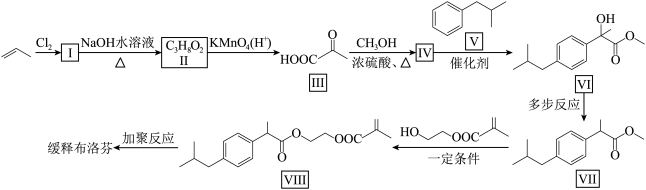
(1)化合物Ⅰ的分子式为
(2)化合物Ⅱ易溶于水的原因是
(3)根据化合物Ⅲ的结构特征,分析预测其可能的化学性质,完成下表。
| 序号 | 结构特征 | 可反应的试剂 | 反应形成的新结构 | 反应类型 |
| ① |
| 还原反应 | ||
| ② | Na | 取代反应 |
(4)写出Ⅲ→Ⅳ的化学方程式:
(5)同时满足下列条件的化合物Ⅴ的同分异构体共有
①属于芳香族化合物;②苯环上含有两个取代基。
您最近一年使用:0次
2024-05-07更新
|
1035次组卷
|
3卷引用:上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题
上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题广东省部分学校2024届高三百日冲刺联合学业质量监测(一模)化学试题(已下线)题型12 有机推断题(25题)-2024年高考化学常考点必杀300题(新高考通用)