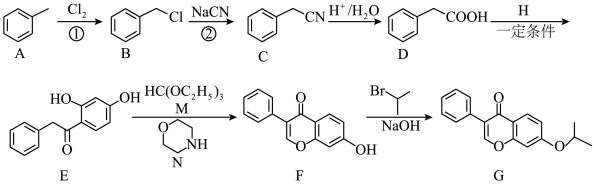
1 . 化合物G俗称依普黄酮,是一种抗骨质疏松药物的主要成分。以甲苯为原料合成该化合物的路线如下图所示:___________ 。
(2)E中官能团的名称为___________ ,反应F→G的反应类型为___________ 。
(3)E与足量的 完全加成后所生成的化合物中手性碳原子(碳原子上连接四个不同的原子或基团)的个数为
完全加成后所生成的化合物中手性碳原子(碳原子上连接四个不同的原子或基团)的个数为___________ 。
(4)已知N为催化剂,则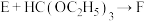 的化学方程式为
的化学方程式为___________ 。
(5)K是D的同系物,其相对分子质量比D多14,满足下列条件的K的同分异构体共有___________ 种。
①苯环上只有两个取代基;
②能与Na反应生成 ;
;
③能与银氨溶液发生银镜反应。
(6)根据上述信息,设计以苯酚和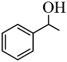 为原料,制备
为原料,制备 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)___________ 。
已知:
(2)E中官能团的名称为
(3)E与足量的
 完全加成后所生成的化合物中手性碳原子(碳原子上连接四个不同的原子或基团)的个数为
完全加成后所生成的化合物中手性碳原子(碳原子上连接四个不同的原子或基团)的个数为(4)已知N为催化剂,则
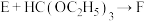 的化学方程式为
的化学方程式为(5)K是D的同系物,其相对分子质量比D多14,满足下列条件的K的同分异构体共有
①苯环上只有两个取代基;
②能与Na反应生成
 ;
;③能与银氨溶液发生银镜反应。
(6)根据上述信息,设计以苯酚和
 为原料,制备
为原料,制备 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)
您最近一年使用:0次
解题方法
2 . 硒(Se)被国内外医药界和营养学界尊称为“生命的火种”,享有“长寿元素”“抗癌之王”“心脏守护神”“天然解毒剂”等美誉。硒在电子工业中可用作光电管、太阳能电池,硒元素形成的多种化合物也有重要作用。
(1)硒和硫同为 A族元素,基态硒原子的价层电子排布式为
A族元素,基态硒原子的价层电子排布式为___________ 。
(2)单质硒的熔点为221℃,其晶体类型为___________ 。
(3)与硒元素相邻的同周期元素是砷和溴,则这三种元素的第一电离能由小到大的顺序为___________ (用元素符号表示)。
(4) 分子中Se原子的杂化轨道类型为
分子中Se原子的杂化轨道类型为___________ ; 的立体构型是
的立体构型是___________ ,写出一种与 互为等电子体的分子
互为等电子体的分子___________ (写化学式)。
(5) 分子中含有的共价键是
分子中含有的共价键是___________ (选填“极性键”或“非极性键”); 水溶液比
水溶液比 水溶液的酸性强,原因是
水溶液的酸性强,原因是___________ 。
(6) -AgI可用作固体离子导体,能通过加热
-AgI可用作固体离子导体,能通过加热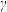 -Ag制得。上述两种晶体的晶胞示意图如图1所示(为了简化,只画出了碘离子在晶胞中的位置)。
-Ag制得。上述两种晶体的晶胞示意图如图1所示(为了简化,只画出了碘离子在晶胞中的位置)。___________ (填字母)。
A.质谱仪 B.红外光谱仪 C.核磁共振仪 D.X射线衍射仪
②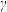 -AgI与
-AgI与 -AgI晶胞的体积之比为
-AgI晶胞的体积之比为___________ 。
③测定 -AgI中导电离子类型的实验装置如图2所示,实验测得支管a中AgI质量不变,可判定导电离子是
-AgI中导电离子类型的实验装置如图2所示,实验测得支管a中AgI质量不变,可判定导电离子是 而不是
而不是 ,依据是
,依据是___________ 。
(1)硒和硫同为
 A族元素,基态硒原子的价层电子排布式为
A族元素,基态硒原子的价层电子排布式为(2)单质硒的熔点为221℃,其晶体类型为
(3)与硒元素相邻的同周期元素是砷和溴,则这三种元素的第一电离能由小到大的顺序为
(4)
 分子中Se原子的杂化轨道类型为
分子中Se原子的杂化轨道类型为 的立体构型是
的立体构型是 互为等电子体的分子
互为等电子体的分子(5)
 分子中含有的共价键是
分子中含有的共价键是 水溶液比
水溶液比 水溶液的酸性强,原因是
水溶液的酸性强,原因是(6)
 -AgI可用作固体离子导体,能通过加热
-AgI可用作固体离子导体,能通过加热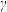 -Ag制得。上述两种晶体的晶胞示意图如图1所示(为了简化,只画出了碘离子在晶胞中的位置)。
-Ag制得。上述两种晶体的晶胞示意图如图1所示(为了简化,只画出了碘离子在晶胞中的位置)。
A.质谱仪 B.红外光谱仪 C.核磁共振仪 D.X射线衍射仪
②
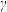 -AgI与
-AgI与 -AgI晶胞的体积之比为
-AgI晶胞的体积之比为③测定
 -AgI中导电离子类型的实验装置如图2所示,实验测得支管a中AgI质量不变,可判定导电离子是
-AgI中导电离子类型的实验装置如图2所示,实验测得支管a中AgI质量不变,可判定导电离子是 而不是
而不是 ,依据是
,依据是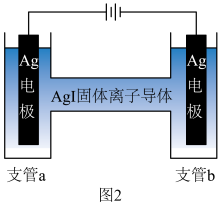
您最近一年使用:0次
解题方法
3 . 乙醇水蒸气重整制 的热化学方程式为
的热化学方程式为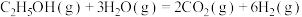
 ,其化学过程可以表述为一系列基元反应,结合反应间联系进一步整理可以得到如下的四个主反应:
,其化学过程可以表述为一系列基元反应,结合反应间联系进一步整理可以得到如下的四个主反应:
反应 :
: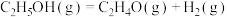
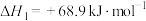
反应 :
: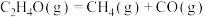
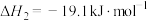
反应 :
: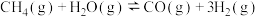
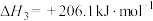
反应 :
: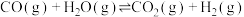
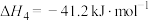
(1)根据题干,
___________  ,平衡时CO的选择性随温度的变化应是图中曲线
,平衡时CO的选择性随温度的变化应是图中曲线___________ (填图中曲线编号)[已知:CO的选择性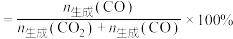 ],理由是
],理由是___________ 。___________ ,原因是___________ 。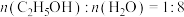 投料,初始压强为p kPa,充分反应后,将混合气体干燥处理,测得
投料,初始压强为p kPa,充分反应后,将混合气体干燥处理,测得 占混合气体(干燥后)总体积的50%,
占混合气体(干燥后)总体积的50%, 占10%,则反应Ⅲ的平衡常数
占10%,则反应Ⅲ的平衡常数
___________ [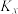 为用摩尔分数表示的平衡常数,
为用摩尔分数表示的平衡常数,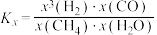 ,x表示该物质占气体的物质的量分数],到达平衡时体系中CO的分压为
,x表示该物质占气体的物质的量分数],到达平衡时体系中CO的分压为___________ kPa, 的产率
的产率___________ (保留2位有效数字)。
 的热化学方程式为
的热化学方程式为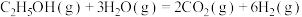
 ,其化学过程可以表述为一系列基元反应,结合反应间联系进一步整理可以得到如下的四个主反应:
,其化学过程可以表述为一系列基元反应,结合反应间联系进一步整理可以得到如下的四个主反应:反应
 :
: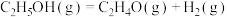
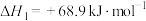
反应
 :
: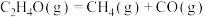
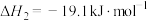
反应
 :
: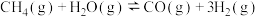
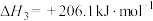
反应
 :
: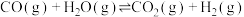
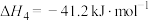
(1)根据题干,

 ,平衡时CO的选择性随温度的变化应是图中曲线
,平衡时CO的选择性随温度的变化应是图中曲线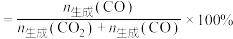 ],理由是
],理由是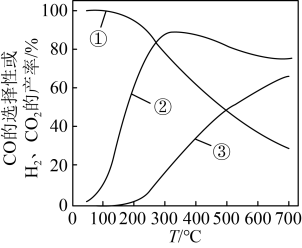
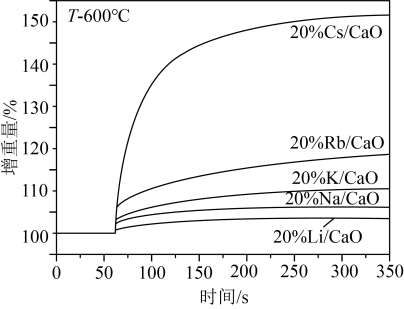
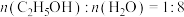 投料,初始压强为p kPa,充分反应后,将混合气体干燥处理,测得
投料,初始压强为p kPa,充分反应后,将混合气体干燥处理,测得 占混合气体(干燥后)总体积的50%,
占混合气体(干燥后)总体积的50%, 占10%,则反应Ⅲ的平衡常数
占10%,则反应Ⅲ的平衡常数
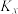 为用摩尔分数表示的平衡常数,
为用摩尔分数表示的平衡常数,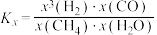 ,x表示该物质占气体的物质的量分数],到达平衡时体系中CO的分压为
,x表示该物质占气体的物质的量分数],到达平衡时体系中CO的分压为 的产率
的产率
您最近一年使用:0次
解题方法
4 . 四氧化三锰( )是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)为原料制备高纯
)是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)为原料制备高纯 的工艺流程如下图所示。
的工艺流程如下图所示。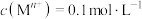 ]形成氢氧化物沉淀的pH范围如下表:
]形成氢氧化物沉淀的pH范围如下表:
回答下列问题:
(1)“氧化”中添加适量的 的作用是
的作用是___________ (用离子方程式表示)。
(2)“除杂1”的目的是除去 、
、 等杂质离子,则“滤渣3”中主要有
等杂质离子,则“滤渣3”中主要有___________ ,“调pH”时溶液的pH范围应调节为___________ 之间。
(3)“除杂2”的目的是生成 沉淀除去
沉淀除去 ,若溶液酸度过高,会导致
,若溶液酸度过高,会导致___________ 。
(4))常温下,利用表格中的数据,计算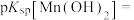
___________ (已知 )。
)。
(5)在“沉锰”时,可用尿素[ ]代替
]代替 ,同时控制温度在115~120℃,写出尿素“沉锰”反应的离子方程式
,同时控制温度在115~120℃,写出尿素“沉锰”反应的离子方程式___________ 。
(6) 和氨水混合在80℃下得到的
和氨水混合在80℃下得到的 的产率最高,若继续升高温度,会导致产率降低,原因可能是
的产率最高,若继续升高温度,会导致产率降低,原因可能是___________ 。
 )是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)为原料制备高纯
)是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)为原料制备高纯 的工艺流程如下图所示。
的工艺流程如下图所示。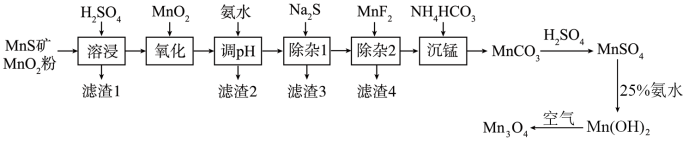
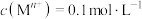 ]形成氢氧化物沉淀的pH范围如下表:
]形成氢氧化物沉淀的pH范围如下表:| 金属离子 |  |  |  |  |  |  |  |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“氧化”中添加适量的
 的作用是
的作用是(2)“除杂1”的目的是除去
 、
、 等杂质离子,则“滤渣3”中主要有
等杂质离子,则“滤渣3”中主要有(3)“除杂2”的目的是生成
 沉淀除去
沉淀除去 ,若溶液酸度过高,会导致
,若溶液酸度过高,会导致(4))常温下,利用表格中的数据,计算
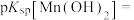
 )。
)。(5)在“沉锰”时,可用尿素[
 ]代替
]代替 ,同时控制温度在115~120℃,写出尿素“沉锰”反应的离子方程式
,同时控制温度在115~120℃,写出尿素“沉锰”反应的离子方程式(6)
 和氨水混合在80℃下得到的
和氨水混合在80℃下得到的 的产率最高,若继续升高温度,会导致产率降低,原因可能是
的产率最高,若继续升高温度,会导致产率降低,原因可能是
您最近一年使用:0次
5 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1.8g  中含有的中子数为0.8 中含有的中子数为0.8 |
B.100mL 1  溶液中含有阳离子的数目大于0.1 溶液中含有阳离子的数目大于0.1 |
C.33.8g过氧化钡( )固体中阴、阳离子总数为0.6 )固体中阴、阳离子总数为0.6 |
D.46g  分子中含极性键数目一定是7 分子中含极性键数目一定是7 |
您最近一年使用:0次
解题方法
6 . “活宁”是一种新型吸入式诱导麻醉药,麻醉性能强,常用作临床麻醉剂,其分子结构式如图所示。其中,X的原子核只有1个质子;元素Y、Z、W原子序数依次增大,均比X多一个电子层;元素E的原子比W原子核外多8个电子。下列说法不正确的是
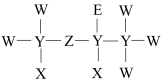
| A.由X、E、Z组成的化合物XEZ是一种强氧化性酸 |
| B.Y、Z、W分别与X形成的简单氢化物的沸点:Z>W>Y |
| C.Y、Z、W、E的氢化物中只有极性键 |
| D.ZW2中,Z的化合价为+2价 |
您最近一年使用:0次
7 . 室温下,向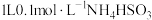 溶液中加入
溶液中加入 固体,溶液中
固体,溶液中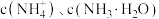 、
、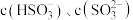 随
随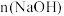 的变化如下图所示(忽略该过程中溶液体积和温度的变化)。已知:室温时,
的变化如下图所示(忽略该过程中溶液体积和温度的变化)。已知:室温时,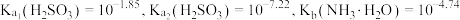 。下列说法不正确的是
。下列说法不正确的是
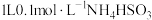 溶液中加入
溶液中加入 固体,溶液中
固体,溶液中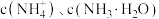 、
、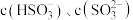 随
随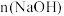 的变化如下图所示(忽略该过程中溶液体积和温度的变化)。已知:室温时,
的变化如下图所示(忽略该过程中溶液体积和温度的变化)。已知:室温时,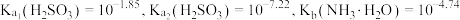 。下列说法不正确的是
。下列说法不正确的是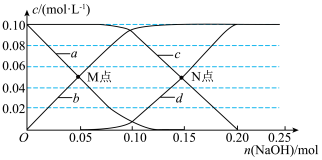
A.曲线 分别代表 分别代表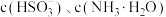 的变化 的变化 |
B.随 的加入, 的加入,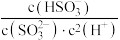 的值不断减小 的值不断减小 |
C.M点存在: |
D.N点时,溶液的 为9.26 为9.26 |
您最近一年使用:0次
2024-04-07更新
|
353次组卷
|
3卷引用:2024届陕西省宝鸡市高三下学期三模考试理科综合试题-高中化学
8 . 化学在“国之重器”的打造中发挥着重要作用。下列说法不正确的是
| A.“库车绿氢”用光伏发电电解水制氢,能有效减少碳排放 |
B.国产大飞机“ ”使用的芳纶蜂窝材料属于有机高分子材料 ”使用的芳纶蜂窝材料属于有机高分子材料 |
C.国产 “龙芯 “龙芯 ”的主要材料与光导纤维的材料相同 ”的主要材料与光导纤维的材料相同 |
| D.“鲲龙”水陆两栖飞机所用的航空煤油是石油分馏产品 |
您最近一年使用:0次
2024-04-07更新
|
412次组卷
|
2卷引用:2024届陕西省宝鸡市高三下学期三模考试理科综合试题-高中化学
9 . 在不同 环境的
环境的 溶液中,
溶液中, 可以转化为
可以转化为 或
或 沉淀。
沉淀。
 溶液中含碳粒子物质的量分数与
溶液中含碳粒子物质的量分数与 的关系如图1所示。
的关系如图1所示。 在图1对应
在图1对应 溶液中在不同
溶液中在不同 环境下,形成
环境下,形成 或
或 的溶解平衡关系如图2所示。下列说法错误的是
的溶解平衡关系如图2所示。下列说法错误的是

 环境的
环境的 溶液中,
溶液中, 可以转化为
可以转化为 或
或 沉淀。
沉淀。
 溶液中含碳粒子物质的量分数与
溶液中含碳粒子物质的量分数与 的关系如图1所示。
的关系如图1所示。 在图1对应
在图1对应 溶液中在不同
溶液中在不同 环境下,形成
环境下,形成 或
或 的溶解平衡关系如图2所示。下列说法错误的是
的溶解平衡关系如图2所示。下列说法错误的是
A.曲线Ⅰ代表 的溶解平衡曲线 的溶解平衡曲线 |
B.若溶液的 , ,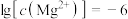 ,无沉淀生成 ,无沉淀生成 |
C.由图可知 的 的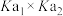 的数量级为 的数量级为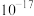 |
D.增大 , ,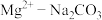 溶液体系中均可发生反应: 溶液体系中均可发生反应: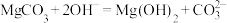 |
您最近一年使用:0次
10 . 化合物G是一种重要的合成药物中间体,其合成路线如图所示:
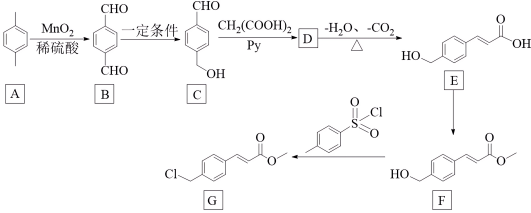
(1)A的名称为___________ ;E中含氧官能团的名称为___________ 。
(2)F→G的反应类型为___________ ;若C→D的反应类型为加成反应,则D的结构简式为___________ 。
(3)写出E→F反应的化学方程式___________ 。
(4)在E的同分异构体中,同时具备下列条件的结构有___________ 种(不考虑立体异构)。
①遇氯化铁溶液发生显色反应;
②能发生银镜反应和水解反应;
③苯环上只有三个取代基,其中一个取代基为环状结构。
符合上述条件的有机物体在酸性条件下水解时,生成的水解产物中,含苯环、核磁共振氢谱为5组峰,且面积之比为4∶2∶2∶1∶1的是___________ (任写一种水解产物的结构简式)。
(5)苯甲醇、丙二酸为原料合成肉桂酸(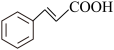 ),设计合成路线
),设计合成路线___________ (无机试剂任选)。

(1)A的名称为
(2)F→G的反应类型为
(3)写出E→F反应的化学方程式
(4)在E的同分异构体中,同时具备下列条件的结构有
①遇氯化铁溶液发生显色反应;
②能发生银镜反应和水解反应;
③苯环上只有三个取代基,其中一个取代基为环状结构。
符合上述条件的有机物体在酸性条件下水解时,生成的水解产物中,含苯环、核磁共振氢谱为5组峰,且面积之比为4∶2∶2∶1∶1的是
(5)苯甲醇、丙二酸为原料合成肉桂酸(
 ),设计合成路线
),设计合成路线
您最近一年使用:0次



