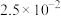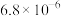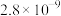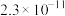名校
解题方法
1 . 亚砷酸C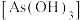 ,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数
,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数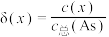 。下列说法错误的是
。下列说法错误的是
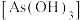 ,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数
,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数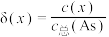 。下列说法错误的是
。下列说法错误的是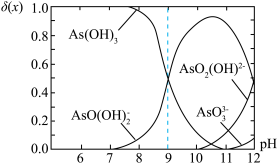
A. |
B. 时,水电离的 时,水电离的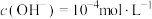 |
C.等物质的量浓度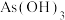 和 和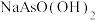 混合溶液中 混合溶液中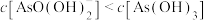 |
D.当溶液 后,体系中 后,体系中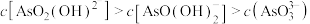 |
您最近一年使用:0次
2024-06-16更新
|
124次组卷
|
2卷引用:2024届陕西省部分学校高三下学期5月份高考适应性考试理科综合试题-高中化学
解题方法
2 . 硼(B)、钴( )和锰(
)和锰( )形成的物质在生产、生活中应用广泛。回答下列问题:
)形成的物质在生产、生活中应用广泛。回答下列问题:
(1)基态 原子核外电子排布式为
原子核外电子排布式为___________ ,在第二周期中,第一电离能比N高的元素是___________ (填元素符号)。
(2)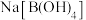 可用于织物漂白。
可用于织物漂白。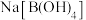 的化学键除了共价键外,还存在
的化学键除了共价键外,还存在___________ 。
(3)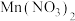 工业制备中常用的催化剂,
工业制备中常用的催化剂,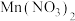 中阴离子的空间构型为
中阴离子的空间构型为___________ ;写出一种与其互为等电子体的分子式:___________ 。
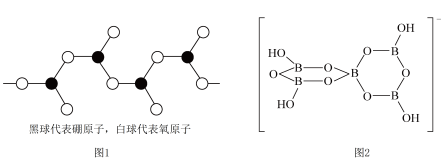
(4)如图1表示偏硼酸根的一种无限长的链式结构,其化学式可表示为___________ (以n表示硼原子的个数);___________ 。
(5)立方 和立方
和立方 均为共价晶体,结构相似,
均为共价晶体,结构相似, 的熔点高于
的熔点高于 的原因是
的原因是___________ 。
(6)一种新型轻质储氢材料的晶胞结构如图所示,设阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
 )和锰(
)和锰( )形成的物质在生产、生活中应用广泛。回答下列问题:
)形成的物质在生产、生活中应用广泛。回答下列问题:(1)基态
 原子核外电子排布式为
原子核外电子排布式为(2)
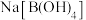 可用于织物漂白。
可用于织物漂白。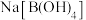 的化学键除了共价键外,还存在
的化学键除了共价键外,还存在(3)
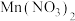 工业制备中常用的催化剂,
工业制备中常用的催化剂,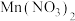 中阴离子的空间构型为
中阴离子的空间构型为(4)如图1表示偏硼酸根的一种无限长的链式结构,其化学式可表示为
(5)立方
 和立方
和立方 均为共价晶体,结构相似,
均为共价晶体,结构相似, 的熔点高于
的熔点高于 的原因是
的原因是(6)一种新型轻质储氢材料的晶胞结构如图所示,设阿伏加德罗常数的值为
 ,该晶体的密度为
,该晶体的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
3 . 近期我国科学家报道了一种低成本高储能液流电池,其工作原理如下图。下列说法中错误的是
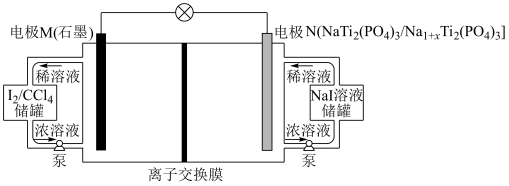
| A.电极M为正极 |
| B.离子交换膜应选用阳离子交换膜 |
C.电极N上发生反应的电极反应为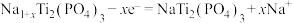 |
D.理论上N电极质量减少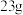 ,电路中转移的电子数目为 ,电路中转移的电子数目为 |
您最近一年使用:0次
2024-06-12更新
|
138次组卷
|
2卷引用:2024届陕西省部分学校高三下学期5月份高考适应性考试理科综合试题-高中化学
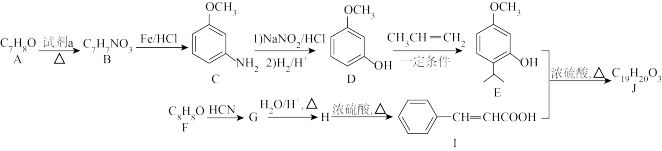
4 . 一种新型药物的中间体J的一种合成路线如图所示。 ;
;
(1)F的化学名称为___________ ;B中所含官能团名称为___________ 。
(2)H的分子式为___________ ;试剂a为___________ ;D→E的反应类型为___________ 。
(3)试写出E+I→J反应的化学方程式:___________ 。
(4)物质B的同分异构体有多种,符合下列条件的同分异构体共有___________ 种(不考虑立体异构),其中,分子中有4种不同化学环境的氢,且氢原子数目比为1:2:2:2的同分异构体的结构简式为___________ 。
①遇 溶液显紫色;②分子中含有
溶液显紫色;②分子中含有 官能团。
官能团。
(5)写出以 为原料合成乳酸(
为原料合成乳酸(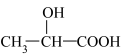 )的路线(其他试剂任选):
)的路线(其他试剂任选):___________ 。
 ;
;②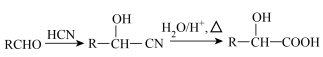 。
。
(1)F的化学名称为
(2)H的分子式为
(3)试写出E+I→J反应的化学方程式:
(4)物质B的同分异构体有多种,符合下列条件的同分异构体共有
①遇
 溶液显紫色;②分子中含有
溶液显紫色;②分子中含有 官能团。
官能团。(5)写出以
 为原料合成乳酸(
为原料合成乳酸(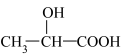 )的路线(其他试剂任选):
)的路线(其他试剂任选):
您最近一年使用:0次
解题方法
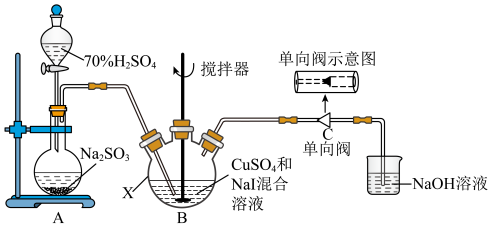
5 . 碘化亚铜(CuI)可用作有机合成催化剂,是一种白色粉末,不溶于水,在空气中相对稳定。实验室制备碘化亚铜的装置如图(部分夹持及加热装置已略去):
I.取50.0g 、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
Ⅱ.打开分液漏斗,将A中产生的 通向B中的黄色沉淀,充分反应后得到白色沉淀;
通向B中的黄色沉淀,充分反应后得到白色沉淀;
Ⅲ.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
Ⅳ.测定产品中CuI的纯度。
回答下列问题:
(1)在使用分液漏斗组装发生装置之前,必需进行的操作是___________ 。仪器X的名称是___________ 。
(2)已知步骤I中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为___________ 。
(3)步骤Ⅱ通入 的主要目的是
的主要目的是___________ 。写出通入 所发生的离子反应方程式
所发生的离子反应方程式___________ 。
(4)下图中能起到与单向阀C相同作用的是___________ (填字母)。(下图容器中未标注的液体均为氢氧化钠溶液) 浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为
浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为 并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为___________ %,据此推算CuI的产率接近于___________ (填字母)。
I.取50.0g
 、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
、80.0gNaI于仪器X中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;Ⅱ.打开分液漏斗,将A中产生的
 通向B中的黄色沉淀,充分反应后得到白色沉淀;
通向B中的黄色沉淀,充分反应后得到白色沉淀;Ⅲ.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
Ⅳ.测定产品中CuI的纯度。
回答下列问题:
(1)在使用分液漏斗组装发生装置之前,必需进行的操作是
(2)已知步骤I中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为
(3)步骤Ⅱ通入
 的主要目的是
的主要目的是 所发生的离子反应方程式
所发生的离子反应方程式(4)下图中能起到与单向阀C相同作用的是

 浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为
浓度在一定范围内的关系如图。取0.1mgCuI粗产品,经预处理,将其中Cu元素全部转化为 并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
并定容至1L。取样1mL测得荧光强度比值为10.7,则产品中CuI的纯度为
您最近一年使用:0次
6 . 25℃时,向一定浓度的 溶液中滴加NaOH溶液,混合液中
溶液中滴加NaOH溶液,混合液中 随pOH的变化如图所示,下列说法错误的是
随pOH的变化如图所示,下列说法错误的是 中x表示
中x表示 、
、 、
、 ;
;
② 。
。
 溶液中滴加NaOH溶液,混合液中
溶液中滴加NaOH溶液,混合液中 随pOH的变化如图所示,下列说法错误的是
随pOH的变化如图所示,下列说法错误的是
 中x表示
中x表示 、
、 、
、 ;
;②
 。
。A.曲线III表示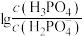 随pOH的变化关系 随pOH的变化关系 |
B.M点时,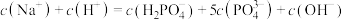 |
C.当溶液 时, 时, |
D. 的平衡常数为 的平衡常数为 |
您最近一年使用:0次
7 . CO2的转化和利用是实现碳中和的有效途径,其中CO2转化为CH3OH被认为是最可能利用的路径,该路径涉及反应如下:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.01kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.01kJ•mol-1
反应II:CO2(g)+H2(g) CO(g)+H2O(g) △H2>0
CO(g)+H2O(g) △H2>0
请回答下列问题:
(1)若利用反应I计算反应II的反应热△H2,还需要知道一个化学反应的△H,写出该反应的化学方程式_______ 。
(2)在催化剂条件下,反应I的反应机理和相对能量变化如图1(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。_______ 。
(3)在恒温恒压(260℃,1.8MPa)下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如表。
已知:
i.分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;
ii.CH3OH的选择性=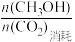 ×100%
×100%
①在普通反应器(A)中,下列能作为反应I和反应II均达到平衡状态的判断判据是_______ (填字母)。
A.气体压强不再变化
B.气体的密度不再改变
C.v正(CO2)=3v逆(H2)
D.各物质浓度比不再改变
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是_______ ;在反应器(B)中,CO2的平衡转化率明显高于反应器(A),可能的原因是______ 。
③若反应器(A)中初始时n(CO2)=1mol,反应I从开始到平衡态的平均反应速率v(CH3OH)=_______ mol•s-1;反应II的化学平衡常数Kp(II)=_______ (列出化简后的计算式即可)。
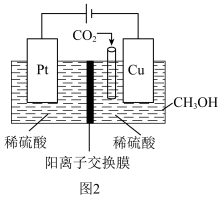
(4)近年来,有研究人员用CO2通过电催化生成CH3OH,实现CO2的回收利用,其工作原理如图2所示,请写出Cu电极上的电极反应:_______ 。
反应I:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.01kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.01kJ•mol-1反应II:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2>0
CO(g)+H2O(g) △H2>0请回答下列问题:
(1)若利用反应I计算反应II的反应热△H2,还需要知道一个化学反应的△H,写出该反应的化学方程式
(2)在催化剂条件下,反应I的反应机理和相对能量变化如图1(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
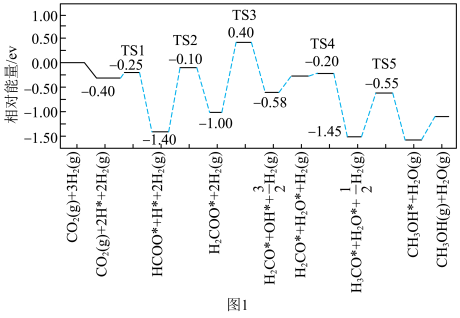
(3)在恒温恒压(260℃,1.8MPa)下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如表。
| 反应器 | CO2平衡转化率 | 甲醇的选择性 | 达到平衡时间/s |
| 普通反应器(A) | 25.0% | 80.0% | 10.0 |
| 分子筛膜催化反应器(B) | >25.0% | 100.0% | 8.0 |
i.分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;
ii.CH3OH的选择性=
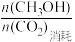 ×100%
×100%①在普通反应器(A)中,下列能作为反应I和反应II均达到平衡状态的判断判据是
A.气体压强不再变化
B.气体的密度不再改变
C.v正(CO2)=3v逆(H2)
D.各物质浓度比不再改变
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是
③若反应器(A)中初始时n(CO2)=1mol,反应I从开始到平衡态的平均反应速率v(CH3OH)=
(4)近年来,有研究人员用CO2通过电催化生成CH3OH,实现CO2的回收利用,其工作原理如图2所示,请写出Cu电极上的电极反应:
您最近一年使用:0次
2024-06-06更新
|
117次组卷
|
2卷引用:2024届陕西省渭南市临渭区高三下学期三模理综试题-高中化学
名校
解题方法
8 . 钴酸锂( )常用作锂离子电池的正极材料。以某卤水(含浓度较大的LiCl、少量
)常用作锂离子电池的正极材料。以某卤水(含浓度较大的LiCl、少量 、
、 、
、 等)为原料制备
等)为原料制备 并获得金属Mg副产品的一种工艺流程如图所示:
并获得金属Mg副产品的一种工艺流程如图所示:
① 的溶解度随温度升高而降低。
的溶解度随温度升高而降低。
②常温下,几种难溶物质的溶度积数据如下表所示。
回答下列问题:
(1)某小组同学利用右图装置进行“除杂1”相关操作,装置图中有一处不符合操作规范,该不规范之处是指_________________ 。
____________  。若“蒸发浓缩”步骤在实验室中进行,使用的硅酸盐仪器除了酒精灯之外,还需要
。若“蒸发浓缩”步骤在实验室中进行,使用的硅酸盐仪器除了酒精灯之外,还需要_________________ 。
(3)“洗涤” 固体时最好选用
固体时最好选用__________ (填“热水”或“冷水”),检验 否洗涤干净的操作是
否洗涤干净的操作是_____________________ 。
(4)高温下,“合成”反应的化学方程式为_____________________ 。
(5) 固体“溶解”后经过“一系列操作”,可以得到
固体“溶解”后经过“一系列操作”,可以得到 晶体,则“一系列操作”为
晶体,则“一系列操作”为___________________ 。
(6)“脱水”时加入 能抑制
能抑制 的水解,原因是
的水解,原因是_________________ 。
 )常用作锂离子电池的正极材料。以某卤水(含浓度较大的LiCl、少量
)常用作锂离子电池的正极材料。以某卤水(含浓度较大的LiCl、少量 、
、 、
、 等)为原料制备
等)为原料制备 并获得金属Mg副产品的一种工艺流程如图所示:
并获得金属Mg副产品的一种工艺流程如图所示: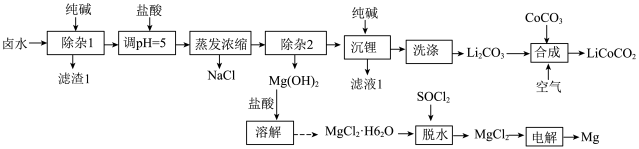
①
 的溶解度随温度升高而降低。
的溶解度随温度升高而降低。②常温下,几种难溶物质的溶度积数据如下表所示。
物质 |
|
|
|
|
|
室温下 |
|
|
|
|
|
(1)某小组同学利用右图装置进行“除杂1”相关操作,装置图中有一处不符合操作规范,该不规范之处是指
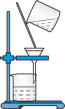

 。若“蒸发浓缩”步骤在实验室中进行,使用的硅酸盐仪器除了酒精灯之外,还需要
。若“蒸发浓缩”步骤在实验室中进行,使用的硅酸盐仪器除了酒精灯之外,还需要(3)“洗涤”
 固体时最好选用
固体时最好选用 否洗涤干净的操作是
否洗涤干净的操作是(4)高温下,“合成”反应的化学方程式为
(5)
 固体“溶解”后经过“一系列操作”,可以得到
固体“溶解”后经过“一系列操作”,可以得到 晶体,则“一系列操作”为
晶体,则“一系列操作”为(6)“脱水”时加入
 能抑制
能抑制 的水解,原因是
的水解,原因是
您最近一年使用:0次
2024-06-06更新
|
46次组卷
|
2卷引用:2024届陕西省铜川市王益中学高三下学期模拟预测理综试题-高中化学
名校
解题方法
9 . 四氯化碳( )主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
)主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
① 与溴水反应生成硫酸和氢溴酸等,可用溴水吸收
与溴水反应生成硫酸和氢溴酸等,可用溴水吸收 ;
;
② 与
与 在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
③硫单质的沸点445℃, 的沸点46.5℃,
的沸点46.5℃, 沸点76.8℃、密度1.6
沸点76.8℃、密度1.6 。
。
回答下列问题:
(1)装置A中仪器a的名称是___________ ,用浓盐酸与 反应制取
反应制取 ,发生反应的离子方程式为
,发生反应的离子方程式为____________ (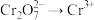 )。
)。
(2)装置的连接顺序为___________ 。
A→_______→________→_______→_____→E。
(3)为使冷凝效果较好,应选用的冷凝管为_______ (填编号);装置C中冷凝管的作用是____________ ,冷水从_________ 口通入。 、
、 ,此时装置F的作用为
,此时装置F的作用为_________________ 。
(5)反应一段时间后,装置C中出现淡黄色固体,写出装置C中发生反应的化学方程式:_________ 。
(6)装置C中反应结束后,先过滤除去固体_________ (填名称),再经过_________ (填操作名称)可得到 。
。
 )主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。
)主要用作优良的溶剂、灭火剂、制冷剂、萃取剂等。某化学小组模拟工业原理,用二硫化碳与氯气反应制取四氯化碳,所用实验各部分装置如下图所示(部分夹持仪器、加热装置已省略)。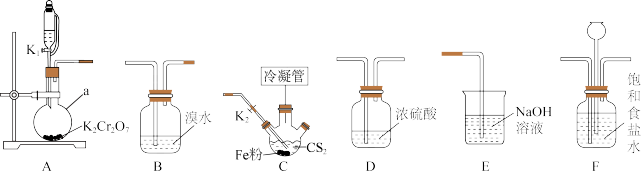
①
 与溴水反应生成硫酸和氢溴酸等,可用溴水吸收
与溴水反应生成硫酸和氢溴酸等,可用溴水吸收 ;
;②
 与
与 在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;
在铁作催化剂的条件下,在装置C中(85~95℃)反应可生成四氯化碳;③硫单质的沸点445℃,
 的沸点46.5℃,
的沸点46.5℃, 沸点76.8℃、密度1.6
沸点76.8℃、密度1.6 。
。回答下列问题:
(1)装置A中仪器a的名称是
 反应制取
反应制取 ,发生反应的离子方程式为
,发生反应的离子方程式为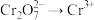 )。
)。(2)装置的连接顺序为
A→_______→________→_______→_____→E。
(3)为使冷凝效果较好,应选用的冷凝管为

 、
、 ,此时装置F的作用为
,此时装置F的作用为(5)反应一段时间后,装置C中出现淡黄色固体,写出装置C中发生反应的化学方程式:
(6)装置C中反应结束后,先过滤除去固体
 。
。
您最近一年使用:0次
2024-06-06更新
|
77次组卷
|
2卷引用:2024届陕西省铜川市王益中学高三下学期模拟预测理综试题-高中化学
名校
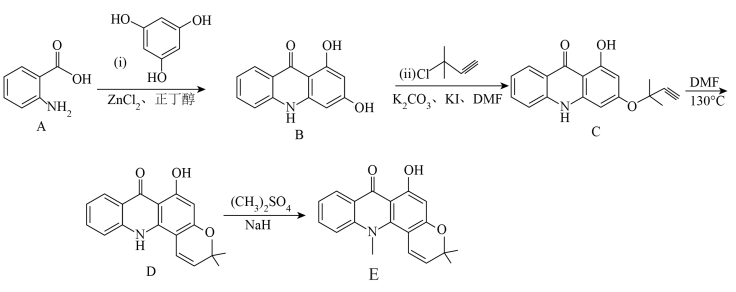
10 . 有机物E是一种广谱抗癌药,一种合成路线如下:
(1)A中所含官能团的名称是_____ 。
(2)B→C中 的作用是
的作用是_____ 。D→E的反应类型是_____ 。
(3)1moli与足量溴水反应,最多消耗_____ 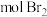 。
。
(4)写出A→B的化学方程式:_____ 。
(5)在A的芳香族同分异构体中,苯环上直接连—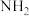 且能发生银镜反应的物质有
且能发生银镜反应的物质有_____ 种(不考虑立体异构),其中核磁共振氢谱上有四组峰且峰面积比为1:2:2:2的结构简式为_____ 。
(6)设计以苯酚和1,3-丁二烯为原料合成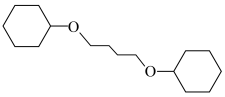 的路线
的路线_____ (其他试剂任选)。
(1)A中所含官能团的名称是
(2)B→C中
 的作用是
的作用是(3)1moli与足量溴水反应,最多消耗
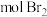 。
。(4)写出A→B的化学方程式:
(5)在A的芳香族同分异构体中,苯环上直接连—
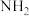 且能发生银镜反应的物质有
且能发生银镜反应的物质有(6)设计以苯酚和1,3-丁二烯为原料合成
 的路线
的路线
您最近一年使用:0次
2024-06-04更新
|
149次组卷
|
2卷引用:2024届陕西省安康市高新中学高三下学期5月模拟预测理综试题-高中化学