解题方法
1 . 某工厂通过如下装置处理两个车间的废气(电极均为惰性电极),既处理了污染物,又变废为宝。下列说法正确的是
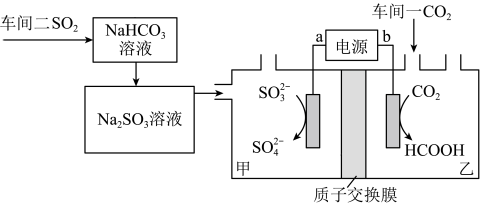
A.电极电势: |
B.工作时 由乙池移向甲池 由乙池移向甲池 |
C.通电一段时间后甲区域的 增大 增大 |
D.阴极反应式: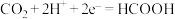 |
您最近一年使用:0次
解题方法
2 . 下列有关实验的离子方程式正确的是
A.将少量 加入蒸馏水中: 加入蒸馏水中: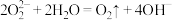 |
B.将铁粉加入足量稀硫酸中: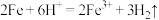 |
C.将 加入过量氢碘酸中: 加入过量氢碘酸中: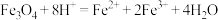 |
D.将少量 溶液加入 溶液加入 溶液中: 溶液中: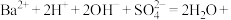 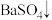 |
您最近一年使用:0次
解题方法
3 . 烯烃的加氢甲酰化反应是醛合成中重要的均相催化工业反应之一。我国科学家利用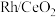 催化剂实现烯烃甲酰化。回答下列问题:
催化剂实现烯烃甲酰化。回答下列问题: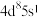 ,位于周期表第五周期第
,位于周期表第五周期第_____ 族,位于_____ 区。
(2)基态O原子核外电子有_____ 种不同的空间运动状态。
(3)乙中C原子的杂化类型是_____ 。
(4)丙分子中所含元素电负性由大到小顺序为_____ 。丙分子有_____ 个手性碳原子。
(5)已知: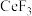 、
、 的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是
的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是_____ 。
(6) 的立方晶胞结构如图所示。已知
的立方晶胞结构如图所示。已知 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为 。
。_____ 。该晶体密度为_____  。
。
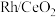 催化剂实现烯烃甲酰化。回答下列问题:
催化剂实现烯烃甲酰化。回答下列问题: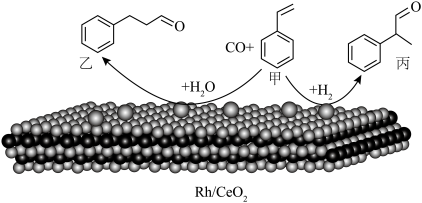
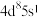 ,位于周期表第五周期第
,位于周期表第五周期第(2)基态O原子核外电子有
(3)乙中C原子的杂化类型是
(4)丙分子中所含元素电负性由大到小顺序为
(5)已知:
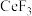 、
、 的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是
的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是(6)
 的立方晶胞结构如图所示。已知
的立方晶胞结构如图所示。已知 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为 。
。
 。
。
您最近一年使用:0次
4 . 室温下,用 的二甲胺
的二甲胺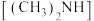 溶液(二甲胺在水中的电离与一水合氨相似)滴定
溶液(二甲胺在水中的电离与一水合氨相似)滴定 盐酸溶液。溶液
盐酸溶液。溶液 随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
 的二甲胺
的二甲胺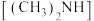 溶液(二甲胺在水中的电离与一水合氨相似)滴定
溶液(二甲胺在水中的电离与一水合氨相似)滴定 盐酸溶液。溶液
盐酸溶液。溶液 随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是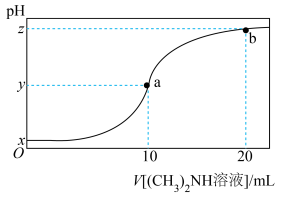
| A.x=1,y=7 |
B.a、b两点的溶液中, 不相等 不相等 |
| C.本实验应该选择酚酞作指示剂 |
D.b点溶液中存在: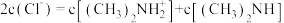 |
您最近一年使用:0次
名校
解题方法
5 .  在生物学、医学等领域有重要应用,传统制氢成本高、技术复杂,研究新型制氢意义重大,已成为科学家研究的重要课题。回答下列问题:
在生物学、医学等领域有重要应用,传统制氢成本高、技术复杂,研究新型制氢意义重大,已成为科学家研究的重要课题。回答下列问题:
(1)我国科学家发现,Rh催化单分子甲酸分解制 的过程如图1所示,其中带“*”的物种表示吸附在Rh表面,该反应过程中决定反应速率步骤的化学方程式为
的过程如图1所示,其中带“*”的物种表示吸附在Rh表面,该反应过程中决定反应速率步骤的化学方程式为___________ ;甲酸分解制 的热化学方程式可表示为
的热化学方程式可表示为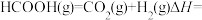
_______  (下图为单分子甲酸分解相对能量变化,能量单位为eV,阿伏加德罗常数用
(下图为单分子甲酸分解相对能量变化,能量单位为eV,阿伏加德罗常数用 表示)。
表示)。 可直接分解制取
可直接分解制取 ,反应的原理如下:
,反应的原理如下: 。实际生产中向刚性容器中同时通入
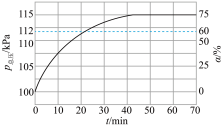
。实际生产中向刚性容器中同时通入 和水蒸气,水蒸气与反应体系的任何物质均不发生反应,测得容器总压(
和水蒸气,水蒸气与反应体系的任何物质均不发生反应,测得容器总压(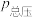 )和
)和 的转化率(α)随时间的变化关系如图所示。计算反应在0~20min内的平均反应速率
的转化率(α)随时间的变化关系如图所示。计算反应在0~20min内的平均反应速率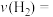
_____  ;平衡时,
;平衡时,
_____ kPa,平衡常数
_____ kPa,(Kp为以分压表示的平衡常数)。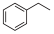 )气体催化脱氢法制取
)气体催化脱氢法制取 ,同时生成苯乙烯(
,同时生成苯乙烯(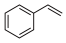 )气体。其他条件不变时,在不同催化剂(n、m、p)作用下,反应进行相同时间后,乙苯的转化率随反应温度的变化如图所示。相同温度下,三种催化剂(n、m、p)的催化活性由高到低的顺序为
)气体。其他条件不变时,在不同催化剂(n、m、p)作用下,反应进行相同时间后,乙苯的转化率随反应温度的变化如图所示。相同温度下,三种催化剂(n、m、p)的催化活性由高到低的顺序为___________ ;b点乙苯的转化率高于a点的原因是___________ 。
 在生物学、医学等领域有重要应用,传统制氢成本高、技术复杂,研究新型制氢意义重大,已成为科学家研究的重要课题。回答下列问题:
在生物学、医学等领域有重要应用,传统制氢成本高、技术复杂,研究新型制氢意义重大,已成为科学家研究的重要课题。回答下列问题:(1)我国科学家发现,Rh催化单分子甲酸分解制
 的过程如图1所示,其中带“*”的物种表示吸附在Rh表面,该反应过程中决定反应速率步骤的化学方程式为
的过程如图1所示,其中带“*”的物种表示吸附在Rh表面,该反应过程中决定反应速率步骤的化学方程式为 的热化学方程式可表示为
的热化学方程式可表示为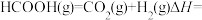
 (下图为单分子甲酸分解相对能量变化,能量单位为eV,阿伏加德罗常数用
(下图为单分子甲酸分解相对能量变化,能量单位为eV,阿伏加德罗常数用 表示)。
表示)。
 可直接分解制取
可直接分解制取 ,反应的原理如下:
,反应的原理如下: 。实际生产中向刚性容器中同时通入
。实际生产中向刚性容器中同时通入 和水蒸气,水蒸气与反应体系的任何物质均不发生反应,测得容器总压(
和水蒸气,水蒸气与反应体系的任何物质均不发生反应,测得容器总压(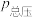 )和
)和 的转化率(α)随时间的变化关系如图所示。计算反应在0~20min内的平均反应速率
的转化率(α)随时间的变化关系如图所示。计算反应在0~20min内的平均反应速率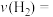
 ;平衡时,
;平衡时,

 )气体催化脱氢法制取
)气体催化脱氢法制取 ,同时生成苯乙烯(
,同时生成苯乙烯( )气体。其他条件不变时,在不同催化剂(n、m、p)作用下,反应进行相同时间后,乙苯的转化率随反应温度的变化如图所示。相同温度下,三种催化剂(n、m、p)的催化活性由高到低的顺序为
)气体。其他条件不变时,在不同催化剂(n、m、p)作用下,反应进行相同时间后,乙苯的转化率随反应温度的变化如图所示。相同温度下,三种催化剂(n、m、p)的催化活性由高到低的顺序为
您最近一年使用:0次
解题方法
6 . 利用电解法将污染性气体 转化为
转化为 溶液的原理如图所示。下列说法错误的是
溶液的原理如图所示。下列说法错误的是
 转化为
转化为 溶液的原理如图所示。下列说法错误的是
溶液的原理如图所示。下列说法错误的是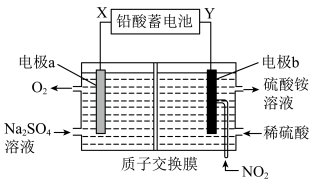
A.电解时,当有2mol 透过质子交换膜,则电极Y增重96g 透过质子交换膜,则电极Y增重96g |
B. 在电极b上的反应式为 在电极b上的反应式为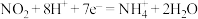 |
C.电解过程中, 由a极区向b极区迁移 由a极区向b极区迁移 |
D.电解时 溶液的浓度保持不变 溶液的浓度保持不变 |
您最近一年使用:0次
7 . 铬、钛、钴都属于过渡元素。
(1)铬元素属于元素周期表的___________ 区,基态Cr有___________ 个未成对电子。在同周期的基态原子中,与Cr的最高能层电子数相同的还有___________ (填元素符号)。
(2)铬与钛都可形成+3价的金属氯化物, 的熔点为1300℃、
的熔点为1300℃、 的熔点为440℃,二者的熔点相差较大的原因可能是
的熔点为440℃,二者的熔点相差较大的原因可能是___________ 。
(3) 可形成配合物
可形成配合物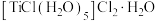 ,其配位原子是
,其配位原子是___________ 。(用化学符号表示),该配合物中含有的化学键类型有___________ (填字母)。
A.离子键 B.非极性键 C.配位键 D.金属键
(4)钴的某种配合物的化学式为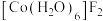 ,该配合物的立方晶胞如图所示,其晶胞参数为apm。
,该配合物的立方晶胞如图所示,其晶胞参数为apm。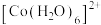 最近的
最近的 有
有___________ 个。
②设阿伏加德罗常数的值为 ,则
,则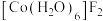 晶体的密度为
晶体的密度为___________  。
。
(1)铬元素属于元素周期表的
(2)铬与钛都可形成+3价的金属氯化物,
 的熔点为1300℃、
的熔点为1300℃、 的熔点为440℃,二者的熔点相差较大的原因可能是
的熔点为440℃,二者的熔点相差较大的原因可能是(3)
 可形成配合物
可形成配合物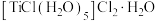 ,其配位原子是
,其配位原子是A.离子键 B.非极性键 C.配位键 D.金属键
(4)钴的某种配合物的化学式为
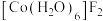 ,该配合物的立方晶胞如图所示,其晶胞参数为apm。
,该配合物的立方晶胞如图所示,其晶胞参数为apm。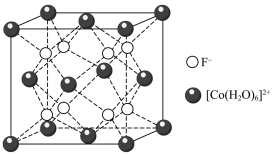
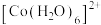 最近的
最近的 有
有②设阿伏加德罗常数的值为
 ,则
,则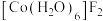 晶体的密度为
晶体的密度为 。
。
您最近一年使用:0次
8 . 氮化镁用途广泛,常用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其他元素的氮化物时作为催化剂。第一次成功合成立方氮化硼时,使用的催化剂就是氮化镁。实验室可用如图装置制取 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。___________ 。
(2)装置C中氧化铜的作用是氧化氨气制取 ,其反应的化学方程式为
,其反应的化学方程式为___________ 。
(3)装置D的作用是___________ 。
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是___________ 。
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为___________ ,固体试剂X可以为___________ (填字母)。
(6)实验室还可用 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为___________ 。___________ 。
 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。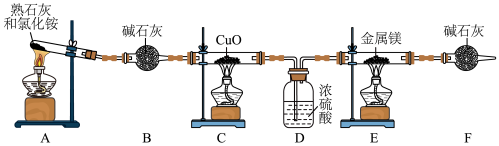
(2)装置C中氧化铜的作用是氧化氨气制取
 ,其反应的化学方程式为
,其反应的化学方程式为(3)装置D的作用是
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为
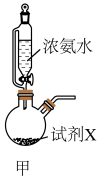
(6)实验室还可用
 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为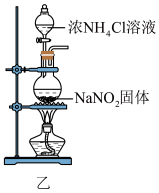
您最近一年使用:0次
9 . 下列实验中,由实验现象得出的结论正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向 溶液中通入足量的 溶液中通入足量的 | 生成淡黄色沉淀 |  不溶于盐酸 不溶于盐酸 |
| B | 少量 粉加到 粉加到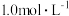 的 的 溶液中 溶液中 | 溶液颜色变浅 | 金属 比Fe活泼 比Fe活泼 |
| C | 向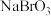 溶液中滴入1滴新制氯水 溶液中滴入1滴新制氯水 | 溶液变橙色 | 氧化性: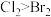 |
| D | 向浓度均为 的 的 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液 溶液 | 仅出现浅蓝色沉淀 |  的溶度积比 的溶度积比 的小 的小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 科技飞速发展,无人驾驶逐渐进入生活。下列无人驾驶车所使用材料属于合金的是
|
|
| A.车轮毂 | B.车轮胎 |
|
|
| C.聚氨酯内装饰 | D.车润滑油 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次







