名校
解题方法
1 . 高分子M广泛用于牙膏、牙科粘合剂等口腔护理产品,合成路线如图:
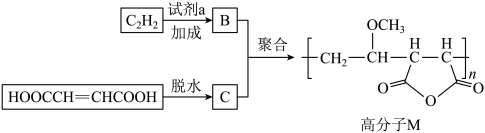
| A.试剂a是甲醇 | B.合成M的反应类型是缩聚反应 |
| C.第一电离能大小顺序为:O>H>C | D.化合物C中碳和氧原子均采用 杂化 杂化 |
您最近一年使用:0次
2 . 一种太空生命保障系统利用电解水供氧,生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,水可循环使用。
(1)已知 与
与 的燃烧热分别为
的燃烧热分别为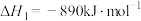 ,
, ;
;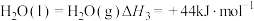 ,写出
,写出 与
与 生成
生成 和
和 的热化学方程式
的热化学方程式_________________ 。
(2)一定温度下,在恒容密闭容器中 与
与 反应生成
反应生成 和
和 。
。
①能说明该反应达到平衡状态的是_________________ (填字母)。
A. B.容器内压强一定
B.容器内压强一定
C.气体平均相对分子质量一定 D.混合气体密度一定
②已知容器的容积为 ,初始加入
,初始加入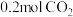 ,和
,和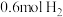 ,反应平衡后测得
,反应平衡后测得 的转化率为
的转化率为 ,则该反应的平衡常数为
,则该反应的平衡常数为_________________ 。
③温度不变,往②平衡状态中再加入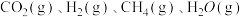 各
各 ,则此时反应速率
,则此时反应速率
_________________ 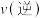 。(填“
。(填“ ”“
”“ ”或“
”或“ ")
")
(3)工业上在一定条件下利用 与
与 可直接合成有机中间体二甲醚:
可直接合成有机中间体二甲醚: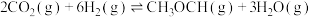 。
。
当 时,实验测得
时,实验测得 的平衡转化率随温度及压强变化如图所示:
的平衡转化率随温度及压强变化如图所示:
_________________ (填“ ”或“
”或“ ”)0。
”)0。
②图中压强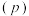 由大到小的顺序是
由大到小的顺序是_________________ 。
(1)已知
 与
与 的燃烧热分别为
的燃烧热分别为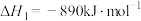 ,
, ;
;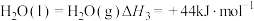 ,写出
,写出 与
与 生成
生成 和
和 的热化学方程式
的热化学方程式(2)一定温度下,在恒容密闭容器中
 与
与 反应生成
反应生成 和
和 。
。①能说明该反应达到平衡状态的是
A.
 B.容器内压强一定
B.容器内压强一定C.气体平均相对分子质量一定 D.混合气体密度一定
②已知容器的容积为
 ,初始加入
,初始加入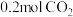 ,和
,和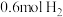 ,反应平衡后测得
,反应平衡后测得 的转化率为
的转化率为 ,则该反应的平衡常数为
,则该反应的平衡常数为③温度不变,往②平衡状态中再加入
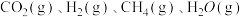 各
各 ,则此时反应速率
,则此时反应速率
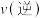 。(填“
。(填“ ”“
”“ ”或“
”或“ ")
")(3)工业上在一定条件下利用
 与
与 可直接合成有机中间体二甲醚:
可直接合成有机中间体二甲醚: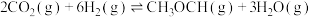 。
。当
 时,实验测得
时,实验测得 的平衡转化率随温度及压强变化如图所示:
的平衡转化率随温度及压强变化如图所示: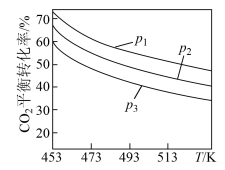

 ”或“
”或“ ”)0。
”)0。②图中压强
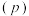 由大到小的顺序是
由大到小的顺序是
您最近一年使用:0次
3 . 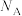 阿伏加德罗常数的值,下列说法正确的是
阿伏加德罗常数的值,下列说法正确的是
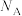 阿伏加德罗常数的值,下列说法正确的是
阿伏加德罗常数的值,下列说法正确的是A.常温下,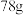  含有 含有 键的数目为 键的数目为 |
B.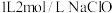 水溶液中阴离子数目之和为 水溶液中阴离子数目之和为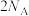 |
C.铁片上镀铜,阴极增重 时,理论上外电路转移电子数为 时,理论上外电路转移电子数为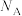 |
D.标准状况下, 和 和 混合气中含有的分子数为 混合气中含有的分子数为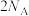 |
您最近一年使用:0次
解题方法
4 . 工业上,常用离子交换法软化自来水,其原理是 ,
, 。常温下,向一定体积的自来水中加入离子交换树脂
。常温下,向一定体积的自来水中加入离子交换树脂 ,测得自来水中
,测得自来水中 变化如图所示。下列叙述正确的是
变化如图所示。下列叙述正确的是
 ,
, 。常温下,向一定体积的自来水中加入离子交换树脂
。常温下,向一定体积的自来水中加入离子交换树脂 ,测得自来水中
,测得自来水中 变化如图所示。下列叙述正确的是
变化如图所示。下列叙述正确的是
A.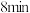 时加入少量 时加入少量 固体,离子交换反应平衡常数减小 固体,离子交换反应平衡常数减小 |
B.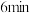 时的逆反应速率大于 时的逆反应速率大于 时的逆反应速率 时的逆反应速率 |
C.其他条件不变时, 时离子交换反应已停止 时离子交换反应已停止 |
D.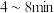 内平均反应速率: 内平均反应速率: |
您最近一年使用:0次
名校
5 . 琥珀酸(丁二酸,简记为 )为二元弱酸。常温下,在含
)为二元弱酸。常温下,在含 和
和 的混合液中滴加
的混合液中滴加 溶液,溶液
溶液,溶液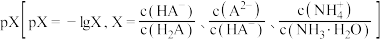 与
与 的关系如图所示。
的关系如图所示。
 )为二元弱酸。常温下,在含
)为二元弱酸。常温下,在含 和
和 的混合液中滴加
的混合液中滴加 溶液,溶液
溶液,溶液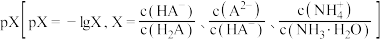 与
与 的关系如图所示。
的关系如图所示。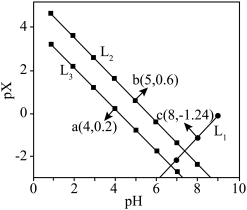
A.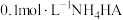 溶液中: 溶液中: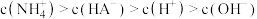 |
B.当 时, 时,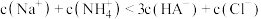 |
C.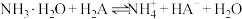 的平衡常数K小于 的平衡常数K小于 |
D. 和 和 直线交点坐标为(7.42,-1.82) 直线交点坐标为(7.42,-1.82) |
您最近一年使用:0次
名校
6 . 设 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.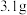 白磷( 白磷( ,正四面体结构)中含有 ,正四面体结构)中含有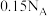 个 个 键 键 |
B. 氧气在充分反应过程中,转移的电子数目一定为 氧气在充分反应过程中,转移的电子数目一定为 |
C.标准状况下,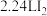 与 与 充分反应,生成的 充分反应,生成的 分子数目为 分子数目为 |
D.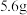 铁粉与 铁粉与 的硝酸充分反应,产生的 的硝酸充分反应,产生的 分子数目为 分子数目为 |
您最近一年使用:0次
2024-05-31更新
|
120次组卷
|
2卷引用:2024届海南省琼海市嘉积中学高三下学期模拟预测化学试题
名校
7 . 已知X、Y、Z、W为元素周期表中原子序数依次增大的前20号主族元素,X元素的某种核素能测定文物年代,Y元素原子最外层电子数是内层电子总数的3倍,Z元素原子最外层电子数比内层电子数之和少3,W元素原子最外层电子数和最内层电子数相等。下列说法正确的是
A.简单离子的半径: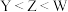 |
B.最高价氧化物对应水化物的酸性: |
C. 中既含有离子键又含有非极性键 中既含有离子键又含有非极性键 |
D. 是极性分子 是极性分子 |
您最近一年使用:0次
名校
解题方法
8 . 过硫酸铵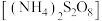 也称过二硫酸铵,常用作食品保存剂、氧化剂以及高分子聚合物的引发剂,见光易分解,易溶于水,微溶于乙醇。用30%双氧水、浓硫酸和氨气加热至
也称过二硫酸铵,常用作食品保存剂、氧化剂以及高分子聚合物的引发剂,见光易分解,易溶于水,微溶于乙醇。用30%双氧水、浓硫酸和氨气加热至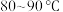 制备过硫酸铵的装置如图所示。
制备过硫酸铵的装置如图所示。
(1)每个过硫酸铵(S元素的化合价为+6价)中含有过氧键个数为___________ 。
(2)仪器的连接顺序为
___________ (用小写字母连接)。
(3)盛放浓硫酸的仪器名称为___________ 。装置A中 的作用是
的作用是___________ 。过硫酸铵保存在棕色试剂瓶中的原因是___________ 。
(4)A中制取过硫酸铵的反应的化学方程式为___________ 。充分反应后,将A中混合液经一系列操作得到晶体,然后用无水乙醇洗涤。选择用无水乙醇洗涤的目的是___________ 。
(5)过硫酸铵可用于测定锰钢中 元素的含量:取
元素的含量:取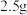 锰钢样品,加入过量浓硝酸,在加热条件下将
锰钢样品,加入过量浓硝酸,在加热条件下将 溶出形成
溶出形成 ,再用
,再用 过硫酸铵溶液恰好将溶出的
过硫酸铵溶液恰好将溶出的 全部转化为
全部转化为 ,通过检测
,通过检测 的浓度得出样品中
的浓度得出样品中 元素的质量分数为54%,则
元素的质量分数为54%,则
___________ (保留两位小数)。
(6)根据本实验可得出, 的氧化性从大到小的顺序为
的氧化性从大到小的顺序为___________ 。
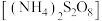 也称过二硫酸铵,常用作食品保存剂、氧化剂以及高分子聚合物的引发剂,见光易分解,易溶于水,微溶于乙醇。用30%双氧水、浓硫酸和氨气加热至
也称过二硫酸铵,常用作食品保存剂、氧化剂以及高分子聚合物的引发剂,见光易分解,易溶于水,微溶于乙醇。用30%双氧水、浓硫酸和氨气加热至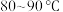 制备过硫酸铵的装置如图所示。
制备过硫酸铵的装置如图所示。
(1)每个过硫酸铵(S元素的化合价为+6价)中含有过氧键个数为
(2)仪器的连接顺序为

(3)盛放浓硫酸的仪器名称为
 的作用是
的作用是(4)A中制取过硫酸铵的反应的化学方程式为
(5)过硫酸铵可用于测定锰钢中
 元素的含量:取
元素的含量:取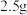 锰钢样品,加入过量浓硝酸,在加热条件下将
锰钢样品,加入过量浓硝酸,在加热条件下将 溶出形成
溶出形成 ,再用
,再用 过硫酸铵溶液恰好将溶出的
过硫酸铵溶液恰好将溶出的 全部转化为
全部转化为 ,通过检测
,通过检测 的浓度得出样品中
的浓度得出样品中 元素的质量分数为54%,则
元素的质量分数为54%,则
(6)根据本实验可得出,
 的氧化性从大到小的顺序为
的氧化性从大到小的顺序为
您最近一年使用:0次
9 . 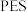 材料在生产、生活中有广泛应用。环氧乙烷合成
材料在生产、生活中有广泛应用。环氧乙烷合成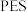 的原理如图所示:
的原理如图所示:
 材料在生产、生活中有广泛应用。环氧乙烷合成
材料在生产、生活中有广泛应用。环氧乙烷合成 的原理如图所示:
的原理如图所示: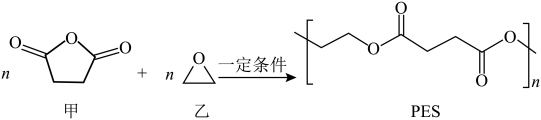
A.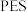 属于混合物 属于混合物 | B.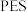 中含酯基,乙中含醚键 中含酯基,乙中含醚键 |
| C.乙醛是乙的同分异构体 | D.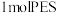 最多能消耗 最多能消耗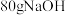 |
您最近一年使用:0次
2024-05-12更新
|
218次组卷
|
3卷引用:2024届海南省琼海市嘉积中学高三下学期模拟预测化学试题
名校
解题方法
10 . 磁性材料氮化铁镍合金应用广泛。
(1)基态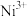 核外电子排布式为
核外电子排布式为_______ 。基态 原子与基态
原子与基态 原子核外未成对电子数之比为
原子核外未成对电子数之比为_______ 。
(2)丁二酮肟(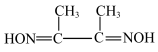 )是检验
)是检验 的灵敏试剂。丁二酮肟分子中碳原子轨道的杂化类型为
的灵敏试剂。丁二酮肟分子中碳原子轨道的杂化类型为_______ ,除 以外的非金属元素的第一电离能由小到大的顺序为
以外的非金属元素的第一电离能由小到大的顺序为_______ (用元素符号表示)。
(3)如图为一种含镍配合物及其配体。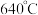 可发生置换反应,产物之一的晶胞结构如图,该反应的化学方程式为
可发生置换反应,产物之一的晶胞结构如图,该反应的化学方程式为_______ ;该晶胞中与铁原子最近且距离相等的铁原子个数为_______ 个。
(1)基态
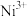 核外电子排布式为
核外电子排布式为 原子与基态
原子与基态 原子核外未成对电子数之比为
原子核外未成对电子数之比为(2)丁二酮肟(
 )是检验
)是检验 的灵敏试剂。丁二酮肟分子中碳原子轨道的杂化类型为
的灵敏试剂。丁二酮肟分子中碳原子轨道的杂化类型为 以外的非金属元素的第一电离能由小到大的顺序为
以外的非金属元素的第一电离能由小到大的顺序为(3)如图为一种含镍配合物及其配体。

①物质 在一定条件下水解生成邻羟基苯甲醛(
在一定条件下水解生成邻羟基苯甲醛( ),其沸点为
),其沸点为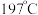 ,而对羟基苯甲醛(
,而对羟基苯甲醛(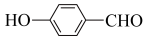 )的沸点为
)的沸点为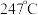 ,导致两种物质沸点相差较大的原因是
,导致两种物质沸点相差较大的原因是
②由于 原子上存在孤电子对,使含氮分子有碱性。
原子上存在孤电子对,使含氮分子有碱性。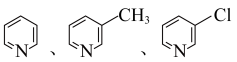 的碱性与
的碱性与 原子电子云密度有关,电子云密度越大、碱性越强,由此判断这三种物质中碱性最弱的是
原子电子云密度有关,电子云密度越大、碱性越强,由此判断这三种物质中碱性最弱的是
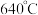 可发生置换反应,产物之一的晶胞结构如图,该反应的化学方程式为
可发生置换反应,产物之一的晶胞结构如图,该反应的化学方程式为
您最近一年使用:0次



