1 . 一种太空生命保障系统利用电解水供氧,生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,水可循环使用。
(1)已知 与
与 的燃烧热分别为
的燃烧热分别为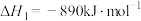 ,
, ;
;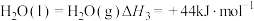 ,写出
,写出 与
与 生成
生成 和
和 的热化学方程式
的热化学方程式_________________ 。
(2)一定温度下,在恒容密闭容器中 与
与 反应生成
反应生成 和
和 。
。
①能说明该反应达到平衡状态的是_________________ (填字母)。
A. B.容器内压强一定
B.容器内压强一定
C.气体平均相对分子质量一定 D.混合气体密度一定
②已知容器的容积为 ,初始加入
,初始加入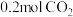 ,和
,和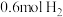 ,反应平衡后测得
,反应平衡后测得 的转化率为
的转化率为 ,则该反应的平衡常数为
,则该反应的平衡常数为_________________ 。
③温度不变,往②平衡状态中再加入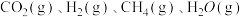 各
各 ,则此时反应速率
,则此时反应速率
_________________ 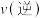 。(填“
。(填“ ”“
”“ ”或“
”或“ ")
")
(3)工业上在一定条件下利用 与
与 可直接合成有机中间体二甲醚:
可直接合成有机中间体二甲醚: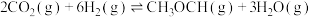 。
。
当 时,实验测得
时,实验测得 的平衡转化率随温度及压强变化如图所示:
的平衡转化率随温度及压强变化如图所示:
_________________ (填“ ”或“
”或“ ”)0。
”)0。
②图中压强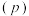 由大到小的顺序是
由大到小的顺序是_________________ 。
(1)已知
 与
与 的燃烧热分别为
的燃烧热分别为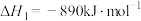 ,
, ;
;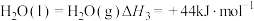 ,写出
,写出 与
与 生成
生成 和
和 的热化学方程式
的热化学方程式(2)一定温度下,在恒容密闭容器中
 与
与 反应生成
反应生成 和
和 。
。①能说明该反应达到平衡状态的是
A.
 B.容器内压强一定
B.容器内压强一定C.气体平均相对分子质量一定 D.混合气体密度一定
②已知容器的容积为
 ,初始加入
,初始加入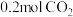 ,和
,和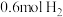 ,反应平衡后测得
,反应平衡后测得 的转化率为
的转化率为 ,则该反应的平衡常数为
,则该反应的平衡常数为③温度不变,往②平衡状态中再加入
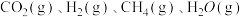 各
各 ,则此时反应速率
,则此时反应速率
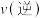 。(填“
。(填“ ”“
”“ ”或“
”或“ ")
")(3)工业上在一定条件下利用
 与
与 可直接合成有机中间体二甲醚:
可直接合成有机中间体二甲醚: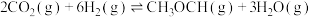 。
。当
 时,实验测得
时,实验测得 的平衡转化率随温度及压强变化如图所示:
的平衡转化率随温度及压强变化如图所示: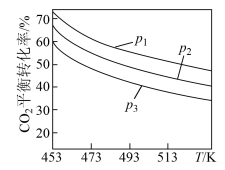

 ”或“
”或“ ”)0。
”)0。②图中压强
 由大到小的顺序是
由大到小的顺序是
您最近一年使用:0次
名校
2 . 中国科学院大连化学物理研究所李灿开发粉末纳米颗粒光催化剂体系的太阳能规模化分解水制氢的“氢农场”,模拟装置如图所示。下列叙述正确的是

| A.电极X为阳极 |
| B.电极Y发生氧化反应 |
C.电极Y的电极反应之一: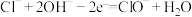 |
D.电极X、Y产生气体质量比一定等于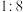 |
您最近一年使用:0次
名校
3 . 中国科学家首次实现了二氧化碳到淀粉的从头合成,CO2的捕集、利用与封存成为科学家研究的重要课题。
以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
I.CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
II.C2H6(g) CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
(1)反应I的反应历程可分为如下两步:
i. C2H6(g) C2H4(g)+H2(g) ΔH1 (反应速率较快)
C2H4(g)+H2(g) ΔH1 (反应速率较快)
ii. H2(g)+CO2(g) H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
①∆H1=_______
②相比于提高c(C2H6),提高c(CO2)对反应I速率影响更大,原因是_______ 。
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示,工业生产综合各方面的因素,反应选择800℃的原因是_______ 。 C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
____ (用含有x的代数式表示);当温度升高时,k正增大m倍,k逆增大n倍,则m_____ n(填“>”、“<”或“=”)。
以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
I.CO2(g)+C2H6(g)
 C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
C2H4(g)+H2O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)II.C2H6(g)
 CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)
CH4(g)+H2(g)+C(s) ΔH=+9kJ·mol-1 (副反应)(1)反应I的反应历程可分为如下两步:
i. C2H6(g)
 C2H4(g)+H2(g) ΔH1 (反应速率较快)
C2H4(g)+H2(g) ΔH1 (反应速率较快)ii. H2(g)+CO2(g)
 H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)
H2O(g)+CO(g) ΔH2=+44kJ·mol-1 (反应速率较慢)①∆H1=
②相比于提高c(C2H6),提高c(CO2)对反应I速率影响更大,原因是
(2)向恒压密闭容器中充入CO2和C2H6合成C2H4,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响如图所示,工业生产综合各方面的因素,反应选择800℃的原因是
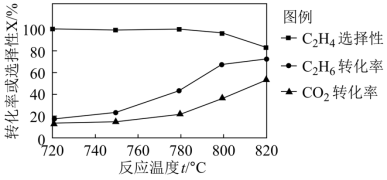
 C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示:
C2H4(g)+2H2(g) ΔH>0,温度T时,向2L的恒容反应器中充入2molCH4,仅发生上述反应,反应过程中CH4的物质的量随时间变化如图所示: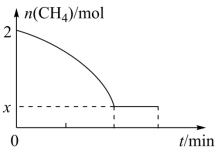

您最近一年使用:0次
4 .  常用作催化剂、固体离子电解质等。以锑白(主要成分为
常用作催化剂、固体离子电解质等。以锑白(主要成分为 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图所示。
的工艺流程如图所示。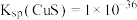 ,
,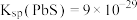 。
。
回答下列问题:
(1) 属于正盐,则
属于正盐,则 属于
属于___________ 元酸。
(2)其他条件不变,升高温度,“酸浸”速率先变快,后变慢,“变慢”的主要原因是________ 。
(3)“除杂1”中可能存在反应: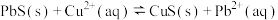 ,该反应的平衡常数
,该反应的平衡常数
___________ 。
(4)“除杂2”中 将
将 还原为
还原为 ,自身被氧化为
,自身被氧化为 ,其中氧化剂与还原剂的物质的量之比为
,其中氧化剂与还原剂的物质的量之比为___________ 。
(5)“电解”中阴极材料是___________
(6)“氟化”中不能选用玻璃容器,其原因是___________ (用化学方程式表示)。
 常用作催化剂、固体离子电解质等。以锑白(主要成分为
常用作催化剂、固体离子电解质等。以锑白(主要成分为 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图所示。
的工艺流程如图所示。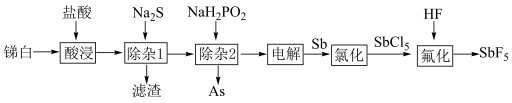
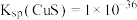 ,
,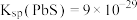 。
。回答下列问题:
(1)
 属于正盐,则
属于正盐,则 属于
属于(2)其他条件不变,升高温度,“酸浸”速率先变快,后变慢,“变慢”的主要原因是
(3)“除杂1”中可能存在反应:
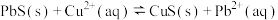 ,该反应的平衡常数
,该反应的平衡常数
(4)“除杂2”中
 将
将 还原为
还原为 ,自身被氧化为
,自身被氧化为 ,其中氧化剂与还原剂的物质的量之比为
,其中氧化剂与还原剂的物质的量之比为(5)“电解”中阴极材料是
(6)“氟化”中不能选用玻璃容器,其原因是
您最近一年使用:0次
2023-12-16更新
|
219次组卷
|
3卷引用:海南省2023-2024学年高三上学期高考全真模拟卷(四)化学试题
名校
解题方法
5 . 中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量含氧橄榄石矿物(ZxW2-xRX4)。已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种氧化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料,基态Z原子核外s,p能级上电子总数相等。下列叙述正确的是
| A.原子半径:Z>R>Y>X |
| B.X的第一电离能比同周期相邻元素小 |
| C.X的简单氢化物的热稳定性强于Y的简单氢化物 |
| D.熔点:ZY2>RX2 |
您最近一年使用:0次
2023-10-26更新
|
1049次组卷
|
7卷引用:2024届海南省海南中学高三下学期第一次模拟化学试题
2024届海南省海南中学高三下学期第一次模拟化学试题湖南省郴州市2024届高三上学期一模化学试题广西名校2023-2024学年高三上学期仿真卷(一)化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)重庆市江北区2023-2024学年高三下学期模拟测试化学试题(七)湖南省邵阳市绥宁县世贤中学2023-2024学年高三上学期12月月考化学试题湖南省常德市 临澧县第一中学2023-2024学年高三上学期第五次阶段性考试化学试题
名校
解题方法
6 . “消洗灵”常应用于医院床上用品的洗涤消毒,其化学组成可以表示为Na10P3O13Cl·5H2O(磷酸三钠次氯酸钠)。实验室制备Na10P3O13Cl·5H2O的装置如图所示(夹持装置省略)。
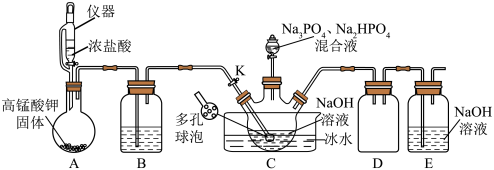
回答下列问题:
(1)HCl的电子式为___________ ;实验中用仪器a加浓盐酸的优点是___________ ;装置A中发生反应的离子方程式为__________ 。
(2)装置B中盛装的试剂名称为___________ ,装置C中采用多孔球泡的目的是___________ ,装置D的作用是___________ 。
(3)Na10P3O13Cl·5H2O中氯元素的化合价为___________ ,若装置C中参加反应的Na3PO4与Na2HPO4的物质的量之比为1∶2,则装置C中发生反应的化学方程式为__________ 。
(4)产品纯度的测定(Na10P3O13Cl·5H2O的摩尔质量为656.5 g·mol-1)。
①取a g待测试样溶于蒸馏水中并配成250 mL溶液;
②取25.00 mL待测液于锥形瓶中,加入10 mL 2 mol·L-1硫酸和25 mL 0.1 mol·L-1碘化钾溶液(过量),此时溶液出现棕色;
③滴入3滴5%的淀粉溶液,用0.05 mol·L-1的硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗溶液的体积为20.00 mL。已知:2S2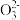 +I2=S4
+I2=S4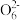 +2I-。
+2I-。
则产品的纯度为___________ (用含a的代数式表示)。

回答下列问题:
(1)HCl的电子式为
(2)装置B中盛装的试剂名称为
(3)Na10P3O13Cl·5H2O中氯元素的化合价为
(4)产品纯度的测定(Na10P3O13Cl·5H2O的摩尔质量为656.5 g·mol-1)。
①取a g待测试样溶于蒸馏水中并配成250 mL溶液;
②取25.00 mL待测液于锥形瓶中,加入10 mL 2 mol·L-1硫酸和25 mL 0.1 mol·L-1碘化钾溶液(过量),此时溶液出现棕色;
③滴入3滴5%的淀粉溶液,用0.05 mol·L-1的硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗溶液的体积为20.00 mL。已知:2S2
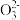 +I2=S4
+I2=S4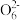 +2I-。
+2I-。则产品的纯度为
您最近一年使用:0次
名校
7 . 在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式如下:
反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH=-164.7 kJ·mol-1
CH4(g)+2H2O(g) ΔH=-164.7 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.2 kJ·mol-1
CO(g)+H2O(g) ΔH=+41.2 kJ·mol-1
反应Ⅲ:2CO(g)+2H2(g) CO2(g)+CH4(g) ΔH=-247.1 kJ·mol-1
CO2(g)+CH4(g) ΔH=-247.1 kJ·mol-1
向恒压、密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2的物质的量随温度的变化曲线如图所示。则图中曲线A表示的物质是
反应I:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH=-164.7 kJ·mol-1
CH4(g)+2H2O(g) ΔH=-164.7 kJ·mol-1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.2 kJ·mol-1
CO(g)+H2O(g) ΔH=+41.2 kJ·mol-1反应Ⅲ:2CO(g)+2H2(g)
 CO2(g)+CH4(g) ΔH=-247.1 kJ·mol-1
CO2(g)+CH4(g) ΔH=-247.1 kJ·mol-1向恒压、密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2的物质的量随温度的变化曲线如图所示。则图中曲线A表示的物质是
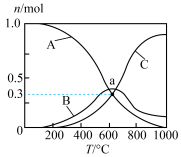
| A.CO | B.CH4 | C.CO2 | D.无法确定 |
您最近一年使用:0次
名校
解题方法
8 . 化合物M(奥司他韦)是目前治疗流感的最常用药物之一,其合成路线如下:
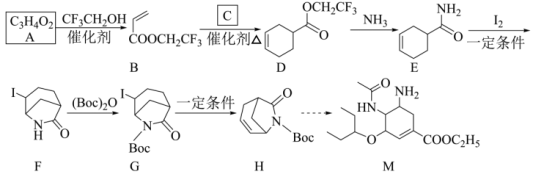
已知:①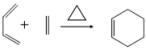 ;②
;②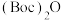 的结构简式为
的结构简式为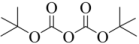
回答问题:
(1)A的结构简式为_______ ;C的化学名称为_______ 。
(2)E与NaOH溶液共热的化学方程式为_______ 。
(3)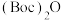 的核磁共振氢谱有
的核磁共振氢谱有_______ 组峰。
(4)G→H的反应类型是_______ ;M中不含氧的官能团的名称是_______ 。
(5)B有多种同分异构体,同时满足下列条件的同分异构体共有_______ 种(不考虑立体异构)。
a.分子结构中含有
b.能与 溶液发生反应产生气体
溶液发生反应产生气体
(6)参照上述合成路线,以 和
和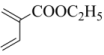 为原料设计合成
为原料设计合成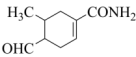 的路线
的路线_______ (其它试剂任选)。

已知:①
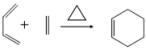 ;②
;②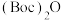 的结构简式为
的结构简式为
回答问题:
(1)A的结构简式为
(2)E与NaOH溶液共热的化学方程式为
(3)
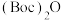 的核磁共振氢谱有
的核磁共振氢谱有(4)G→H的反应类型是
(5)B有多种同分异构体,同时满足下列条件的同分异构体共有
a.分子结构中含有

b.能与
 溶液发生反应产生气体
溶液发生反应产生气体(6)参照上述合成路线,以
 和
和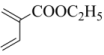 为原料设计合成
为原料设计合成 的路线
的路线
您最近一年使用:0次
解题方法
9 .  的资源化利用是当前解决温室效应,实现“碳中和”目标的最恰当途径。回答下列问题:
的资源化利用是当前解决温室效应,实现“碳中和”目标的最恰当途径。回答下列问题:
(1)二氧化碳与氢气催化重整可制备甲醇,已知:

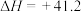 kJ⋅mol-1
kJ⋅mol-1

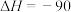 kJ⋅mol-1
kJ⋅mol-1
则 、
、 反应生成
反应生成 与
与 的热化学方程式为
的热化学方程式为___________ 。
(2)在相同催化剂条件下,向初始容积均为2 L的甲、乙两个密闭容器中均充入4 mol 、12 mol
、12 mol  的混合气体并使它们均发生反应:
的混合气体并使它们均发生反应: 。反应中甲容器维持容积不变,乙容器维持压强不变,测得甲容器中0~t min内
。反应中甲容器维持容积不变,乙容器维持压强不变,测得甲容器中0~t min内 的转化率与温度(T)的关系如图所示(不考虑催化剂活性变化):
的转化率与温度(T)的关系如图所示(不考虑催化剂活性变化):
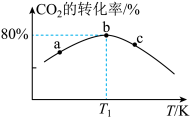
①a、b、c三点中,肯定不是平衡态的为___________ 点。若在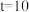 ,
, K时,反应达到平衡,则0~10min内,
K时,反应达到平衡,则0~10min内,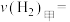
___________ ,平衡常数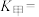
___________ (结果保留两位有效数字)。
② K时,乙容器中反应达到平衡所需要的时间
K时,乙容器中反应达到平衡所需要的时间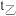
___________  (填“>”“=”或“<”,下同),相应的平衡常数
(填“>”“=”或“<”,下同),相应的平衡常数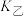
___________  。
。
 的资源化利用是当前解决温室效应,实现“碳中和”目标的最恰当途径。回答下列问题:
的资源化利用是当前解决温室效应,实现“碳中和”目标的最恰当途径。回答下列问题:(1)二氧化碳与氢气催化重整可制备甲醇,已知:

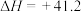 kJ⋅mol-1
kJ⋅mol-1
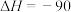 kJ⋅mol-1
kJ⋅mol-1则
 、
、 反应生成
反应生成 与
与 的热化学方程式为
的热化学方程式为(2)在相同催化剂条件下,向初始容积均为2 L的甲、乙两个密闭容器中均充入4 mol
 、12 mol
、12 mol  的混合气体并使它们均发生反应:
的混合气体并使它们均发生反应: 。反应中甲容器维持容积不变,乙容器维持压强不变,测得甲容器中0~t min内
。反应中甲容器维持容积不变,乙容器维持压强不变,测得甲容器中0~t min内 的转化率与温度(T)的关系如图所示(不考虑催化剂活性变化):
的转化率与温度(T)的关系如图所示(不考虑催化剂活性变化):
①a、b、c三点中,肯定不是平衡态的为
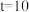 ,
, K时,反应达到平衡,则0~10min内,
K时,反应达到平衡,则0~10min内,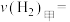
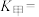
②
 K时,乙容器中反应达到平衡所需要的时间
K时,乙容器中反应达到平衡所需要的时间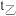
 (填“>”“=”或“<”,下同),相应的平衡常数
(填“>”“=”或“<”,下同),相应的平衡常数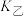
 。
。
您最近一年使用:0次
2023-04-22更新
|
217次组卷
|
2卷引用:海南省海口市2023届高三下学期一模联考化学试题
10 . 美好生活离不开化学。下列人类活动运用的化学原理正确的是
| 选项 | 人类活动 | 化学原理 |
| A | 常温下用铝罐盛放浓硫酸 | 浓硫酸使铝表面形成致密的氧化膜 |
| B | 液氨作制冷剂 |  溶于水吸收大量的热 溶于水吸收大量的热 |
| C |  在医疗上作“钡餐” 在医疗上作“钡餐” |  为弱电解质 为弱电解质 |
| D |  可用作氮肥 可用作氮肥 |  受热易分解 受热易分解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-22更新
|
555次组卷
|
5卷引用:海南省海口市2023届高三下学期一模联考化学试题



