名校
解题方法
1 . 已知 在酸性溶液中易被还原成
在酸性溶液中易被还原成 ,
, 、
、 、
、 、
、 的氧化性依次减弱。下列反应在水溶液中不可能发生的是
的氧化性依次减弱。下列反应在水溶液中不可能发生的是
 在酸性溶液中易被还原成
在酸性溶液中易被还原成 ,
, 、
、 、
、 、
、 的氧化性依次减弱。下列反应在水溶液中不可能发生的是
的氧化性依次减弱。下列反应在水溶液中不可能发生的是A.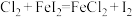 |
B.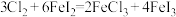 |
C.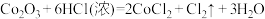 |
D.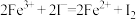 |
您最近一年使用:0次
2023-12-06更新
|
167次组卷
|
62卷引用:陕西省西安高级中学2021-2022学年高一上学期竞赛化学试题
陕西省西安高级中学2021-2022学年高一上学期竞赛化学试题陕西省榆林市定边四中2023届高三上学期第一次月考化学试题陕西省咸阳市武功县普集高级中学2022-2023学年高一上学期第一次月考化学试题陕西省西安市蓝田县乡镇高中联考2023-2024学年高一上学期11月期中化学试题福建省厦门第六中学2019-2020学年高一下学期3月月考化学试题(已下线)【浙江新东方】6广东省东莞市东华高级中学2020-2021学年高一上学期第一次月考化学试题广东省深圳外国语学校2021届高三第二次月考化学试题云南省保山市第九中学2021届高三上学期阶段测试化学试题湖南省长沙市实验中学2020—2021学年高一上学期第一次月考(10月)化学试题(已下线)【浙江新东方】61河南省许昌市建安区第一高级中学2020-2021学年高一上学期阶段性测试(12月)化学试题安徽省示范高中培优联盟2020-2021学年高一上学期冬季联赛化学试题(已下线)练习4 氧化还原反应-2020-2021学年【补习教材·寒假作业】高一化学(人教版)安徽省六安市城南中学2021届高三上学期第二次月考化学试题河南省滑县实验学校2020-2021学年高一上学期11月半月考试化学试题(已下线)专题04 氧化还原反应-备战2021届高考化学二轮复习题型专练甘肃省镇原县第二中学2020-2021学年高一上学期期中考试化学试题云南省保山市第九中学2021届高三上学期期中考试化学试题安徽省江淮名校2020-2021学年高一下学期开学联考化学试题山西省临汾市县底中学校2020-2021学年高三上学期开学考试化学试题黑龙江省哈尔滨市第三中学2020-2021学年高一上学期期末考试化学试卷(已下线)衔接点07 氧化剂和还原剂-2021年初升高化学无忧衔接(已下线)专题1.3.3 氧化剂、还原剂(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)(已下线)专题05 氧化还原反应 (热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)课时10 氧化还原反应规律及应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)安徽省泗县第一中学2021-2022学年高二上学期开学考试化学试题河南省洛阳市第四十三中学2022届高三上学期开学考试化学试题湖南省益阳市箴言中学2021-2022学年高一上学期10月月考化学试题 黑龙江省鸡西实验中学2020-2021学年高一上学期第一次月考化学试题河北省石家庄市第二中学2021-2022学年高一上学期10月月考化学试题湖南省邵阳市邵东创新实验学校2021-2022学年高三上学期第一次月考化学试题湖北省巴东县第一高级中学2021-2022学年高一上学期第一次教学质量检测化学试题(已下线)易错专题08 氧化还原反应规律的应用及相关计算-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)河南省商丘市高级中学2021-2022学年高一上学期期末考试暨学学考试化学试题湖北省问津联合体2021-2022学年高一下学期5月质量检测化学试题(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)衔接点12 氧化剂和还原剂-2022年初升高化学无忧衔接?(已下线)第03练 氧化还原反应-2023年高考化学一轮复习小题多维练(全国通用)江西省丰城市第九中学(日新班)2021-2022学年高一下学期期末检测化学试题四川省德阳市德阳五中2021-2022学年高一上学期期末考试化学试题(已下线)第一章 物质及其变化(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)浙江省绿谷联盟2022-2023学年高一上学期10月份考试化学试题 安徽省合肥市第六中学2020-2021学年高一上学期第一次月考化学试题河北省石家庄市第二中学2022-2023学年高一上学期10月月考化学试题内蒙古呼和浩特市第二中学致远级部2022-2023学年高一上学期第一次月考化学试题重庆市南开中学2022-2023学年高一上学期12月定时练习化学试题安徽省皖北地区2022-2023学年高一上学期期末联考化学试题(已下线)考点04 氧化还原反应的基本概念和规律(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点巩固卷02 化学物质及其变化(3大考点44题)?-2024年高考化学一轮复习考点通关卷(新高考通用)第2课时 氧化剂和还原剂湖南省长沙市长郡中学2023-2024学年高一上学期第一次月考化学试题甘肃省部分学校2023-2024学年高一上学期10月期中考试化学试题天津市南开中学2023-2024学年高三上学期第二次考试化学试题湖南省永州市第一中学2023-2024学年高一上学期第一次月考化学试题北京市第一六一中学2022-2023学年高一上学期12月月考化学试题安徽省亳州市第二完全中学2023-2024学年高一上学期期末考试化学试题海南省琼海市嘉积中学2023-2024学年高一上学期期末考试化学试题A卷黑龙江省哈尔滨市第三中学校2023-2024学年高一下学期寒假验收考试 化学试卷
名校
解题方法
2 . 已知:





若使 液态酒精完全燃烧,最后恢复到室温,则放出的热量为(单位为
液态酒精完全燃烧,最后恢复到室温,则放出的热量为(单位为 )
)






若使
 液态酒精完全燃烧,最后恢复到室温,则放出的热量为(单位为
液态酒精完全燃烧,最后恢复到室温,则放出的热量为(单位为 )
)A.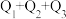 | B.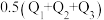 |
C. | D. |
您最近一年使用:0次
2022-12-08更新
|
211次组卷
|
58卷引用:陕西省渭南韩城市2019-2020学年高二上学期竞赛考试化学试题
陕西省渭南韩城市2019-2020学年高二上学期竞赛考试化学试题(已下线)2011届陕西省长安一中高三上学期第三次质量检测化学试卷陕西省西安中学2016-2017学年高一(实验班)下学期期中考试化学试题陕西省西安市远东第一中学2018-2019学年高二上学期10月月考化学试题(已下线)2011-2012学年江苏省南京三中高二下学期期末考试化学选修试卷(已下线)2012-2013学年山东省冠县武训高中高二10月月考化学试卷(已下线)2012-2013学年山东省冠县武训高中高二10月月考化学试卷(已下线)2012-2013年海南琼海嘉积中学高二上高中教学质量监测理化学试卷(已下线)2012-2013学年云南省玉溪一中高二下学期期末考试化学试卷(已下线)2013-2014学年贵州省重点高中高二上学期期中考试理科化学试卷(已下线)2014年高考化学指导冲关 第3练化学反应与能量变化练习卷(已下线)2013-2014学年湖北省荆门市高二上学期期末质量检测化学试卷(已下线)2013-2014学年湖北省荆门市高二上学期期末考试化学试卷(已下线)2014-2015学年浙江台州中学高二上学期第一次统练化学试卷2015-2016学年河南省信阳高级中学高二下开学测化学试卷2016届甘肃省武威六中高三一轮复习阶段测(五)化学试卷2015-2016学年湖北省宜昌一中高二下3月月考化学试卷2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷(已下线)同步君 人教版 选修四 第一章 第三节 第一课时 盖斯定律2015-2016学年山东省烟台市莱山一中高二化学上学期段考试卷2016-2017学年甘肃省天水一中高二上月考一化学试卷黑龙江省齐齐哈尔市第八中学2017-2018学年高二9月月考化学试题黑龙江省饶河县高级中学2017-2018学年高二上学期第一次月考化学试题河北省定州市第二中学2017-2018学年高二上学期第一次月考化学试题西藏日喀则市第一高级中学2017-2018学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市实验中学2018届高三上学期期中考试化学试题高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第一课时(盖斯定律)湖南辰溪博雅实验学校2018-2019学年高二8月月考化学试题【全国百强校】贵州省铜仁市思南中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】甘肃省会宁县第一中学2018-2019学年高二(理科)上学期期中考试化学试题苏教版高二化学选修四专题练习题:专题一 化学反应与能量变化江西省南昌市第十中学2018-2019学年高一下学期期末考试化学试题黑龙江省鹤岗市第一中学2019-2020学年高二上学期开学考试(8月)化学试题山西省应县第一中学校2019-2020学年高二上学期第一次月考化学试题河南省鲁山县第一高级中学2019-2020学年高二上学期9月月考化学试题浙江省嘉兴市第一中学2019-2020学年高二10月月考化学试题广东省深圳市罗湖区高级中学2019-2020学年高二上学期第一次段考试化学试题(已下线)2019年12月18日 《每日一题》化学人教版(选修4)——盖斯定律安徽省潜山第二中学2019-2020学年高二上学期第一次月考化学试题云南省昭通市永善县明志高级中学2019—2020学年高二上学期期末考试化学试题云南省玉溪市玉溪第一中学2018-2019学年高二上学期11月月考化学试题广东省湛江市第二十一中学2019-2020学年高二下学期开学考试化学试题高中必刷题高二选择性必修1第一章 化学反应的热效应 第一章素养检测江西省南昌市第二中学2020-2021学年高二上学期第一次月考化学试题选择性必修1专题1第一单元综合训练江西省名校2021-2022学年高二上学期第一次月考化学试题四川省成都市简阳市阳安中学2021-2022学年高二上学期9月月考化学试卷安徽省淮北市树人高级中学2021-2022学年高二上学期第一次月考化学试题(已下线)必考点01 化学反应的热效应-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)宁夏银川一中2021-2022学年高二上学期期中考试化学试题云南省玉溪澄江市第一中学2021-2022学年下学期高二开学考试化学试题(已下线)化学反应的热效应——进阶学习河南省温县第一高级中学2021-2022学年高二下学期开学考试化学试题福建省石狮市第一中学2022-2023学年高二上学期第一次月考化学试题北京市顺义牛栏山第一中学2022-2023学年高二上学期10月月考化学试题云南省玉溪市华宁县第二中学2021-2022年高二下学期开学考试化学试题江西省宜春市丰城市第九中学2023-2024学年高一上学期12月月考化学试题广西钦州市第四中学2023-2024学年高二上学期9月考试化学试卷
名校
解题方法
3 . A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如图所示。
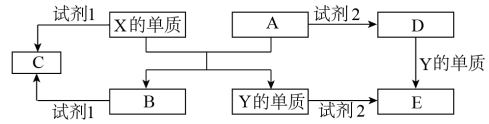
(1)X的单质与A反应的化学方程式是____ 。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是____ 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是____ 。
②某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是____ 。

(1)X的单质与A反应的化学方程式是
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是
②某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是
您最近一年使用:0次
名校
解题方法
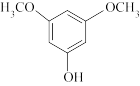
4 . 3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下: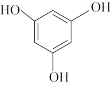 +2CH3OH
+2CH3OH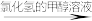
 +2H2O。
+2H2O。
甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是____ 。
②萃取用到的分液漏斗使用前需____ 并洗净,分液时有机层在分液漏斗的____ (填“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是____ 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是____ (填字母)。
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
 +2CH3OH
+2CH3OH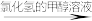
 +2H2O。
+2H2O。甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/g·cm-3 | 溶解性 |
| 甲醇 | 64.7 | 0.7915 | 易溶于水 | |
| 乙醚 | 34.5 | 0.7138 | 微溶于水 | |
| 3,5-二甲氧基苯酚 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
①分离出甲醇的操作是
②萃取用到的分液漏斗使用前需
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
您最近一年使用:0次
名校
解题方法
5 . 氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如图:
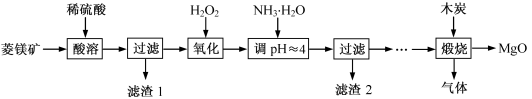
(1)MgCO3与稀硫酸反应的离子方程式为____ 。
(2)加入H2O2氧化时,发生反应的化学方程式为____ 。
(3)滤渣2的成分是____ (填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑;
2MgO+2SO2↑+CO2↑;
MgSO4+C MgO+SO2↑+CO↑;
MgO+SO2↑+CO↑;
MgSO4+3C MgO+S↑+3CO↑。
MgO+S↑+3CO↑。
利用如图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体是____ (填化学式)。
②A中得到的淡黄色固体能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式:____ 。

(1)MgCO3与稀硫酸反应的离子方程式为
(2)加入H2O2氧化时,发生反应的化学方程式为
(3)滤渣2的成分是
(4)煅烧过程存在以下反应:
2MgSO4+C
 2MgO+2SO2↑+CO2↑;
2MgO+2SO2↑+CO2↑;MgSO4+C
 MgO+SO2↑+CO↑;
MgO+SO2↑+CO↑;MgSO4+3C
 MgO+S↑+3CO↑。
MgO+S↑+3CO↑。利用如图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体是
②A中得到的淡黄色固体能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式:
您最近一年使用:0次
2022-06-21更新
|
328次组卷
|
2卷引用:陕西省西安高级中学2021-2022学年高一上学期竞赛化学试题
名校
解题方法
6 . 硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5•H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:

回答下列问题:
(1)写出Mg2B2O5•H2O与硫酸反应的化学方程式____ 。
(2)利用____ 的磁性,可将其从“浸渣”中分离。“浸渣”中还剩余的物质是____ (化学式)。
(3)“净化除杂”需先加H2O2溶液,作用是____ 。
(4)“粗硼酸”中的主要杂质是____ (填名称)。
(5)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程____ 。

回答下列问题:
(1)写出Mg2B2O5•H2O与硫酸反应的化学方程式
(2)利用
(3)“净化除杂”需先加H2O2溶液,作用是
(4)“粗硼酸”中的主要杂质是
(5)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程
您最近一年使用:0次
名校
解题方法
7 . “碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出)。

下列有关该方法的叙述中正确的是

下列有关该方法的叙述中正确的是
| A.能耗小是该方法的一大优点 |
| B.整个过程中,只有一种物质可以循环利用 |
| C.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤 |
| D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品 |
您最近一年使用:0次
名校
解题方法
8 . BaCl2•xH2O中结晶水数目可通过重量法来确定:
①称取1.220g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;②过滤并洗涤沉淀;③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧至恒重,称得沉淀质量为1.165g。则BaCl2•xH2O中的x为
①称取1.220g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;②过滤并洗涤沉淀;③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧至恒重,称得沉淀质量为1.165g。则BaCl2•xH2O中的x为
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
2022-06-21更新
|
216次组卷
|
2卷引用:陕西省西安高级中学2021-2022学年高一上学期竞赛化学试题
名校
解题方法
9 . 一定条件下,在水溶液中1molCl-,ClO (x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是
(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是
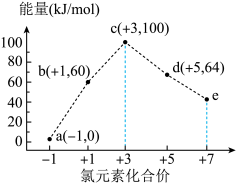
 (x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是
(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是 
A.e是ClO |
| B.b→a+c反应的活化能为60kJ•mol-1 |
| C.a、b、c、d、e中c最稳定 |
D.b→a+d反应的热化学方程式为:3ClO-(aq)=ClO (aq)+2Cl-(aq) △H= -116kJ•mol-1 (aq)+2Cl-(aq) △H= -116kJ•mol-1 |
您最近一年使用:0次
2021-10-13更新
|
327次组卷
|
16卷引用:陕西省渭南韩城市2019-2020学年高二上学期竞赛考试化学试题
陕西省渭南韩城市2019-2020学年高二上学期竞赛考试化学试题【全国百强校】陕西省西安市第一中学2018-2019学年高二上学期10月月考化学试题2016届河南省信阳市高三上学期期末质检化学试卷2016-2017学年江西省师大附中高二上第一次月考化学试卷贵州省思南中学2017-2018学年高二上学期第一次月考化学试题福建省晋江市季延中学2018-2019学年高二(理)上学期期中考试化学试题福建省泉州市泉港区第一中学2020届高三上学期第一次月考化学试题广东省蕉岭县蕉岭中学2019-2020学年高二上学期第一次段考化学试题贵州省三都水族自治县高级中学2019-2020学年高二上学期期末考试化学试题内蒙古自治区乌兰察布市集宁一中2019-2020学年高一下学期第三次月考化学试题(已下线)第19讲 化学能与热能 (精练)-2021年高考化学一轮复习讲练测甘肃省会宁县第一中学2020-2021学年高二上学期第一次月考化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖南省常德市第一中学2021-2022学年高二上学期第一次月考化学试题河南省范县第一中学2021-2022学年高二上学期第一次月考检测化学试题
10 . 在一固定容积的密闭容器中,进行如下化学反应:CO2(g) + H2(g)⇌CO(g) + H2O(g)。其化学平衡常数K和温度t的关系如下:
请回答:
(1)上述反应正向进行时,反应为_______ 热反应(填“放”或“吸”)。
(2)能判断该反应已经达到化学平衡状态的依据是_______ 。
a.容器内压强不变 b.v正(H2) = v逆(CO) c.CO2的质量分数不变
(3)温度为850℃时,可逆反应CO (g) + H2O (g)⇌CO2 (g) + H2 (g) 在固定容积的密闭容器中进行,容器内各物质的浓度变化如下:
计算:3min时(CO的浓度)c1 =_______ mol/L,H2O (g)的转化率=_______ 。
(4)表中5min~6min之间数值发生变化,可能的原因是_______(单选)。
| t/℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答:
(1)上述反应正向进行时,反应为
(2)能判断该反应已经达到化学平衡状态的依据是
a.容器内压强不变 b.v正(H2) = v逆(CO) c.CO2的质量分数不变
(3)温度为850℃时,可逆反应CO (g) + H2O (g)⇌CO2 (g) + H2 (g) 在固定容积的密闭容器中进行,容器内各物质的浓度变化如下:
| 时间/min | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
计算:3min时(CO的浓度)c1 =
(4)表中5min~6min之间数值发生变化,可能的原因是_______(单选)。
| A.增加水蒸气 | B.降低温度 | C.使用催化剂 | D.增加氢气浓度 |
您最近一年使用:0次



