3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下: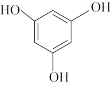 +2CH3OH
+2CH3OH
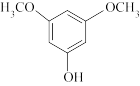 +2H2O。
+2H2O。
甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是____ 。
②萃取用到的分液漏斗使用前需____ 并洗净,分液时有机层在分液漏斗的____ (填“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是____ 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是____ (填字母)。
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
 +2CH3OH
+2CH3OH
 +2H2O。
+2H2O。甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/g·cm-3 | 溶解性 |
| 甲醇 | 64.7 | 0.7915 | 易溶于水 | |
| 乙醚 | 34.5 | 0.7138 | 微溶于水 | |
| 3,5-二甲氧基苯酚 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
①分离出甲醇的操作是
②萃取用到的分液漏斗使用前需
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
更新时间:2022-06-21 12:27:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】苯甲酸广泛应用于制药和化工行业。
I.用甲苯的氧化反应制备苯甲酸的反应原理如下:
 +2KMnO4
+2KMnO4
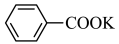 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
 +HCl→
+HCl→ +KCl
+KCl
II.制备及分离出苯甲酸、回收未反应的甲苯的流程如图所示。

(1)操作I、操作II的名称分别是_______ 、_______ 。
(2)滤液的成分是_______ 。
(3)白色固体B是_______ 。
(4)为得到无色液体A,需进行的具体操作是_______ 。
I.用甲苯的氧化反应制备苯甲酸的反应原理如下:
 +2KMnO4
+2KMnO4
 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O +HCl→
+HCl→ +KCl
+KCl| 资料 | ①甲苯被高锰酸钾氧化过程中可能出现苯甲醇,苯甲醛等副产物。 |
| ②甲苯的沸点为110.6℃,苯甲醇的沸点为205.7℃,苯甲醛的沸点为179℃。 | |
| ③苯甲酸在25℃和95℃时溶解度分别为0.3g和6.9g。 |
II.制备及分离出苯甲酸、回收未反应的甲苯的流程如图所示。

(1)操作I、操作II的名称分别是
(2)滤液的成分是
(3)白色固体B是
(4)为得到无色液体A,需进行的具体操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室制备 1,2 —二溴乙烷的反应原理如下:①CH3CH2OH在浓硫酸170℃条件下生成CH2=CH2②CH2=CH2与Br2反应生成BrCH2CH2Br。现用少量溴和50gCH3CH2OH制备1,2 —二溴乙烷。回答下列问题:
(1)制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_______ 。
A 加快反应速度 B 引发反应 C 防止乙醇挥发 D 减少副产物乙醚生成
(2)判断该制备反应已经结束的最简单方法是___________________ 。
(3)将 1,2 —二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____ 层。
(4)若产物中有少量副产物乙醚,可用____________ 的方法除去。
(5)若最终得到纯净1,2 —二溴乙烷94g,本实验的产率是__________ 。
(1)制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是
A 加快反应速度 B 引发反应 C 防止乙醇挥发 D 减少副产物乙醚生成
(2)判断该制备反应已经结束的最简单方法是
(3)将 1,2 —二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
(4)若产物中有少量副产物乙醚,可用
(5)若最终得到纯净1,2 —二溴乙烷94g,本实验的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】乙酰苯胺( )在工业上作磺胺类药物原料等,可通过苯胺和乙酸反应制得:
)在工业上作磺胺类药物原料等,可通过苯胺和乙酸反应制得:
已知:纯乙酰苯胺是白色片状晶体,熔点为114℃;微溶于冷水,可溶于热水,易溶于有机溶剂;加热时易被氧化。
实验室制备乙酰苯胺的步骤如下(部分装置省略):

Ⅰ.粗乙酰苯胺的制备
在150mL 烧瓶中加入15mL(过量)乙酸(沸点117.9℃)、少量Zn粉和10mL(0.11mol)新制得的苯胺,如图接好装置。在石棉网上用小火加热,控制顶端馏出温度105℃左右使之充分反应1h。待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有250mL冷水的烧杯中,乙酰苯胺晶体析出。充分冷却至室温后,减压过滤,用洗涤晶体2~3次。用滤液冲洗烧杯上残留的晶体,再次过滤,两次过滤得到的固体合并在一起。
Ⅱ.乙酰苯胺的提纯
将上述制得的粗乙酰苯胺固体移入500mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,称量产品为11.2g。
回答下列问题:
(1)仪器a的名称是___________ 。
(2)加入锌粉的目的是_____ 。反应中加入锌粉的量不宜过多,试从平衡的角度分析原因为______ 。
(3)步骤Ⅰ控制馏出温度105℃的理由___________ 。洗涤晶体宜选用___________ (填字母)。
A.乙醇 B.CCl4 C.冷水 D.乙醚
(4)步骤Ⅱ中,粗乙酰苯胺溶解后,补加少量蒸馏水的目的是___________ 。
(5)步骤Ⅱ中,称量前的操作是___________ 。上述提纯乙酰苯胺的方法叫___________ 。
(6)乙酰苯胺的产率为___________ 。(计算结果保留3位有效数字)
 )在工业上作磺胺类药物原料等,可通过苯胺和乙酸反应制得:
)在工业上作磺胺类药物原料等,可通过苯胺和乙酸反应制得:已知:纯乙酰苯胺是白色片状晶体,熔点为114℃;微溶于冷水,可溶于热水,易溶于有机溶剂;加热时易被氧化。
实验室制备乙酰苯胺的步骤如下(部分装置省略):

Ⅰ.粗乙酰苯胺的制备
在150mL 烧瓶中加入15mL(过量)乙酸(沸点117.9℃)、少量Zn粉和10mL(0.11mol)新制得的苯胺,如图接好装置。在石棉网上用小火加热,控制顶端馏出温度105℃左右使之充分反应1h。待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有250mL冷水的烧杯中,乙酰苯胺晶体析出。充分冷却至室温后,减压过滤,用洗涤晶体2~3次。用滤液冲洗烧杯上残留的晶体,再次过滤,两次过滤得到的固体合并在一起。
Ⅱ.乙酰苯胺的提纯
将上述制得的粗乙酰苯胺固体移入500mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,称量产品为11.2g。
回答下列问题:
(1)仪器a的名称是
(2)加入锌粉的目的是
(3)步骤Ⅰ控制馏出温度105℃的理由
A.乙醇 B.CCl4 C.冷水 D.乙醚
(4)步骤Ⅱ中,粗乙酰苯胺溶解后,补加少量蒸馏水的目的是
(5)步骤Ⅱ中,称量前的操作是
(6)乙酰苯胺的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】工业生产中,海水提取溴常用空气吹出法。某化学实验小组设计了如下实验装置(夹持装置略去)模拟该法从浓缩的海水中提取溴。
已知:Br2的沸点为58.78 ℃,密度为3.119 g·cm-3,微溶于水,有毒。

(1)实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭活塞________ ,打开活塞________ ,向A中鼓入足量热空气;
③关闭活塞b,打开活塞a,再通过A向B中通入足量Cl2;
④取B中所得溶液进行蒸馏,收集液溴。
(2)步骤①A中主要反应的离子方程式为_________________________ 。
(3)X试剂可以是_____ (填序号),步骤②B中X试剂与Br2发生反应的离子方程式为______________________ 。
a.H2O b.饱和食盐水 c.饱和Na2SO3溶液
(4)该实验中尾气处理所用的试剂可以为__________________________ 。
(5)蒸馏时,除酒精灯、石棉网、铁架台外,还应该选择仪器________ (填序号)。蒸馏操作中应控制温度为________ 。

已知:Br2的沸点为58.78 ℃,密度为3.119 g·cm-3,微溶于水,有毒。

(1)实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭活塞
③关闭活塞b,打开活塞a,再通过A向B中通入足量Cl2;
④取B中所得溶液进行蒸馏,收集液溴。
(2)步骤①A中主要反应的离子方程式为
(3)X试剂可以是
a.H2O b.饱和食盐水 c.饱和Na2SO3溶液
(4)该实验中尾气处理所用的试剂可以为
(5)蒸馏时,除酒精灯、石棉网、铁架台外,还应该选择仪器

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
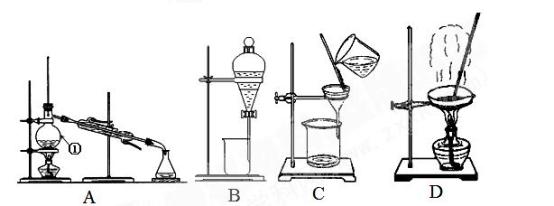
(1)从氯化钠溶液中得到氯化钠固体,选择装置___________ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置___________ ;从碘水中分离出I2,选择装置__________ ,该分离方法的名称为________________ 。
(2)装置A中①的名称是____________ ,进冷却水的方向是___________________ 。装置B在分液时为使液体顺利下滴,应进行的具体操作是______________________ 。
(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用_______ 的方法除去
Fe(OH)3胶体中混有的杂质Cl-离子。

(1)从氯化钠溶液中得到氯化钠固体,选择装置
(2)装置A中①的名称是
(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用
Fe(OH)3胶体中混有的杂质Cl-离子。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】苄酯化合物广泛存在于药物和天然产物中。实验室合成2-氯苯甲酸苄酯( ,相对分子质量为230.5)的反应原理和反应装置如图所示。
,相对分子质量为230.5)的反应原理和反应装置如图所示。
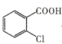 +
+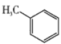 +(CH3)3C-O-OH
+(CH3)3C-O-OH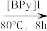
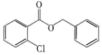 +(CH3)3C-OH+H2O
+(CH3)3C-OH+H2O

已知:①[BPy]I是1-丁基吡啶碘盐,是一种易溶于水的离子液体,可循环利用的催化剂
②2-氯苯甲酸苄酯在乙酸乙酯中具有良好的溶解性
回答下列问题:
(1)仪器X的名称为___________ ,其作用是___________ 。
(2)若无恒温加热器,可替代的加热方式是___________ ;甲苯在反应中既是反应物又是溶剂,反应结束后分离出剩余甲苯常用的物理方法的名称是___________
(3)分离出甲苯后,将混合物转移至___________ (填仪器名称),加入乙酸乙酯和水萃取3次,加入乙酸乙酯是为了萃取___________ ,加入水则主要是为了萃取___________ ;合并有机相后加入无水硫酸钠固体,其作用是___________ ;抽滤除去无水硫酸钠,再通过分离、提纯等操作得到2-氯苯甲酸苄酯。
(4)实验中2-氯苯甲酸(相对分子质量为156.5)的用量为0.1565g,其它反应物足量,最终制得2-氯苯甲酸苄酯0.2075g,产率为___________ 。
 ,相对分子质量为230.5)的反应原理和反应装置如图所示。
,相对分子质量为230.5)的反应原理和反应装置如图所示。 +
+ +(CH3)3C-O-OH
+(CH3)3C-O-OH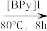
 +(CH3)3C-OH+H2O
+(CH3)3C-OH+H2O
已知:①[BPy]I是1-丁基吡啶碘盐,是一种易溶于水的离子液体,可循环利用的催化剂
②2-氯苯甲酸苄酯在乙酸乙酯中具有良好的溶解性
回答下列问题:
(1)仪器X的名称为
(2)若无恒温加热器,可替代的加热方式是
(3)分离出甲苯后,将混合物转移至
(4)实验中2-氯苯甲酸(相对分子质量为156.5)的用量为0.1565g,其它反应物足量,最终制得2-氯苯甲酸苄酯0.2075g,产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】工业生产中以浓缩海水为原料提取溴的部分过程如图:_______ 。
(2)C装置的作用是_______ 。
(3)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。一位同学根据溴的沸点是59℃,提出采用_______ 方法从该混合液中分离出溴单质;另一位同学用萃取法提取溴单质,使用CCl4作为萃取剂的原因是_______ 。
(4)(CN)2与Cl2性质相似,则(CN)2分子中含有的化学键有_______ (填“离子键”、“极性键”或“非极性键”);(CN)2的制备原理同实验室制取Cl2类似,在酸性条件下用MnO2氧化对应的阴离子得到。写出制取(CN)2的离子方程式:_______ 。
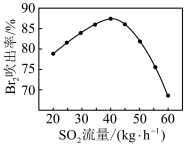
(5)工业生产过程的吹出塔中,Br2吹出率与吸收塔中SO2流量的关系如图所示。_______ 。
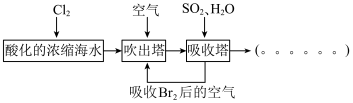
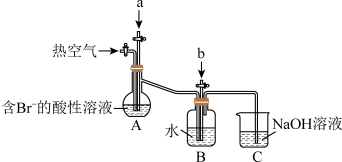
(2)C装置的作用是
(3)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。一位同学根据溴的沸点是59℃,提出采用
(4)(CN)2与Cl2性质相似,则(CN)2分子中含有的化学键有
(5)工业生产过程的吹出塔中,Br2吹出率与吸收塔中SO2流量的关系如图所示。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】从I2—CCl4溶液中提取碘用反萃取法,其流程如下:

(1)常选择有机溶剂CCl4萃取水溶液中的I2,选择CCl4做萃取剂的原因有:CCl4与水不反应也_______ ;I2在CCl4中溶解_______ (填“大于”或“小于”)I2在水中溶解。
(2)“配制100g质量分数为45%H2SO4溶液”一定不会用到“配制100mL 6mol/LNaOH溶液”中的_______ 仪器(填名称)。
(3)对所配制NaOH溶液进行测定,发现其浓度偏低,可能的原因是_______ (填序号)。
A.用生锈砝码称量NaOH固体
B.容量瓶用蒸馏水洗涤后未干燥
C.将溶解后未冷却的NaOH溶液立即转入容量瓶,洗涤、定容
D.转移溶液时,有少量溶液不慎洒到容量瓶外
E.俯视容量瓶刻线进行定容
F.定容后,倒置摇匀容量瓶,发现液面低于刻度线,便补水至刻线处
(4)上述提取过程中的操作1用到的玻璃仪器除了烧杯外,还有_______ ,操作2名称是_______ 。
(5)碘单质与浓NaOH溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O,像这种将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中的方法即为反萃取法。指出上述反应中氧化剂与还原剂的物质的量之比为_______ 。

(1)常选择有机溶剂CCl4萃取水溶液中的I2,选择CCl4做萃取剂的原因有:CCl4与水不反应也
(2)“配制100g质量分数为45%H2SO4溶液”一定不会用到“配制100mL 6mol/LNaOH溶液”中的
(3)对所配制NaOH溶液进行测定,发现其浓度偏低,可能的原因是
A.用生锈砝码称量NaOH固体
B.容量瓶用蒸馏水洗涤后未干燥
C.将溶解后未冷却的NaOH溶液立即转入容量瓶,洗涤、定容
D.转移溶液时,有少量溶液不慎洒到容量瓶外
E.俯视容量瓶刻线进行定容
F.定容后,倒置摇匀容量瓶,发现液面低于刻度线,便补水至刻线处
(4)上述提取过程中的操作1用到的玻璃仪器除了烧杯外,还有
(5)碘单质与浓NaOH溶液发生的反应为:3I2+6NaOH=5NaI+NaIO3+3H2O,像这种将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中的方法即为反萃取法。指出上述反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某课外小组的同学设计如下实验装置模拟海水提溴:
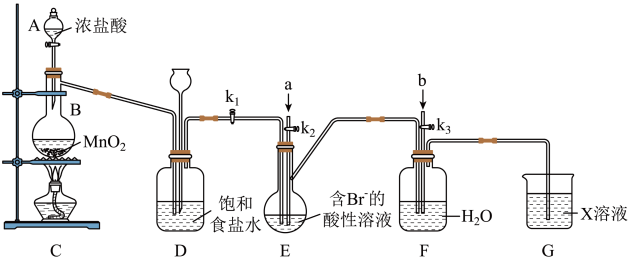
试回答下列问题:
(1)仪器A的名称为_______ 。
(2)实验时,打开 ,关闭
,关闭 、
、 ,点燃C处的酒精灯,反应一段时间。
,点燃C处的酒精灯,反应一段时间。
①仪器B中发生反应的离子方程式是_______ 。
②装置D的作用为_______ (填两点)。
(3)熄灭C处的酒精灯,关闭 ,打开
,打开 、
、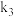 ,从a、b两处分别通入热空气、
,从a、b两处分别通入热空气、 。
。
①通入热空气的目的是_______ 。
②反应过程中,装置F中有 生成,则装置F中发生的主要反应的离子方程式是
生成,则装置F中发生的主要反应的离子方程式是_______ ;
③X溶液可能是_______ 。
(4)该小组的同学向反应后的装置F溶液中通入 ,充分反应后得到混合溶液,用
,充分反应后得到混合溶液,用 从混合溶液中萃取溴的过程如下:
从混合溶液中萃取溴的过程如下:
A.向分液漏斗中加入混合溶液和 ,并盖好玻璃塞;
,并盖好玻璃塞;
B.倒转分液漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
C.把盛有溶液的分液漏斗放在铁架台的铁圈中静置,分层;
D.将分液漏斗上口的玻璃塞打开或使玻璃塞上的凹槽或小孔对准分液漏斗口上的小孔;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液。
①D步骤操作的目的是_______ 。
②已知碘在酒精中的溶解度比在水中大得多,能不能用酒精来萃取碘水中的碘?_______ (填“能”或“不能”),其理由是_______ 。

试回答下列问题:
(1)仪器A的名称为
(2)实验时,打开
 ,关闭
,关闭 、
、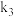 ,点燃C处的酒精灯,反应一段时间。
,点燃C处的酒精灯,反应一段时间。①仪器B中发生反应的离子方程式是
②装置D的作用为
(3)熄灭C处的酒精灯,关闭
 ,打开
,打开 、
、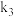 ,从a、b两处分别通入热空气、
,从a、b两处分别通入热空气、 。
。①通入热空气的目的是
②反应过程中,装置F中有
 生成,则装置F中发生的主要反应的离子方程式是
生成,则装置F中发生的主要反应的离子方程式是③X溶液可能是
(4)该小组的同学向反应后的装置F溶液中通入
 ,充分反应后得到混合溶液,用
,充分反应后得到混合溶液,用 从混合溶液中萃取溴的过程如下:
从混合溶液中萃取溴的过程如下:A.向分液漏斗中加入混合溶液和
 ,并盖好玻璃塞;
,并盖好玻璃塞;B.倒转分液漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
C.把盛有溶液的分液漏斗放在铁架台的铁圈中静置,分层;
D.将分液漏斗上口的玻璃塞打开或使玻璃塞上的凹槽或小孔对准分液漏斗口上的小孔;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液。
①D步骤操作的目的是
②已知碘在酒精中的溶解度比在水中大得多,能不能用酒精来萃取碘水中的碘?
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】化合物A~E存在如下转化关系。A和E都是含两个环的有机物,E分子有1个六元环和1个五元环结构。其中A中具有内盐结构; C具有两性、环上有两个取代基,C 的钠盐与碱石灰共热反应后则只余下一个取代基。

已知: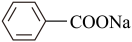 +NaOH
+NaOH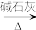
 +Na2CO3
+Na2CO3
回答下列问题:
(1)A的结构简式是_______ ; E的结构简式是_______ 。
(2)写出在一定条件下C形成高聚物的化学方程式_______ 。

已知:
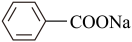 +NaOH
+NaOH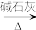
 +Na2CO3
+Na2CO3回答下列问题:
(1)A的结构简式是
(2)写出在一定条件下C形成高聚物的化学方程式
您最近一年使用:0次
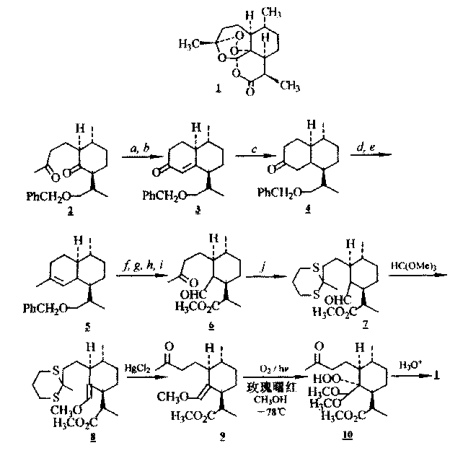
【推荐2】青蒿素是我国科技工作者于1972年从中药青蒿中提取得到的,其结构在1976年得到确认。据英国的《自然》杂志在2003年8月的一篇论文中报道,青蒿素与疟虫接触后直接与疟虫的细胞膜作用而起到杀虫效果,故半衰期短,疟虫也难以产生抗药性。此外,青蒿素还没有抗疟常用药“奎宁”所产生的副作用。我国研制的青蒿素类药物“蒿甲醚”于2004年接受了泰国最高医学奖的表彰。青蒿素的结构式如1所示。
(1)青蒿素分子中有_______ 官能团?
(2)青蒿素分子中有_______ 个手性碳原子?
(3)青蒿素的全合成工作也是由我国的科研人员首次完成的,根据给予的反应过程写出a,b,c,d,e,f,g,h,i,j所代表的反应试剂:_______ 、_______ 、_______ 、_______ 、_______ 、_______ 、_______ 、_______ 、_______ 、_______ 。
(4)全合成工作中最后一步从10到1的反应涉及到哪几种化学反应类型_______ ?
(1)青蒿素分子中有
(2)青蒿素分子中有
(3)青蒿素的全合成工作也是由我国的科研人员首次完成的,根据给予的反应过程写出a,b,c,d,e,f,g,h,i,j所代表的反应试剂:
(4)全合成工作中最后一步从10到1的反应涉及到哪几种化学反应类型

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】阿司匹林(乙酰水杨酸,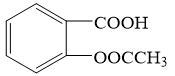 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135°C.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135°C.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
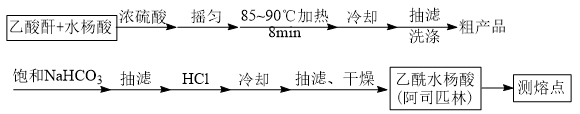
主要试剂和产品的物理常数
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是_______ 。
(2)写出制备阿司匹林的化学方程式_______ 。
(3)①合成阿斯匹林时,最合适的加热方法是_______ 。
②抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是_______ 。
(4)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤,则加饱和NaHCO3溶液的目的是_________ 。
另一种改进的提纯方法,称为重结晶提纯法。方法如下:
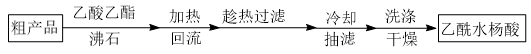
(5)改进的提纯方法中加热回流的装置如图所示,

①使用温度计的目的是_______ ,冷凝水的流进方向是_______ (填“b”或“c”)。
②重结晶提纯法所得产品的有机杂质要比原方案少的原因是_______ 。
(6)检验产品中是否含有水杨酸的化学方法是_______ 。
(7)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称量产品m=2.2g,则所得乙酰水杨酸的产率为_______ 。
 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135°C.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135°C.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
主要试剂和产品的物理常数
| 名称 | 相对分子质量 | 熔点或沸点(°C) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是
(2)写出制备阿司匹林的化学方程式
(3)①合成阿斯匹林时,最合适的加热方法是
②抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是
(4)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤,则加饱和NaHCO3溶液的目的是
另一种改进的提纯方法,称为重结晶提纯法。方法如下:
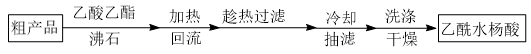
(5)改进的提纯方法中加热回流的装置如图所示,

①使用温度计的目的是
②重结晶提纯法所得产品的有机杂质要比原方案少的原因是
(6)检验产品中是否含有水杨酸的化学方法是
(7)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称量产品m=2.2g,则所得乙酰水杨酸的产率为
您最近一年使用:0次



