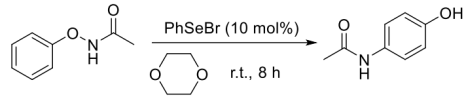
阿司匹林(乙酰水杨酸,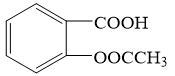 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135°C.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135°C.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
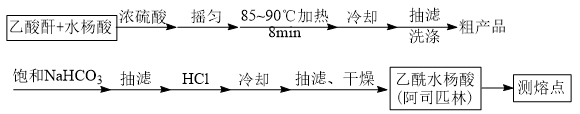
主要试剂和产品的物理常数
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是_______ 。
(2)写出制备阿司匹林的化学方程式_______ 。
(3)①合成阿斯匹林时,最合适的加热方法是_______ 。
②抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是_______ 。
(4)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤,则加饱和NaHCO3溶液的目的是_________ 。
另一种改进的提纯方法,称为重结晶提纯法。方法如下:
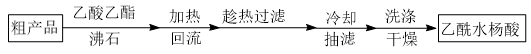
(5)改进的提纯方法中加热回流的装置如图所示,

①使用温度计的目的是_______ ,冷凝水的流进方向是_______ (填“b”或“c”)。
②重结晶提纯法所得产品的有机杂质要比原方案少的原因是_______ 。
(6)检验产品中是否含有水杨酸的化学方法是_______ 。
(7)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称量产品m=2.2g,则所得乙酰水杨酸的产率为_______ 。
 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135°C.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135°C.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
主要试剂和产品的物理常数
| 名称 | 相对分子质量 | 熔点或沸点(°C) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是
(2)写出制备阿司匹林的化学方程式
(3)①合成阿斯匹林时,最合适的加热方法是
②抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是
(4)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤,则加饱和NaHCO3溶液的目的是
另一种改进的提纯方法,称为重结晶提纯法。方法如下:
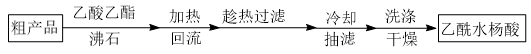
(5)改进的提纯方法中加热回流的装置如图所示,

①使用温度计的目的是
②重结晶提纯法所得产品的有机杂质要比原方案少的原因是
(6)检验产品中是否含有水杨酸的化学方法是
(7)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称量产品m=2.2g,则所得乙酰水杨酸的产率为
2012高二·浙江·竞赛 查看更多[1]
更新时间:2021-08-02 21:59:38
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
【推荐1】G 是一种合成橡胶和树脂的重要原料,用 合成 G 的转化关系如图所示。
合成 G 的转化关系如图所示。

已知:①(RCO)2O 2RCOOH;
2RCOOH;
②RCOOH RCH2OH(其中 R 是烃基);
RCH2OH(其中 R 是烃基);
③F 的核磁共振氢谱有3 组峰,峰面积之比为 2∶2∶3。
请回答以下问题:
(1)A 的分子式为______ ;B 中含氧官能团的名称是______ 。
(2)②的反应类型是______ ;⑥的反应类型是______ 。
(3)E 的结构简式为______ 。
(4)G分子中最多有______ 个原子共平面。G 与 Br2 的 CCl4 溶液反应,所有可能的产物共有______ 种。
(5)反应⑥的化学方程式为______ 。
 合成 G 的转化关系如图所示。
合成 G 的转化关系如图所示。
已知:①(RCO)2O
 2RCOOH;
2RCOOH;②RCOOH
 RCH2OH(其中 R 是烃基);
RCH2OH(其中 R 是烃基);③F 的核磁共振氢谱有3 组峰,峰面积之比为 2∶2∶3。
请回答以下问题:
(1)A 的分子式为
(2)②的反应类型是
(3)E 的结构简式为
(4)G分子中最多有
(5)反应⑥的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某种药物中间体H的一种合成路线如下(部分反应条件略去):
(1)E中官能团的名称为___________ 。
(2)A→B的反应类型是___________ 。
(3)F的结构简式为_____________ 。
(4)写出一种能同时满足下列条件的B的同分异构体结构简式:____________ 。
①含有苯环;②能发生银镜反应;③核磁共振氢谱有4组峰。
(5)KMnO4可以用于氧化甲苯制苯甲酸,得到的粗苯甲酸中会含有少量KCl、MnO2等杂质,可以用重结晶法提纯,完成实验过程:将1.0g粗苯甲酸放入100mL烧杯,加入50mL蒸馏水,______________ 。
已知:氯化钾、苯甲酸在水中的溶解度如下:
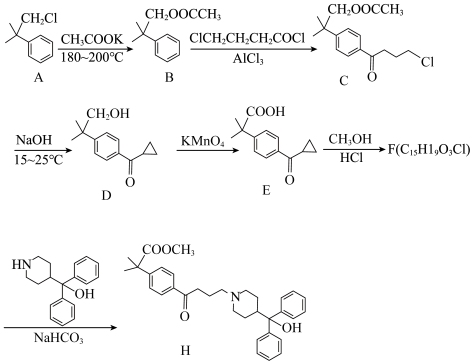
(1)E中官能团的名称为
(2)A→B的反应类型是
(3)F的结构简式为
(4)写出一种能同时满足下列条件的B的同分异构体结构简式:
①含有苯环;②能发生银镜反应;③核磁共振氢谱有4组峰。
(5)KMnO4可以用于氧化甲苯制苯甲酸,得到的粗苯甲酸中会含有少量KCl、MnO2等杂质,可以用重结晶法提纯,完成实验过程:将1.0g粗苯甲酸放入100mL烧杯,加入50mL蒸馏水,
已知:氯化钾、苯甲酸在水中的溶解度如下:
| 温度/℃ | 20 | 40 | 60 | 80 | 90 |
| S氯化钾/g | 34.2 | 40.1 | 45.8 | 51.3 | 53.9 |
| S苯甲酸/g | 0.29 | 0.60 | 1.20 | 2.75 | 4.60 |
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】有机物I是一种新合成药的主要成分,可用于治疗神经衰弱等障碍性疾病。一种合成有机物I的路线如图所示。
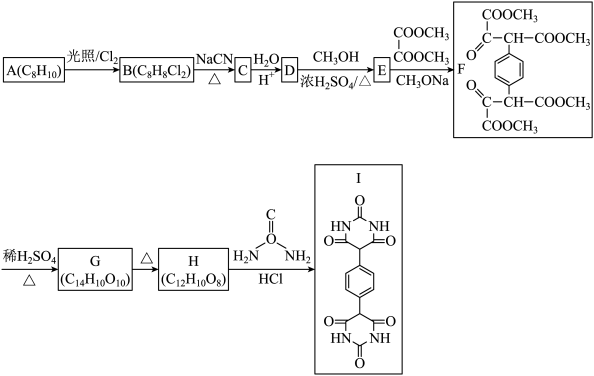
已知:①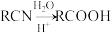 ②
②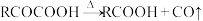
回答下列问题:
(1)A的名称为_______ ,G中所含官能团的名称为_______ ,D→E的反应类型为_______ 。
(2)E的结构简式为_______ ,I的分子式为_______ 。
(3)写出B→C的化学方程式:_______ 。
(4)B的同分异构体有多种,其中苯环上有两个取代基的B的同分异构体有_______ 种(不包括立体异构,不含B本身)。
(5)设计以 和
和 为原料合成
为原料合成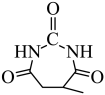 的路线(无机试剂任选)。
的路线(无机试剂任选)。_______

已知:①
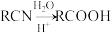 ②
②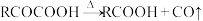
回答下列问题:
(1)A的名称为
(2)E的结构简式为
(3)写出B→C的化学方程式:
(4)B的同分异构体有多种,其中苯环上有两个取代基的B的同分异构体有
(5)设计以
 和
和 为原料合成
为原料合成 的路线(无机试剂任选)。
的路线(无机试剂任选)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】苯乙酮(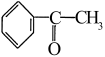 )广泛用于皂用香精和烟草香精中,实验室可用苯和乙酸酐(
)广泛用于皂用香精和烟草香精中,实验室可用苯和乙酸酐(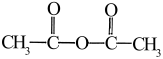 ,遇水生成乙酸)在无水AlCl3作用下制取,操作如下:
,遇水生成乙酸)在无水AlCl3作用下制取,操作如下:
步骤一:在A中加入30mL干燥的苯和30g无水AlCl3粉末,在剧烈搅拌下,缓慢滴入7mL乙酸酐,控制反应温度为30℃,反应过程中释放出HCl气体,HCl释放停止后,再加热至90~95℃,回流反应1h,形成黑黄色液体。装置如图所示。
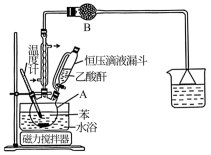
步骤二:将冷却后的反应瓶置于冰水浴中(如图所示),加入15mL苯,慢慢加入混合的盐酸冰水,静置分层,分液,无机相用乙醚萃取,与有机相合并,有机相用10%NaOH液洗涤,分液,弃去无机层,有机层用9mL水洗,分液,弃去无机层,有机层用MgSO4干燥。
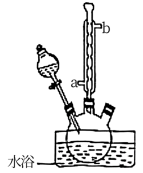
步骤三:分离提纯苯乙酮。
回答下列问题:
(1)仪器A的名称是___________ 。恒压滴液漏斗的作用是___________ 。
(2)写出苯与乙酸酐生成苯乙酮的化学方程式:______ 。
(3)仪器B中盛装无水CaCl2,其作用是___________ 。
(4)步骤二中多次使用到的操作是___________ 、___________ 。
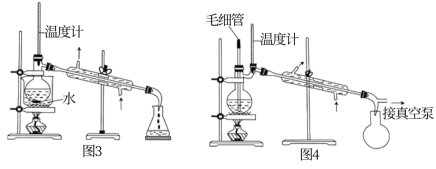
(5)已知常压下:
则步骤三分离提纯苯乙酮使用的操作是___________ ;为了收集纯净的苯乙酮馏分,分离苯乙酮应使用下面的图___________ 装置。(填数字)
 )广泛用于皂用香精和烟草香精中,实验室可用苯和乙酸酐(
)广泛用于皂用香精和烟草香精中,实验室可用苯和乙酸酐( ,遇水生成乙酸)在无水AlCl3作用下制取,操作如下:
,遇水生成乙酸)在无水AlCl3作用下制取,操作如下:步骤一:在A中加入30mL干燥的苯和30g无水AlCl3粉末,在剧烈搅拌下,缓慢滴入7mL乙酸酐,控制反应温度为30℃,反应过程中释放出HCl气体,HCl释放停止后,再加热至90~95℃,回流反应1h,形成黑黄色液体。装置如图所示。

步骤二:将冷却后的反应瓶置于冰水浴中(如图所示),加入15mL苯,慢慢加入混合的盐酸冰水,静置分层,分液,无机相用乙醚萃取,与有机相合并,有机相用10%NaOH液洗涤,分液,弃去无机层,有机层用9mL水洗,分液,弃去无机层,有机层用MgSO4干燥。

步骤三:分离提纯苯乙酮。
回答下列问题:
(1)仪器A的名称是
(2)写出苯与乙酸酐生成苯乙酮的化学方程式:
(3)仪器B中盛装无水CaCl2,其作用是
(4)步骤二中多次使用到的操作是
(5)已知常压下:
| 熔点/℃ | 沸点/℃ | |
| 苯 | 5.5 | 80.1 |
| 乙醚 | -116.3 | 34.6 |
| 苯乙酮 | 19.6 | 202 |

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】葡萄糖酸锌[Zn(C6H11O7)2]是一种有机补锌剂,广泛应用于食药领域。已知葡萄糖酸锌能溶于水,易溶于热水,不溶于乙醇,稍高于100℃即开始分解。某小组由葡萄糖制备葡萄糖酸锌的实验步骤如下:
Ⅰ.制备葡萄糖酸(C6H12O7):60℃水浴下,向一定体积葡萄糖溶液中滴入1%溴水至略过量,保温5min。
Ⅱ.制备葡萄糖酸钙[Ca(C6H11O7)2]:将略过量高纯CaCO3粉末缓慢加入上述溶液,在水浴中振荡,直至无气泡产生。过滤,冷却并加入等体积乙醇,产生沉淀。过滤,用乙醇洗涤固体,溶水待用。
Ⅲ.制备葡萄糖酸锌粗品:在90℃水浴、搅拌下,向ZnSO4溶液中分批加入葡萄糖酸钙溶液。趁热过滤,向滤液中加入无水乙醇并冷却析晶,过滤。
请回答下列问题:
(1)步骤Ⅰ中发生反应的化学方程式为___________ 。
(2)步骤Ⅲ中反应控温在90℃的原因为___________ 。
(3)步骤Ⅲ中向滤液中加入无水乙醇的作用是___________ 。
(4)高纯CaCO3的制备。请设计以石灰石(含少量铁的氧化物,其他杂质不考虑)、盐酸,碳酸铵溶液为原料制备高纯碳酸钙的实验方案:边搅拌边将石灰石粉末分批加入稀盐酸中,至不再有气泡产生,___________ ,得到高纯CaCO3。(实验中须使用的试剂有:氨水、H2O2溶液、HNO3溶液、AgNO3溶液)
Ⅰ.制备葡萄糖酸(C6H12O7):60℃水浴下,向一定体积葡萄糖溶液中滴入1%溴水至略过量,保温5min。
Ⅱ.制备葡萄糖酸钙[Ca(C6H11O7)2]:将略过量高纯CaCO3粉末缓慢加入上述溶液,在水浴中振荡,直至无气泡产生。过滤,冷却并加入等体积乙醇,产生沉淀。过滤,用乙醇洗涤固体,溶水待用。
Ⅲ.制备葡萄糖酸锌粗品:在90℃水浴、搅拌下,向ZnSO4溶液中分批加入葡萄糖酸钙溶液。趁热过滤,向滤液中加入无水乙醇并冷却析晶,过滤。
请回答下列问题:
(1)步骤Ⅰ中发生反应的化学方程式为
(2)步骤Ⅲ中反应控温在90℃的原因为
(3)步骤Ⅲ中向滤液中加入无水乙醇的作用是
(4)高纯CaCO3的制备。请设计以石灰石(含少量铁的氧化物,其他杂质不考虑)、盐酸,碳酸铵溶液为原料制备高纯碳酸钙的实验方案:边搅拌边将石灰石粉末分批加入稀盐酸中,至不再有气泡产生,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】苯甲酸又称安息香酸(C6H5COOH),可用于合成纤维、树脂涂料等也可作为药物或防腐剂使用,有抑制真菌、细菌生长的作用。实验室中由甲苯制备苯甲酸的实验如下:
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
实验步骤:
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4 5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
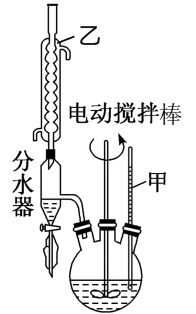
第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)
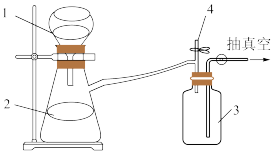
第三步:粗产品用水洗涤2到3次,干燥称量得固体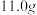 .
.
请回答下列问题:
(1)图1中装置乙的名称为___ 。
(2)分水器的作用是分离出水其主要目的是___ ,判断该反应进行完全的实验现象是___ 。
(3)实验第二步中,趁热过滤的原因是___ ,采用抽滤的优点是____ 。停止抽滤时先旋开图2中4处的旋塞恢复常压,然后关闭抽气泵,装置3起到的作用是____ 。
(4)第三步证明粗产品洗涤干净的方法是___ 。
(5)苯甲酸的产率为____ 。
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为__ 。
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
| 相对分子质量 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) | |
| 苯甲酸 | 122 | 122.4 | 249 | 1.3 |
| 甲苯 | 92 | -95 | 110.6 | 0.9 |
实验步骤:
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4
 5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)

第三步:粗产品用水洗涤2到3次,干燥称量得固体
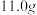 .
.请回答下列问题:
(1)图1中装置乙的名称为
(2)分水器的作用是分离出水其主要目的是
(3)实验第二步中,趁热过滤的原因是
(4)第三步证明粗产品洗涤干净的方法是
(5)苯甲酸的产率为
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学学习小组在实验室制备无水三氯化铁,其实验装置如图。三氯化铁是棕黄色、易潮解、100℃能升华的物质。
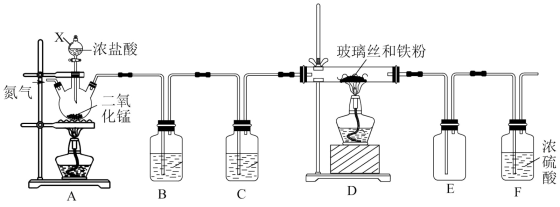
回答下列问题:
(1)装置A中三颈烧瓶里反应的离子方程式是_______ 。
(2)为得到纯净、干燥的Cl2,B、C中的试剂分别为_______ 、_______ 。
(3)实验开始前先通氮气的目的是_______ 。
(4)为使氯气与铁充分反应,应注意的操作是_______ 。
(5)请你评价该装置的主要缺点是_______ 。
(6)设计实验证明D中反应产物中一定含有Fe3+:(要求有试剂、现象和操作)_______ 。

回答下列问题:
(1)装置A中三颈烧瓶里反应的离子方程式是
(2)为得到纯净、干燥的Cl2,B、C中的试剂分别为
(3)实验开始前先通氮气的目的是
(4)为使氯气与铁充分反应,应注意的操作是
(5)请你评价该装置的主要缺点是
(6)设计实验证明D中反应产物中一定含有Fe3+:(要求有试剂、现象和操作)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】锂被誉为“新能源金属”、“金属味精”和“推动世界前进的金属”,具有极高的战略价值。碳酸锂是生产金属锂制品的基础材料,以β-锂辉石为原料,用硫酸焙烧法制取碳酸锂的工艺流程(部分试剂和步骤等已略去)如下。
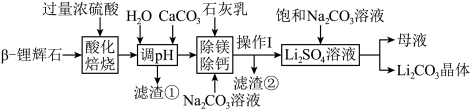
【资料】
①β-锂辉石的主要成分是 ,含少量Ca、Mg元素。
,含少量Ca、Mg元素。
②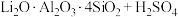 (浓)
(浓)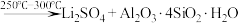 。
。
(1)工业上将β-锂辉石磨至粒径为0.125mm左右,再送入酸化炉的原因是___________ 。
(2)浓硫酸用量不宜过量太多,原因可能是___________ 。
(3)写出“酸化焙烧”步骤中氧化锂发生反应的化学方程式___________ 。
(4)操作Ⅰ的名称为___________ ,滤渣②的成分是___________ 。
(5)在“除镁除钙”步骤中,先加入石灰乳,再加入 溶液。添加试剂的顺序不能调换,其原因是
溶液。添加试剂的顺序不能调换,其原因是___________ 。
(6)母液中的溶质是___________ 。
(7) 和
和 的溶解度如表所示:
的溶解度如表所示:
为了提高产品的纯度,需要将得到的晶体洗涤,需选用___________ ℃的水;证明 晶体洗涤干净的方法操作是
晶体洗涤干净的方法操作是___________ 。

【资料】
①β-锂辉石的主要成分是
 ,含少量Ca、Mg元素。
,含少量Ca、Mg元素。②
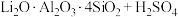 (浓)
(浓)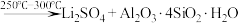 。
。(1)工业上将β-锂辉石磨至粒径为0.125mm左右,再送入酸化炉的原因是
(2)浓硫酸用量不宜过量太多,原因可能是
(3)写出“酸化焙烧”步骤中氧化锂发生反应的化学方程式
(4)操作Ⅰ的名称为
(5)在“除镁除钙”步骤中,先加入石灰乳,再加入
 溶液。添加试剂的顺序不能调换,其原因是
溶液。添加试剂的顺序不能调换,其原因是(6)母液中的溶质是
(7)
 和
和 的溶解度如表所示:
的溶解度如表所示:| T/℃ | 20 | 40 | 60 | 80 |
S( )/g )/g | 1.33 | 1.17 | 1.01 | 0.85 |
S( )/g )/g | 34.2 | 32.8 | 31.9 | 30.7 |
 晶体洗涤干净的方法操作是
晶体洗涤干净的方法操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室利用下列装置可以准备FeCl3(加热、夹持装置和固定装置已略去)。圆底烧瓶中盛装KMnO4,分液漏斗中盛装浓盐酸,B中盛装纯铁粉。已知信息:①FeCl3的熔点为306℃,沸点为315℃。②FeCl3遇水蒸气会产生白雾。请回答下列问题:
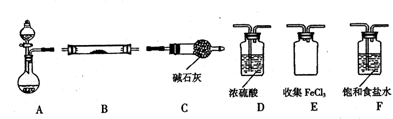
(1)检查A装置气密性的操作方法是 。
(2)按气流由左向右流动的方向为A→( )→( )→( )→( )→( )相连进行实验。
(3)C装置的作用是 。
(4)用0.2mol的高锰酸钾固体和足量的浓盐酸完全反应后,得到标准状况下氯气的体积为11.2L,则含锰元素的生成物中锰元素的化合价为 。
(5)写出A装置中发生反应的化学方程式,并标出电子转移的方向和数目 。
(6)检验产品中是否含有FeCl2的实验方案为 。
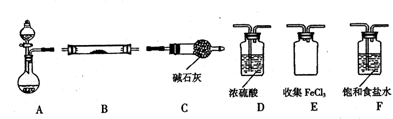
(1)检查A装置气密性的操作方法是 。
(2)按气流由左向右流动的方向为A→( )→( )→( )→( )→( )相连进行实验。
(3)C装置的作用是 。
(4)用0.2mol的高锰酸钾固体和足量的浓盐酸完全反应后,得到标准状况下氯气的体积为11.2L,则含锰元素的生成物中锰元素的化合价为 。
(5)写出A装置中发生反应的化学方程式,并标出电子转移的方向和数目 。
(6)检验产品中是否含有FeCl2的实验方案为 。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下: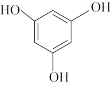 +2CH3OH
+2CH3OH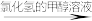
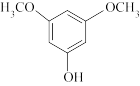 +2H2O。
+2H2O。
甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是____ 。
②萃取用到的分液漏斗使用前需____ 并洗净,分液时有机层在分液漏斗的____ (填“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是____ 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是____ (填字母)。
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
 +2CH3OH
+2CH3OH
 +2H2O。
+2H2O。甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/g·cm-3 | 溶解性 |
| 甲醇 | 64.7 | 0.7915 | 易溶于水 | |
| 乙醚 | 34.5 | 0.7138 | 微溶于水 | |
| 3,5-二甲氧基苯酚 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
①分离出甲醇的操作是
②萃取用到的分液漏斗使用前需
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】生于110年前的德国化学家GeorgWittig,1954年发现了广泛用于有机合成的Wittig反应,为此获得1979年诺贝尔化学奖。下面就是与Wittig有关的反应:
CH3CH2OH CH3CH2Br
CH3CH2Br B
B C
C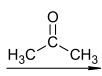 D+E
D+E
上面的反应产物中D是一种烯烃,画出试剂或中间体A、B、C、D、E的结构,并给出D的名称:A_______ 、B_______ 、C_______ 、D_______ 、_______ 、E_______ 。
CH3CH2OH
 CH3CH2Br
CH3CH2Br B
B C
C D+E
D+E上面的反应产物中D是一种烯烃,画出试剂或中间体A、B、C、D、E的结构,并给出D的名称:A
您最近一年使用:0次