苯甲酸又称安息香酸(C6H5COOH),可用于合成纤维、树脂涂料等也可作为药物或防腐剂使用,有抑制真菌、细菌生长的作用。实验室中由甲苯制备苯甲酸的实验如下:
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
实验步骤:
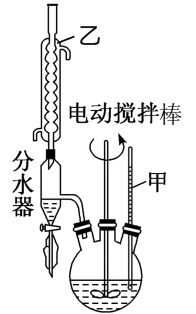
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4 5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
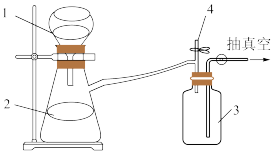
第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)
第三步:粗产品用水洗涤2到3次,干燥称量得固体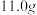 .
.
请回答下列问题:
(1)图1中装置乙的名称为___ 。
(2)分水器的作用是分离出水其主要目的是___ ,判断该反应进行完全的实验现象是___ 。
(3)实验第二步中,趁热过滤的原因是___ ,采用抽滤的优点是____ 。停止抽滤时先旋开图2中4处的旋塞恢复常压,然后关闭抽气泵,装置3起到的作用是____ 。
(4)第三步证明粗产品洗涤干净的方法是___ 。
(5)苯甲酸的产率为____ 。
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为__ 。
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。
查阅资料:
①苯甲酸是一元有机弱酸不易被氧化。在水中溶解度:0.35g(25℃)、2.7g(80℃)、5.9g(100℃)。甲苯易溶于有机溶剂,不溶于水。
②
| 相对分子质量 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) | |
| 苯甲酸 | 122 | 122.4 | 249 | 1.3 |
| 甲苯 | 92 | -95 | 110.6 | 0.9 |
实验步骤:
第一步:将9.2g甲苯和硫酸酸化的KMnO4溶液(过量)置于如图的三颈烧瓶中,加热保持反应物溶液温度在90℃左右至反应结束,主要反应为5C6H5CH3+6KMnO4+9H2SO4
 5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
5C6H5COOH+3K2SO4+4MnSO4+14H2O,制备过程中不断从分水器分离出水;
第二步:将反应后混合液趁热过滤滤液冷却后用硫酸酸化用如图装置抽滤得粗产品;(抽滤又称减压过滤利用抽气泵使抽滤瓶中的压强降低达到固液分离的目的。)

第三步:粗产品用水洗涤2到3次,干燥称量得固体
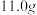 .
.请回答下列问题:
(1)图1中装置乙的名称为
(2)分水器的作用是分离出水其主要目的是
(3)实验第二步中,趁热过滤的原因是
(4)第三步证明粗产品洗涤干净的方法是
(5)苯甲酸的产率为
(6)结合下列试剂和用品设计最简单实验验证苯甲酸是弱酸,具体操作为
0.010mol·L-1的苯甲酸溶液;0.010mol·L-1的苯甲酸钠溶液;0.010mol·L-1的氢氧化钠溶液;0.010mol·L-1的盐酸溶液;广泛pH试纸;甲基橙,酚酞(仪器任选)。
更新时间:2020-06-09 14:23:51
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是石蜡油在炽热碎瓷片的作用下分解产生某种气体,并验证其性质的装置:

回答下列问题:
(1)该气体可以衡量一个国家的石油化工生产水平,该气体的结构简式是___________ 。发生聚合反应的化学方程式_____________________________________ 。
(2)B中酸性高锰酸钾溶液和C中溴的四氯化碳溶液都褪色,说明该气体能被酸性高锰酸钾______ 。在C中发生的化学反应方程式为______________ ,反应类型为_________ 。
(3)该气体通过一系列反应可以得到乙炔,写出实验室制取乙炔的化学方程式:______________________________________ 。
(4)由乙炔可以制取甲苯,甲苯一溴代物的同分异构体有________ 种,其中对溴甲苯的结构简式为__________________ 。
(5)甲苯可用于制造烈性炸药TNT,该反应的化学方程式为______________________ 。

回答下列问题:
(1)该气体可以衡量一个国家的石油化工生产水平,该气体的结构简式是
(2)B中酸性高锰酸钾溶液和C中溴的四氯化碳溶液都褪色,说明该气体能被酸性高锰酸钾
(3)该气体通过一系列反应可以得到乙炔,写出实验室制取乙炔的化学方程式:
(4)由乙炔可以制取甲苯,甲苯一溴代物的同分异构体有
(5)甲苯可用于制造烈性炸药TNT,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学设计如图所示装置制备一硝基甲苯
甲苯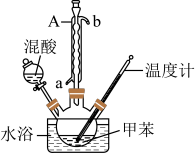
已知.30℃左右主要产物为一硝基甲苯,温度过高时会生成二硝基甲苯和三硝基甲苯。
实验步骤如下.
①配制浓硫酸和浓硝酸(按体积比1.3)的混合物(混酸)
②在三颈瓶里装15ml甲苯
③装好其它药品,并组装好仪器
④向三颈烧瓶中加入混酸,并不断搅拌
⑤控制温度,大约反应10min至三颈烧瓶底有大量液体(淡黄色油状)出现
⑥分离出一硝基甲苯。(已知.甲苯的密度为0.866g/ml,沸点为110.6℃,硝基苯的密度为1.20g/ml,沸点为210.9℃)
根据上述实验,回答下列问题
(1)实验方案中缺少一个必要的仪器,它是___________ 。本实验的关键是控制温度在30℃左右在,如果温度过高,产生的后果是_____________________________________ 。
(2)简述配制混酸的方法_______________________________________________________ ,浓硫酸的作用是______________________________ 。
(3)A仪器的名称是_________________ 进水口是________________ 。
(4)写出甲苯与混酸反应生成间硝基甲苯的化学方程式___________________________ 。
(5)分离产品方案如图所示
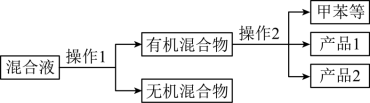
操作2的名称是_________________ 。
(6)经测定,产品1为一硝基甲苯,其核磁共拜氢谱中有3个峰,则其结构简式为_________________ 。
甲苯

已知.30℃左右主要产物为一硝基甲苯,温度过高时会生成二硝基甲苯和三硝基甲苯。
实验步骤如下.
①配制浓硫酸和浓硝酸(按体积比1.3)的混合物(混酸)
②在三颈瓶里装15ml甲苯
③装好其它药品,并组装好仪器
④向三颈烧瓶中加入混酸,并不断搅拌
⑤控制温度,大约反应10min至三颈烧瓶底有大量液体(淡黄色油状)出现
⑥分离出一硝基甲苯。(已知.甲苯的密度为0.866g/ml,沸点为110.6℃,硝基苯的密度为1.20g/ml,沸点为210.9℃)
根据上述实验,回答下列问题
(1)实验方案中缺少一个必要的仪器,它是
(2)简述配制混酸的方法
(3)A仪器的名称是
(4)写出甲苯与混酸反应生成间硝基甲苯的化学方程式
(5)分离产品方案如图所示

操作2的名称是
(6)经测定,产品1为一硝基甲苯,其核磁共拜氢谱中有3个峰,则其结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】一种合成解热镇痛类药物布洛芬方法如下:

(1)A的名称是___________ ,C中所含官能团名称为___________ 。
(2)C→D 的反应类型为___________ 。
(3)从组成和结构特点的角度分析 C 与 E 的关系为___________ 。
(4)合成B实验现象是产生白雾和刺激性气味,写出A→B的反应方程式___________ 。
(5)写出一种满足以下条件的布洛芬H的同分异构体:___________ 。
① 1 mol 该物质与浓溴水反应时最多消耗 4 mol Br2;
② 分子中含有 6 种不同化学环境的氢原子。
(6)请写出以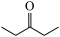 和
和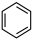 为原料制备
为原料制备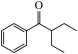 的合成路线流程图(无机试剂和有机溶剂任选)
的合成路线流程图(无机试剂和有机溶剂任选)___________ 。

(1)A的名称是
(2)C→D 的反应类型为
(3)从组成和结构特点的角度分析 C 与 E 的关系为
(4)合成B实验现象是产生白雾和刺激性气味,写出A→B的反应方程式
(5)写出一种满足以下条件的布洛芬H的同分异构体:
① 1 mol 该物质与浓溴水反应时最多消耗 4 mol Br2;
② 分子中含有 6 种不同化学环境的氢原子。
(6)请写出以
 和
和 为原料制备
为原料制备 的合成路线流程图(无机试剂和有机溶剂任选)
的合成路线流程图(无机试剂和有机溶剂任选)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】乙酸正丁酯有愉快的果香气味,可用于香料工业,它的一种合成步骤如下:
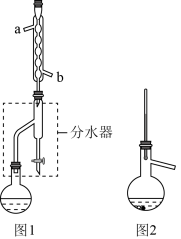
I.合成:在干燥的圆底烧瓶中加11.5 mL(9.3 g,0.125 mol)正丁醇、7.2 mL(7.5 g,0.125 mol)冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器中预先加入5.00 mL水,其水面低于分水器回流支管下沿3~5 mm,然后用小火加热,反应大约40 min。
①当分水器中的液面不再升高时,冷却,放出分水器中的水,把反应后的溶液与分水器中的酯层合并,转入分液漏斗中,用10 mL10%的碳酸钠溶液洗至酯层无酸性,充分振荡后静置,分去水层。
②将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥(生成MgSO4·7H2O晶体)。
③将乙酸正丁酯粗产品转入 50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。主要试剂及产物的物理常数如下:
制备过程中还可能发生的副反应有:2 CH3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
根据以上信息回答下列问题:
(1)写出合成乙酸正丁酯的化学方程式___________ 。
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从___________ (填“a”或“b”)管口通入。
(3)分离提纯步骤①中的碳酸钠溶液的作用主要是除去___________ 。
(4)在步骤②后(即酯层用无水硫酸镁干燥后),应先进行___________ (填实验揉作名称),再将乙酸正丁酯粗产品转入蒸馏烧瓶中。
(5)步骤③中常压蒸馏装置如图2所示,应收集___________ ℃左右的馏分,则收集到的产品中可能混有___________ 杂质。
(6)反应结束后,若放出的水为6.98 mL(水的密度为l g · mL-1),则正丁醇的转化率为___________ (精确到1%)。
I.合成:在干燥的圆底烧瓶中加11.5 mL(9.3 g,0.125 mol)正丁醇、7.2 mL(7.5 g,0.125 mol)冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器中预先加入5.00 mL水,其水面低于分水器回流支管下沿3~5 mm,然后用小火加热,反应大约40 min。
①当分水器中的液面不再升高时,冷却,放出分水器中的水,把反应后的溶液与分水器中的酯层合并,转入分液漏斗中,用10 mL10%的碳酸钠溶液洗至酯层无酸性,充分振荡后静置,分去水层。
②将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥(生成MgSO4·7H2O晶体)。
③将乙酸正丁酯粗产品转入 50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。主要试剂及产物的物理常数如下:
| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度/g· mL-1 | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
| 在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
 CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O根据以上信息回答下列问题:
(1)写出合成乙酸正丁酯的化学方程式
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从
(3)分离提纯步骤①中的碳酸钠溶液的作用主要是除去
(4)在步骤②后(即酯层用无水硫酸镁干燥后),应先进行
(5)步骤③中常压蒸馏装置如图2所示,应收集
(6)反应结束后,若放出的水为6.98 mL(水的密度为l g · mL-1),则正丁醇的转化率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室制备1,2-二溴乙烷的原理:
CH3CH2OH CH2=CH2↑+H2O
CH2=CH2↑+H2O
CH2=CH2+Br2→BrCH2CH2Br
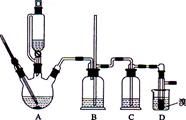
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
有关数据列表如下:
(1)在反应中若加热后发现未加沸石,应采取的正确方法是________________ ;判断该制备反应已经结束的最简单方法是_________________ 。
(2)装置C中应加入______________ ,吸收反应中产生的某些有影响的杂质气体(填写正确选项前的字母)
a.水 b.浓硫酸 c.NaOH溶液 d.KMnO4溶液
(3)装置B中竖直的长导管起安全管的作用,其原理是_____________ 。
(4)若产物中有少量Br2,最好用_________ 洗涤除去(填写正确选项前的字母)
a.水 b.乙醇 c.KI溶液 d.NaHSO3溶液
发生反应的化学方程为____________________ 。
(5)若产物中有少量副产物乙醚,可用__________ 的方法除去。
(6)反应过程中应用冷水冷却装置D,主要目的是__________________ ,但又不能过度冷却(如用冰水),其原因是_________________ 。
CH3CH2OH
 CH2=CH2↑+H2O
CH2=CH2↑+H2OCH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm -3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(2)装置C中应加入
a.水 b.浓硫酸 c.NaOH溶液 d.KMnO4溶液
(3)装置B中竖直的长导管起安全管的作用,其原理是
(4)若产物中有少量Br2,最好用
a.水 b.乙醇 c.KI溶液 d.NaHSO3溶液
发生反应的化学方程为
(5)若产物中有少量副产物乙醚,可用
(6)反应过程中应用冷水冷却装置D,主要目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】增塑剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,实验装置(部分装置省略)如图甲,实验原理如图乙。已知:邻苯二甲酸二丁酯是无色透明、具有芳香气味的油状液体,酸性条件下,温度超过180℃时易发生分解。
可能用到的有关数据如下:

实验步骤:①向三颈烧瓶内加入7.4g邻苯二甲酸酐、12.2g正丁醇、少量浓硫酸和碎瓷片。
②加热,搅拌,反应约2小时。
③冷却至室温,将反应后混合物倒出,洗涤,分液得到粗产品。
④粗产品加无水硫酸镁处理,过滤,蒸馏。
⑤称量,得产品9.0g。
请回答下列问题:
(1)仪器a的名称_______ ,碎瓷片作用_______ 。
(2)步骤②加热温度不宜超过180℃,主要原因是_______ 。
(3)反应过程中可能产生的有机副产物_______ 。(写一种)
(4)反应Ⅰ进行得迅速而完全,反应Ⅱ是可逆反应,进行得较缓慢,为提高反应Ⅱ的转化率,不宜采取的措施是_______ 。 (填序号)
A.分离出水 B.增加正丁醇的量 C.增大压强
(5)洗涤操作中,用碳酸钠溶液洗涤,碳酸钠溶液作用是_______ 。
(6)无水硫酸镁的作用是_______ 。
(7)本实验中,邻苯二甲酸二丁酯的产率为_______ 。(保留三位有效数字)
可能用到的有关数据如下:
| 相对分子质量 | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 正丁醇 | 74 | -89 | 118 | 微溶于水 |
| 邻苯二甲酸酐 | 148 | 130 | 284 | 难溶于水 |
| 邻苯二甲酸二丁酯 | 278 | -35 | 340 | 难溶于水 |

实验步骤:①向三颈烧瓶内加入7.4g邻苯二甲酸酐、12.2g正丁醇、少量浓硫酸和碎瓷片。
②加热,搅拌,反应约2小时。
③冷却至室温,将反应后混合物倒出,洗涤,分液得到粗产品。
④粗产品加无水硫酸镁处理,过滤,蒸馏。
⑤称量,得产品9.0g。
请回答下列问题:
(1)仪器a的名称
(2)步骤②加热温度不宜超过180℃,主要原因是
(3)反应过程中可能产生的有机副产物
(4)反应Ⅰ进行得迅速而完全,反应Ⅱ是可逆反应,进行得较缓慢,为提高反应Ⅱ的转化率,不宜采取的措施是
A.分离出水 B.增加正丁醇的量 C.增大压强
(5)洗涤操作中,用碳酸钠溶液洗涤,碳酸钠溶液作用是
(6)无水硫酸镁的作用是
(7)本实验中,邻苯二甲酸二丁酯的产率为
您最近一年使用:0次



