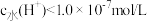常温下,在烧杯中将0.025 mol  粉末加水配成1 L悬浊液,然后向烧杯中加入
粉末加水配成1 L悬浊液,然后向烧杯中加入 固体并充分搅拌(忽略溶液体积的变化)。加入
固体并充分搅拌(忽略溶液体积的变化)。加入 固体的过程中溶液中几种离子的浓度变化曲线如图。下列说法正确的是
固体的过程中溶液中几种离子的浓度变化曲线如图。下列说法正确的是
 粉末加水配成1 L悬浊液,然后向烧杯中加入
粉末加水配成1 L悬浊液,然后向烧杯中加入 固体并充分搅拌(忽略溶液体积的变化)。加入
固体并充分搅拌(忽略溶液体积的变化)。加入 固体的过程中溶液中几种离子的浓度变化曲线如图。下列说法正确的是
固体的过程中溶液中几种离子的浓度变化曲线如图。下列说法正确的是
A.常温下,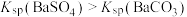 |
B. 在水中的溶解度、 在水中的溶解度、 均比在 均比在 溶液中的大 溶液中的大 |
C.MP曲线表示的是溶液中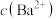 的变化 的变化 |
D. 恰好全部转化为 恰好全部转化为 时,离子浓度大小关系为 时,离子浓度大小关系为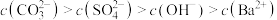 |
更新时间:2024-05-26 09:58:12
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列实验现象和结论正确的是
| 选项 | 实验目的 | 实验操作 | 实验现象、结论 |
| A | 探究盐类水解程度 | 常温下,用pH计测得0.1mol•L-1弱酸盐NaHA、NaB、Na2A溶液pH值为a、b、c | 若c>b>a,则水解程度:A2->B->HA- |
| B | 实现沉淀的转化 | 向1mL0.1mol•L-1NaOH溶液中滴入2滴0.1mol•L-1MgCl2溶液,再滴入2滴0.1mol•L-1CuSO4溶液 | 若白色沉淀→蓝色沉淀,则Ksp:Cu(OH)2<Mg(OH)2 |
| C | 验证乙炔化学性质 | 将电石与饱和食盐水反应生成的气体通入酸性KMnO4溶液中 | 若紫红色褪去,则证明乙炔能使KMnO4溶液褪色 |
| D | 卤代烃中卤原子的检验 | 有机物A加入到NaOH乙醇溶液中,充分加热:冷却后,取混合液加足量硝酸酸化后滴加AgNO3溶液 | 若不产生浅黄色沉淀,则有机物A也可能为溴代烃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温时,改变饱和氯水的pH,得到部分含氯微粒的物质的量分数与pH的关系如图所示。下列叙述不正确 的是
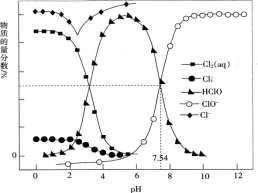

| A.氯水中的Cl2、ClO-、HClO均能与KI发生反应 |
B.常温下反应Cl2(aq)+Cl-(aq)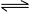 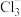 (aq)的K=0.191,当pH增大时,K减小 (aq)的K=0.191,当pH增大时,K减小 |
C.pH=1的氯水中,c(Cl2)>c(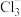 )>c(HClO)>c(ClO-) )>c(HClO)>c(ClO-) |
D.该温度下,HClO H++ClO-的电离常数Ka的对值lgKa=-7.54 H++ClO-的电离常数Ka的对值lgKa=-7.54 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列实验操作对应的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向一定浓度的CuSO4溶液中通入适量H2S气体 | 出现黑色沉淀 | H2S的酸性比H2SO4强 |
| B | 向4mL0.01mol·L-1KMnO4酸性溶液中分别加入2mL0.1mol·L-1H2C2O4溶液和2mL0.2mol·L-1H2C2O4溶液 | 后者褪色所需时间短 | 反应物浓度越大,反应速率越快 |
| C | 将铜粉加入1.0mol·L-1Fe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 说明金属铁比铜活泼 |
| D | 把Cl2和SO2分别通入到盛有石蕊溶液的试 管中 | 两个试管中的溶液,均先变红再褪色 | Cl2和SO2均具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25℃时,5种银盐的溶度积常数(Ksp)分别是:
下列说法正确的是
| AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
| A.氯化银、溴化银和碘化银的溶解度依次增大 |
| B.将硫酸银溶解于水后,向其中加入少量硫化钠固体,不能得到黑色沉淀 |
| C.在5mL1.5×10-5 mol•L-1的NaCl溶液中,加入1滴(1mL约20滴)1.0×10-3mol•L-1的AgNO3溶液,不能观察到白色沉淀 |
| D.在烧杯中放入6.24 g 硫酸银固体,加200 g 水,经充分溶解后,所得饱和溶液的体积为200 mL,溶液中Ag + 的物质的量浓度为0.2 mol•L-1。 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】25 ℃时有关物质的颜色和溶度积(Ksp)如下表:
下列叙述中不正确的是( )
| 物质 | AgCl | AgBr | AgI | Ag2S |
| 颜色 | 白 | 淡黄 | 黄 | 黑 |
| Ksp | 1.8×10-10 | 7.7×10-13 | 1.5×10-16 | 1.8×10-50 |
| A.向AgCl的白色悬浊液中加入0.1 mol/L KI溶液,有黄色沉淀产生 |
| B.25 ℃时,利用表中的溶度积(Ksp),可以计算AgCl、AgBr、AgI、Ag2S饱和水溶液中Ag+的浓度 |
| C.25 ℃,AgCl固体分别在等物质的量浓度NaCl、CaCl2溶液中溶解达到平衡,两溶液中,c(Ag+)和溶度积均相同 |
| D.在5 mL 1.8×10-6 mol/L NaCl溶液中,加入1滴(20滴约为1 mL)1×10-3 mol/L AgNO3溶液,不能产生白色沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将盐酸滴入NaHCO3溶液中 | 有气泡产生 | 氯的非金属性比碳的强 |
| B | 用pH试纸分别测定0.1mol·L-1的Na2SO3溶液和0.1mol·L-1的NaHSO3溶液的pH | Na2SO3溶液的pH约为10 NaHSO3溶液的pH约为5 | HSO3-结合H+的能力比SO32-强 |
| C | 分别将乙烯与SO2通入酸性KMnO4溶液中 | KMnO4溶液均褪色 | 两种气体使酸性KMnO4溶液褪色的原理相同 |
| D | 向2ml0.1mol·L-1MgCl2溶液中加入5ml0.1mol·L-1NaOH溶液,出现白色沉淀后,继续滴入几滴FeCl3浓溶液,静置 | 出现红褐色沉淀 | 同温下,Ksp[Mg(OH)2] >Ksp[Fe(OH)3] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】已知: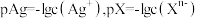 。
。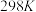 时,几种物质的
时,几种物质的 如表:
如表:
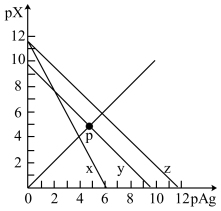
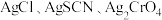 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
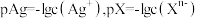 。
。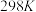 时,几种物质的
时,几种物质的 如表:
如表:| 化学式 |  |  |  |
| 颜色 | 白 | 浅黄 | 红 |
 |  | 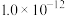 |  |
 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
A.图中x代表 曲线,z代表 曲线,z代表 曲线 曲线 |
B. 时,在 时,在 和 和 的物质的量浓度均为 的物质的量浓度均为 的溶液中,滴入少量 的溶液中,滴入少量 溶液,首先产生的是白色沉淀 溶液,首先产生的是白色沉淀 |
C. 时,若增大p点的阴离子浓度,则y上的点沿曲线向上移动 时,若增大p点的阴离子浓度,则y上的点沿曲线向上移动 |
D. 时, 时, 的平衡常数 的平衡常数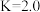 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】已知25°C时有关物质的颜色和溶度积(Ksp)如下表所示:
下列叙述中正确的是
| 物质 | AgCl | AgBr | AgI | Ag2S |
| 颜色 | 白 | 淡黄 | 黄 | 黑 |
| Ksp | 1.8×10-10 | 7.7×10-13 | 1.5×10-16 | 1.8×10-50 |
| A.向AgCl悬浊液中加入0.1mol·L-lNa2S溶液,有黑色沉淀产生 |
| B.25°C时,AgBr、AgI饱和水溶液中c(Ag+)的大小关系为后者大于前者 |
| C.25°C,AgCl固体在等物质的量浓度NaCl、CaCl2溶液中的溶度积不相同 |
| D.在5mL1.8×10-6mol·L-1NaCl溶液中,加入1滴(20滴约为1mL)1×10-3mol·L-1AgNO3溶液,能产生白色沉淀 |
您最近一年使用:0次
【推荐1】常温下,用AgNO3溶液分别滴定浓度均为0.0lmol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
| A.b表示AgCl的沉淀溶解平衡图像 |
| B.Ksp(Ag2C2O4)的数量级等于10-10 |
C.向c(Cl-)=c( )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 |
D.Ag2C2O4(s)+2Cl-(l) 2AgCl(s)+ 2AgCl(s)+ (aq)的平衡常数为109.04 (aq)的平衡常数为109.04 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
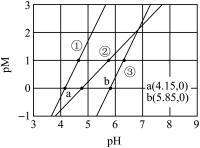
【推荐2】常温下,向含有CH3COOH、CuSO4、FeSO4的工业废水中逐滴加入NaOH溶液,pM随pH变化关系如图所示[pM表示 或
或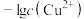 或
或 ],曲线①③斜率相同。已知:
],曲线①③斜率相同。已知: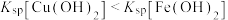 ;当离子浓度
;当离子浓度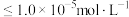 时,可认为该离子沉淀完全。下列说法不正确的是
时,可认为该离子沉淀完全。下列说法不正确的是
 或
或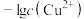 或
或 ],曲线①③斜率相同。已知:
],曲线①③斜率相同。已知: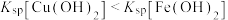 ;当离子浓度
;当离子浓度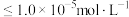 时,可认为该离子沉淀完全。下列说法不正确的是
时,可认为该离子沉淀完全。下列说法不正确的是
A.曲线①表示 与pH的关系 与pH的关系 |
B.pH=6时,溶液中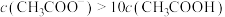 |
C.pH=7时,可认为 沉淀完全 沉淀完全 |
D.pH=8时 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=9.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A.H2CO3、HCO3-、CH3COO-、ClO-在溶液中可以大量共存 |
| B.等体积等浓度的CH3COONa和NaClO中离子总数:CH3COONa<NaClO |
| C.向浓度均为1.0×10-3 mol·L-1的KCl和K2CrO4混合溶液中滴加1.0×10-3 mol·L-1的AgNO3溶液,CrO42-先形成沉淀 |
| D.向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液中至c(CH3COOH):c(CH3COO-)=5∶9,此时溶液的pH=5 |
您最近一年使用:0次

 变化关系如图所示。
变化关系如图所示。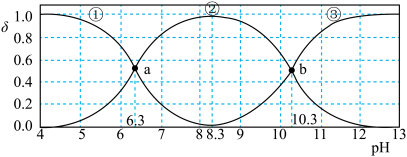
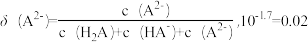 。
。