已知25°C时有关物质的颜色和溶度积(Ksp)如下表所示:
下列叙述中正确的是
| 物质 | AgCl | AgBr | AgI | Ag2S |
| 颜色 | 白 | 淡黄 | 黄 | 黑 |
| Ksp | 1.8×10-10 | 7.7×10-13 | 1.5×10-16 | 1.8×10-50 |
| A.向AgCl悬浊液中加入0.1mol·L-lNa2S溶液,有黑色沉淀产生 |
| B.25°C时,AgBr、AgI饱和水溶液中c(Ag+)的大小关系为后者大于前者 |
| C.25°C,AgCl固体在等物质的量浓度NaCl、CaCl2溶液中的溶度积不相同 |
| D.在5mL1.8×10-6mol·L-1NaCl溶液中,加入1滴(20滴约为1mL)1×10-3mol·L-1AgNO3溶液,能产生白色沉淀 |
更新时间:2022-01-13 17:21:29
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某温度下, 和
和 的饱和溶液中
的饱和溶液中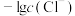 或
或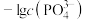 与
与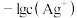 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是

 和
和 的饱和溶液中
的饱和溶液中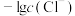 或
或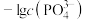 与
与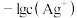 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.曲线Ⅰ表示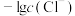 与 与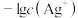 的关系 的关系 |
B.此温度下, |
C.a点混合体系中加入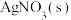 , ,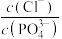 减小 减小 |
D.向 溶液中加入 溶液中加入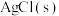 ,可生成 ,可生成 沉淀 沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】T℃下,三种硫酸盐MSO4,(M表示Pb2+或Ba2+或Sr2+)的沉淀溶解平衡曲线如图所示。已知pM=-lgc(M),p(SO42-)=-lgc(SO42-)。下列说法正确的是( )


| A.BaSO4在任何条件下都不可能转化成PbSO4 |
| B.X点和Z点分别是SrSO4和BaSO4的饱和溶液,对应的溶液中c(M)=c(SO42-) |
| C.在ToC时,用0.01mol.L-1Na2SO4溶液滴定20mL浓度均是0.01mol.L-1的Ba(NO3)2和Sr(NO3)2的混合溶液,Sr2+先沉淀 |
D.ToC下,反应PbSO4(s)+Ba2+(aq) BaSO4(s)+Pb2+(aq)的平衡常数为102.4 BaSO4(s)+Pb2+(aq)的平衡常数为102.4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
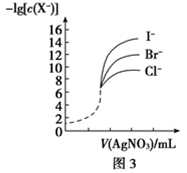
【推荐3】下列图示与对应的叙述相符的是( )
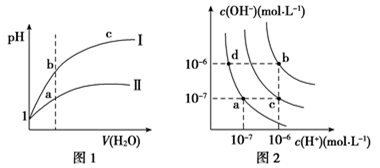


| A.图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图2中纯水仅升高温度,就可以从a点变到c点 |
| C.图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性 |
| D.用0.010 0 mol/L硝酸银标准溶液,滴定浓度均为0.100 0 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl- |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知Ksp(CaCO3)=3.36×10—9,Ksp(CaF2)=3.45×10—11。下列关于CaCO3和CaF2两悬浊液说法错误的是
| A.CaCO3悬浊液中c(Ca2+)较小 |
| B.分别滴加稀硫酸,溶度积常数均增大 |
| C.分别加入0.1mol/L的CaCl2溶液,c(CO32—)和 c(F—)均减小 |
| D.CaF2更容易转化成CaCO3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】298K时含大量 固体的溶液中离子浓度关系如图所示。
固体的溶液中离子浓度关系如图所示。

已知:298K时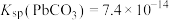 ,
, 固体溶解吸热。
固体溶解吸热。
下列说法正确的是
 固体的溶液中离子浓度关系如图所示。
固体的溶液中离子浓度关系如图所示。
已知:298K时
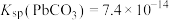 ,
, 固体溶解吸热。
固体溶解吸热。下列说法正确的是
| A.T小于298K,e点溶液中阴阳离子浓度相等 |
B.298K时碳酸铅的溶解度约为 g g |
| C.向d点浊液中滴加几滴蒸馏水,溶液由d点向f点迁移 |
D.298K时,向d点浊液加少量 ,溶液由d点向e点迁移 ,溶液由d点向e点迁移 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】某废水中含有 和
和 ,若始终保持
,若始终保持 饱和,且
饱和,且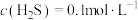 ,调节pH使
,调节pH使 和
和 形成硫化物而分离,体系中pH与
形成硫化物而分离,体系中pH与 关系如图所示(c为
关系如图所示(c为 、
、 、
、 、
、 的浓度)。下列说法正确的是
的浓度)。下列说法正确的是
 和
和 ,若始终保持
,若始终保持 饱和,且
饱和,且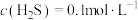 ,调节pH使
,调节pH使 和
和 形成硫化物而分离,体系中pH与
形成硫化物而分离,体系中pH与 关系如图所示(c为
关系如图所示(c为 、
、 、
、 、
、 的浓度)。下列说法正确的是
的浓度)。下列说法正确的是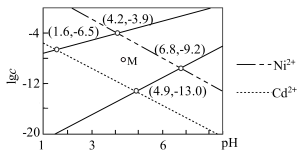
A. |
B.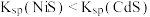 |
C.调节pH同时沉淀 和 和 时, 时,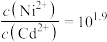 |
D.M点条件下能生成 沉淀,不能生成 沉淀,不能生成 沉淀 沉淀 |
您最近一年使用:0次
【推荐2】工业生产中利用方铅矿(主要成分为PbS,含有FeS2等杂质)制备PbSO4晶体的工艺流程如图:

已知:PbCl2难溶于冷水,易溶于热水;PbCl2(s)+2Cl-(aq)
 (aq) △H>0;Ksp(PbSO4)=1. 08×10-8,Ksp(PbCl2)=1.6×10-5。
(aq) △H>0;Ksp(PbSO4)=1. 08×10-8,Ksp(PbCl2)=1.6×10-5。
下列说法正确的是

已知:PbCl2难溶于冷水,易溶于热水;PbCl2(s)+2Cl-(aq)

 (aq) △H>0;Ksp(PbSO4)=1. 08×10-8,Ksp(PbCl2)=1.6×10-5。
(aq) △H>0;Ksp(PbSO4)=1. 08×10-8,Ksp(PbCl2)=1.6×10-5。下列说法正确的是
| A.“浸取”时发生的主要离子反应为MnO2+PbS+4H++4Cl-=PbCl2+S+MnCl2+2H2O |
B.“沉淀转化”过程中,当溶液中c(Cl-)=0.1 mol/L时,c( )=6.75×10-6 mol/L )=6.75×10-6 mol/L |
C.“沉降”时加入冰水使PbCl2(s)+2Cl-(aq)   (aq)平衡向右移 (aq)平衡向右移 |
| D.“滤渣2”的主要成分是Fe(OH)2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】某温度下,向10 mL 0.1 mol/LCuCl2溶液中滴加0.1 mol/L的Na2S溶液,滴加过程中溶液中−lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,已知:lg2=0.3,Ksp(ZnS)=3×10-25 。下列有关说法正确的是
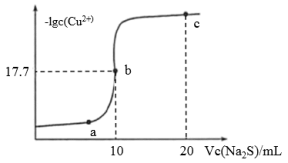

| A.a、b、c三点中,水的电离程度最大的为b点 |
| B.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
| C.该温度下Ksp(CuS)=4×10-36 |
| D.向100 mL Zn2+、Cu2+浓度均为10-5 mol/L的混合溶液中逐滴加入10-4 mol/L的Na2S溶液,Zn2+先沉淀 |
您最近一年使用:0次
【推荐1】已知:常温下, ,
,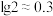 。常温下在含大量
。常温下在含大量 和
和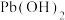 的浊液中滴加
的浊液中滴加 溶液,浊液中
溶液,浊液中 [
[ ,
, 、
、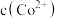 、
、 ]与
]与 关系如图,平衡常数K大于或等于
关系如图,平衡常数K大于或等于 时认为反应不可逆(即完全反应),下列叙述正确的是
时认为反应不可逆(即完全反应),下列叙述正确的是
 ,
,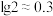 。常温下在含大量
。常温下在含大量 和
和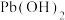 的浊液中滴加
的浊液中滴加 溶液,浊液中
溶液,浊液中 [
[ ,
, 、
、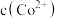 、
、 ]与
]与 关系如图,平衡常数K大于或等于
关系如图,平衡常数K大于或等于 时认为反应不可逆(即完全反应),下列叙述正确的是
时认为反应不可逆(即完全反应),下列叙述正确的是
A. 直线代表 直线代表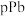 和 和 的关系 的关系 |
B.常温下,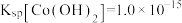 |
C.当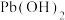 、 、 共存时, 共存时,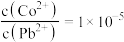 |
D. 、 、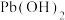 都能完全溶于亚硝酸溶液中 都能完全溶于亚硝酸溶液中 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】向AgCl饱和溶液(有足量AgCl固体)中滴加氨水,发生反应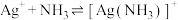 和
和 ,
, 与
与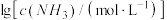 的关系如图所示{其中M代表
的关系如图所示{其中M代表 、
、 、
、 或
或 }。
}。
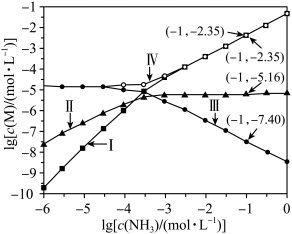
下列说法正确的是
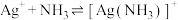 和
和 ,
, 与
与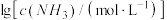 的关系如图所示{其中M代表
的关系如图所示{其中M代表 、
、 、
、 或
或 }。
}。
下列说法正确的是
A.曲线Ⅲ表示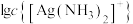 随 随 的变化曲线 的变化曲线 |
B.随 增大, 增大, 先增大后减小 先增大后减小 |
C.反应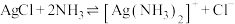 的平衡常数为 的平衡常数为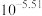 |
D. 时,溶液中 时,溶液中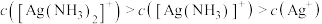 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知锌及其化合物的性质与铝及其化合物相似。如图横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4 ]2-的物质的量浓度的对数。25℃时,下列说法中不正确的是
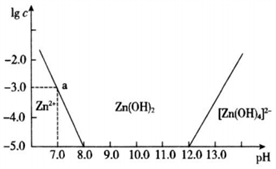

| A.往ZnCl2溶液中加入过量氢氧化钠溶液,反应的离子方程式为Zn2++4OH-=[Zn(OH)4]2- |
| B.若要从某废液中完全沉淀Zn2+,通常可以调控该溶液的pH在8.0—12.0之间 |
| C.pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108 |
| D.该温度时,Zn(OH)2的溶度积常数(Ksp)为1×l0-10 |
您最近一年使用:0次

 溶液中再加入少量的
溶液中再加入少量的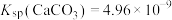
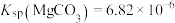
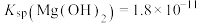

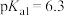 ,
,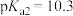 ;
; 沉淀范围:pH9.4~12.4。
沉淀范围:pH9.4~12.4。 ,饱和
,饱和
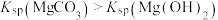 ,
, 溶液,有
溶液,有 溶液,可生成沉淀。
溶液,可生成沉淀。

