已知: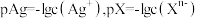 。
。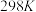 时,几种物质的
时,几种物质的 如表:
如表:
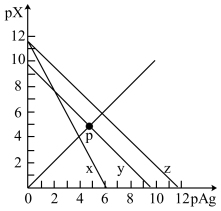
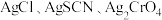 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
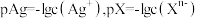 。
。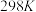 时,几种物质的
时,几种物质的 如表:
如表:| 化学式 |  |  |  |
| 颜色 | 白 | 浅黄 | 红 |
 |  | 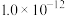 |  |
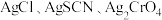 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
A.图中x代表 曲线,z代表 曲线,z代表 曲线 曲线 |
B. 时,在 时,在 和 和 的物质的量浓度均为 的物质的量浓度均为 的溶液中,滴入少量 的溶液中,滴入少量 溶液,首先产生的是白色沉淀 溶液,首先产生的是白色沉淀 |
C. 时,若增大p点的阴离子浓度,则y上的点沿曲线向上移动 时,若增大p点的阴离子浓度,则y上的点沿曲线向上移动 |
D. 时, 时, 的平衡常数 的平衡常数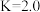 |
更新时间:2022-05-29 09:21:36
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是( )
| A.常温下,向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大 |
| B.0.1 mol·L-1的醋酸加水稀释,c(CH3COOH)/c(CH3COO-)减小,但K不变。 |
| C.足量体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 |
| D.25℃,在AgCl悬浊液中加入少量NaCl固体,c(Ag+)减小,Ksp(AgCl)减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。25℃时,平衡体系中含Ag微粒的分布系数δ[如δ(AgCl )=
)=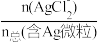 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是

 )=
)=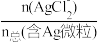 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
| A.25℃时,AgCl的溶解度随c(Cl-)增大而不断减小 |
| B.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol·L-1 |
C.当c(Cl-)=10-2.54mol·L-1时,溶液中c(Ag+)>c(AgCl )>c(Cl )>c(Cl ) ) |
D.25℃时,AgCl +Cl- +Cl- AgCl AgCl 的平衡常数K=100.2 的平衡常数K=100.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】已知 是难溶于水、可溶于酸的盐。常温下,用盐酸调节
是难溶于水、可溶于酸的盐。常温下,用盐酸调节 浊液的
浊液的 ,测得在不同
,测得在不同 条件下,体系中
条件下,体系中 与
与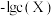 (X为
(X为 、
、 )的变化关系如图所示。下列说法错误的是
)的变化关系如图所示。下列说法错误的是
 是难溶于水、可溶于酸的盐。常温下,用盐酸调节
是难溶于水、可溶于酸的盐。常温下,用盐酸调节 浊液的
浊液的 ,测得在不同
,测得在不同 条件下,体系中
条件下,体系中 与
与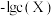 (X为
(X为 、
、 )的变化关系如图所示。下列说法错误的是
)的变化关系如图所示。下列说法错误的是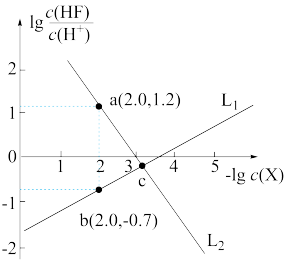
A. 表示 表示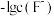 与 与 的变化曲线 的变化曲线 |
B.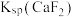 的数量级为 的数量级为 |
C.c点溶液中: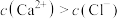 |
D.a、b、c三点的溶液中: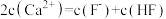 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】相关物质的溶度积常数见下表(25℃):
下列有关说法中不正确的是
物质 | Mg(OH)2 | CH3COOAg | AgCl | Ag2CrO4 |
Ksp(单位略) | 1.1×10—11 | 2.3×10﹣3 | 1.8×10﹣10 | 1.9×10﹣12 |
| A.浓度均为0.2 mol•L﹣1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 |
| B.将0.001 mol•L﹣1的AgNO3溶液滴入0.001 mol•L﹣1的KCl和0.001 mol•L﹣1 的K2CrO4混合溶液中.先产生Ag2CrO4沉淀 |
| C.0.11 mol•L﹣1的MgCl2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9 |
| D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】根据Al(OH)3的Ksp = 1.3×10-33、 Mg(OH) 2的Ksp =5.6×10-12 ,等物质的量浓度AlCl3、MgCl2
混合溶液与NaOH溶液反应生成相应沉淀,pH与沉淀量关系如下图:

下列有关说法正确的是
混合溶液与NaOH溶液反应生成相应沉淀,pH与沉淀量关系如下图:

下列有关说法正确的是
| A.Al(OH) 3和Mg(OH)2在水溶液中的电离过程完全相同 |
| B.若改变溶液的pH,在pH<4.7时,n(Mg2+)几乎不变化 |
| C.当pH>11.1时,溶液中只有NaCl和NaAlO2(Na[Al(OH)4]) |
| D.物质的量浓度Al3+、Mg2+混合溶液与氨水反应生成相应沉淀,氨水的pH与沉淀量关系与上图相似 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向10mL浓度均为0.1mol·L-1的FeSO4和ZnSO4的混合溶液中加入0.1mol·L-1氨水,溶液中金属元素有不同的存在形式,它们的物质的量浓度与氨水(Kb=1.8×10-5)体积关系如下图所示。测得M、N点溶液pH分别为8.04、8.95。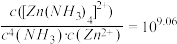
ii.Ksp[Zn(OH)2]<Ksp[Fe(OH)2]
下列说法正确的是
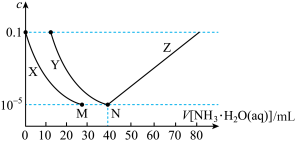
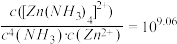
ii.Ksp[Zn(OH)2]<Ksp[Fe(OH)2]
下列说法正确的是
| A.曲线Y表示Zn2+ |
| B.Ksp[Fe(OH)2]=10-16.92 |
| C.N点以后,锌元素主要以Zn2+形式存在 |
| D.Zn(OH)2+4NH3⇌[Zn(NH3)4]2++2OH- K=10-7.86 |
您最近一年使用:0次
【推荐3】室温下,两种难溶盐AgCl(白色)、Ag2CrO4(砖红色)的离子浓度关系曲线如图所示,其中p(Cl-)=-lgc(Cl-)、p(CrO )=-lgc(CrO
)=-lgc(CrO )、p(Ag+)=-lgc(Ag+),lg2=0.3。下列说法正确的是
)、p(Ag+)=-lgc(Ag+),lg2=0.3。下列说法正确的是

 )=-lgc(CrO
)=-lgc(CrO )、p(Ag+)=-lgc(Ag+),lg2=0.3。下列说法正确的是
)、p(Ag+)=-lgc(Ag+),lg2=0.3。下列说法正确的是
| A.Ksp(Ag2CrO4)=4×10-10 |
B.向A点的混合溶液中,加入硝酸银固体,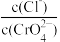 变小 变小 |
| C.向等浓度的NaCl和Na2CrO4混合溶液中滴加AgNO3溶液,先产生白色沉淀 |
| D.B点条件下既能生成白色沉淀,也能生成砖红色沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】室温下,分别调节 溶液、HF溶液、HA溶液[已知
溶液、HF溶液、HA溶液[已知 (HF)>
(HF)> (HA)]的pH,测得溶液中pX[
(HA)]的pH,测得溶液中pX[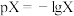 ;X代表
;X代表 、
、 、
、 随溶液pH的变化如图所示[已知
随溶液pH的变化如图所示[已知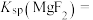
 ]。下列说法错误的是
]。下列说法错误的是
 溶液、HF溶液、HA溶液[已知
溶液、HF溶液、HA溶液[已知 (HF)>
(HF)> (HA)]的pH,测得溶液中pX[
(HA)]的pH,测得溶液中pX[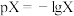 ;X代表
;X代表 、
、 、
、 随溶液pH的变化如图所示[已知
随溶液pH的变化如图所示[已知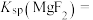
 ]。下列说法错误的是
]。下列说法错误的是
A. 代表溶液中 代表溶液中 随溶液pH的变化 随溶液pH的变化 | B.NaF、NaA的混合溶液中: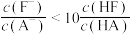 |
C. 转化为 转化为 较容易实现 较容易实现 | D. 和 和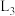 的交点A对应的pH约为6.7 的交点A对应的pH约为6.7 |
您最近一年使用:0次
单选题
|
较难
(0.4)
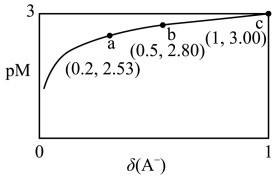
【推荐2】HA是一元弱酸,微溶盐 的饱和溶液中
的饱和溶液中 随
随 而变化,
而变化, 不发生水解。25℃时,实验测得pM与
不发生水解。25℃时,实验测得pM与 的关系如图所示,其中a点对应的pH=5.0.[已知:
的关系如图所示,其中a点对应的pH=5.0.[已知: ,
,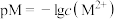 ,
,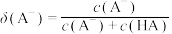 ]。下列说法正确的是
]。下列说法正确的是
 的饱和溶液中
的饱和溶液中 随
随 而变化,
而变化, 不发生水解。25℃时,实验测得pM与
不发生水解。25℃时,实验测得pM与 的关系如图所示,其中a点对应的pH=5.0.[已知:
的关系如图所示,其中a点对应的pH=5.0.[已知: ,
,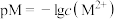 ,
,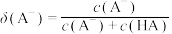 ]。下列说法正确的是
]。下列说法正确的是
A.25℃时,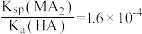 |
B.25℃时,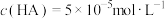 |
C.25℃时,b点溶液中, |
| D.a、b、c三点溶液中水的电离程度:a>b>c |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】工业上常用 作沉淀剂除去废水中的
作沉淀剂除去废水中的 和
和 。通过调节溶液的pH可使
。通过调节溶液的pH可使 和
和 逐一沉降,处理过程中始终保持
逐一沉降,处理过程中始终保持 溶液为饱和状态即
溶液为饱和状态即 mol/L,体系中
mol/L,体系中 、
、 、
、 ,
, 浓度(mol/L)的负对数pM与pH的关系如图所示。已知:
浓度(mol/L)的负对数pM与pH的关系如图所示。已知: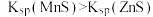 。下列说法不正确的是
。下列说法不正确的是
 作沉淀剂除去废水中的
作沉淀剂除去废水中的 和
和 。通过调节溶液的pH可使
。通过调节溶液的pH可使 和
和 逐一沉降,处理过程中始终保持
逐一沉降,处理过程中始终保持 溶液为饱和状态即
溶液为饱和状态即 mol/L,体系中
mol/L,体系中 、
、 、
、 ,
, 浓度(mol/L)的负对数pM与pH的关系如图所示。已知:
浓度(mol/L)的负对数pM与pH的关系如图所示。已知: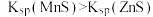 。下列说法不正确的是
。下列说法不正确的是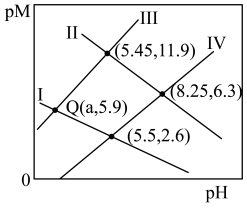
A.Ⅱ表示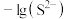 与pH的关系曲线 与pH的关系曲线 |
B.Q点对应 的数量级为 的数量级为 |
C.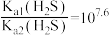 |
D.溶液中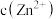 和 和 均为0.1mol/L, 均为0.1mol/L, 完全沉淀时溶液的最小pH为2 完全沉淀时溶液的最小pH为2 |
您最近一年使用:0次


 溶液由
溶液由 ,测溶液pH
,测溶液pH 的水解程度增大
的水解程度增大 溶液2滴,试管2中加入
溶液2滴,试管2中加入
 时,双氧水分解反应的活化能较小
时,双氧水分解反应的活化能较小 的悬浊液中滴加
的悬浊液中滴加 溶液
溶液
 和NaClO溶液的pH
和NaClO溶液的pH 水解程度大于
水解程度大于


