名校
1 . 微生物脱盐池的a极上加入了呼吸细菌,工作时可将工业废水中的有机污染物转化为 ,其工作原理如图所示。下列说法正确的是
,其工作原理如图所示。下列说法正确的是
 ,其工作原理如图所示。下列说法正确的是
,其工作原理如图所示。下列说法正确的是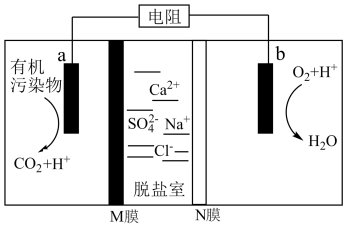
A.工作时, 极发生还原反应,电子从 极发生还原反应,电子从 极流向 极流向 极 极 |
B. 膜为阴离子交换膜,脱盐室最终可得到淡盐水 膜为阴离子交换膜,脱盐室最终可得到淡盐水 |
C. 极上消耗 极上消耗 气体,则通过 气体,则通过 膜的离子的物质的量为 膜的离子的物质的量为 |
D.若有机物的分子式为 ,则 ,则 极的电极反应式为 极的电极反应式为 |
您最近一年使用:0次
2024-05-06更新
|
386次组卷
|
2卷引用:2024届陕西省西安市浐灞第二中学高三上学期一模理综试卷-高中化学
2 . 化合物 (
(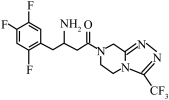 )是磷酸西他列汀的重要中间体,可以2,4,5—三氟苯乙酸为原料通过下列路线进行合成:
)是磷酸西他列汀的重要中间体,可以2,4,5—三氟苯乙酸为原料通过下列路线进行合成:

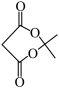
已知:①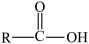 +
+

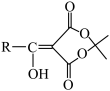
②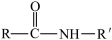
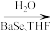
 +R′-NH2
+R′-NH2
(1)C分子中含氧官能团的名称为
(2)C→D的反应类型为
(3)
 是A的同分异构体,其化学名称为
是A的同分异构体,其化学名称为(4)化合物F的结构简式为
(5)已知:
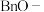 为苄氧基,结构为
为苄氧基,结构为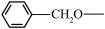 ,则G→H的化学方程式为
,则G→H的化学方程式为(6)M是A的同分异构体,满足下列条件的M共有
a.可与
 溶液发生显色反应 b.含有三氟甲基(
溶液发生显色反应 b.含有三氟甲基( )
)其中核磁共振氢谱有三组峰,且峰面积比为2:2:1的同分异构体的结构简式为
(7)已知:
 、
、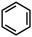
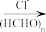
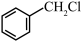 。结合所学知识,设计以
。结合所学知识,设计以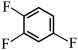 为原料制备
为原料制备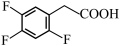 的合成路线:
的合成路线:
您最近一年使用:0次
解题方法
3 . 植物骆驼蹄瓣中有多种有机活性药用成分,如奎洛维酸,其结构如图所示,下列有关该物质的说法错误的是
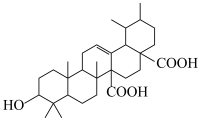
| A.能使溴水或酸性高锰酸钾溶液褪色 |
| B.所有碳原子不可能位于同一平面上 |
| C.含有两种官能团 |
| D.能发生取代反应和氧化反应 |
您最近一年使用:0次
4 . 某课题组发展了可控的 键形成策略,实现了
键形成策略,实现了 硅杂哌啶的高效合成,其反应原理如下:
硅杂哌啶的高效合成,其反应原理如下:
(1)下面B原子的电子排布图中,属于基态电子排布图的为___________ (填标号,下同),激发态电子排布图中能量最高的是___________ 。___________ (用元素符号表示)。晶体硅的熔点低于晶体硼,试解释其原因:___________ 。
(3)已知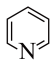 为平面结构,则合成的4-硅杂哌啶分子中,有
为平面结构,则合成的4-硅杂哌啶分子中,有 和
和 两种杂化方式的元素为
两种杂化方式的元素为___________ (填元素符号)。
(4)氮和硼可形成新型半导体材料 ,其晶胞结构如图所示,晶胞中每个
,其晶胞结构如图所示,晶胞中每个 周围最近的
周围最近的 原子个数为
原子个数为___________ 。若晶胞边长为 ,用
,用 表示阿伏加德罗常数的值,则最近的硼原子间的距离为
表示阿伏加德罗常数的值,则最近的硼原子间的距离为___________  (用含
(用含 的代数式表示),晶体密度为
的代数式表示),晶体密度为___________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
 键形成策略,实现了
键形成策略,实现了 硅杂哌啶的高效合成,其反应原理如下:
硅杂哌啶的高效合成,其反应原理如下: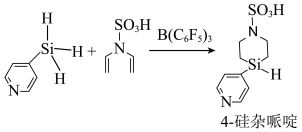
(1)下面B原子的电子排布图中,属于基态电子排布图的为
a.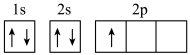 b.
b.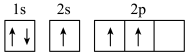
c. d.
d.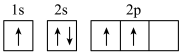
(3)已知
 为平面结构,则合成的4-硅杂哌啶分子中,有
为平面结构,则合成的4-硅杂哌啶分子中,有 和
和 两种杂化方式的元素为
两种杂化方式的元素为(4)氮和硼可形成新型半导体材料
 ,其晶胞结构如图所示,晶胞中每个
,其晶胞结构如图所示,晶胞中每个 周围最近的
周围最近的 原子个数为
原子个数为 ,用
,用 表示阿伏加德罗常数的值,则最近的硼原子间的距离为
表示阿伏加德罗常数的值,则最近的硼原子间的距离为 (用含
(用含 的代数式表示),晶体密度为
的代数式表示),晶体密度为 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
5 . 利用含钴废料(主要成分为 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: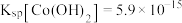 ;
;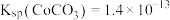 。
。
请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为 和
和___________ 。“酸浸”时 发生反应的总离子方程式为
发生反应的总离子方程式为___________ 。
(2)“萃取”时 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)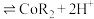 ,若萃取剂的量一定时,
,若萃取剂的量一定时,___________ (填“一次萃取”或“少量多次萃取”)的萃取效率更高。若“酸浸”后浸出液的 ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为___________ (结果保留一位小数,溶液体积变化忽略不计)。
(3)“沉锰”时, 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为___________ 。
(4)可以通过电解 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是___________ 。若Ⅱ室溶液中溶质的质量增加了 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为___________ 。
 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: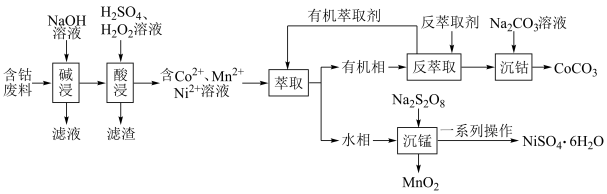
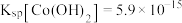 ;
;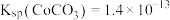 。
。请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为
 和
和 发生反应的总离子方程式为
发生反应的总离子方程式为(2)“萃取”时
 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)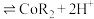 ,若萃取剂的量一定时,
,若萃取剂的量一定时, ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为(3)“沉锰”时,
 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为(4)可以通过电解
 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为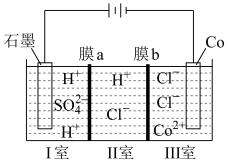
您最近一年使用:0次
解题方法
6 . 化学反应在生产生活中应用广泛。下列离子方程式书写正确且能解释相应应用的是
| 选项 | 应用 | 离子方程式 |
| A | 使用碳酸钠溶液浸泡锅炉水垢 | 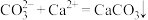 |
| B | 使用 溶液腐蚀铜制电路板 溶液腐蚀铜制电路板 |  |
| C | 海水提溴时,吸收塔利用 溶液吸收从吹出塔出来的溴蒸气 溶液吸收从吹出塔出来的溴蒸气 | 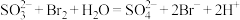 |
| D | 使用盐酸清洗铜器表面的铜绿 | 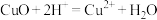 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 .  具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、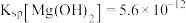 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:___________ ;加入 的目的是
的目的是___________ 。
(2)滤渣1的主要成分为___________ 、___________ 及不溶于酸、碱的杂质;加入 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
___________ 。
(3)若通入过量 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为___________ 。
(4)写出洗去固体A表面杂质的简要操作:___________ 。
(5)“煅烧”固体A反应的化学方程式为___________ 。
 具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、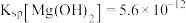 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:
 的目的是
的目的是(2)滤渣1的主要成分为
 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
(3)若通入过量
 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为(4)写出洗去固体A表面杂质的简要操作:
(5)“煅烧”固体A反应的化学方程式为
您最近一年使用:0次
2024-04-25更新
|
195次组卷
|
3卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
8 . 镓 、铟
、铟 都是典型的稀有分散元素。回答下列问题:
都是典型的稀有分散元素。回答下列问题:
(1)基态 原子的核外价电子排布式为
原子的核外价电子排布式为_____ ,最高能级电子的电子云形状为_____ 。
(2)一种含镓药物的合成方法如图所示: 原子的杂化方式为
原子的杂化方式为_____ , 化合物
化合物 中含有的
中含有的 键的物质的量为
键的物质的量为_____ 。化合物Ⅰ中所含元素的电负性由大到小的顺序为_____ (用元素符号表示)。
②化合物Ⅱ中 的配位数为
的配位数为_____ ,
_____ 。
(3)一种由 组成的晶体属四方晶系,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞棱边夹角均为 ,其晶胞结构如图。
,其晶胞结构如图。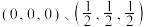 。则C点原子的分数坐标为
。则C点原子的分数坐标为_____ 。
② 表示阿伏加德罗常数的值,该晶体的密度为
表示阿伏加德罗常数的值,该晶体的密度为_____ (用含 的代数式表示)
的代数式表示) 。
。
 、铟
、铟 都是典型的稀有分散元素。回答下列问题:
都是典型的稀有分散元素。回答下列问题:(1)基态
 原子的核外价电子排布式为
原子的核外价电子排布式为(2)一种含镓药物的合成方法如图所示:

 原子的杂化方式为
原子的杂化方式为 化合物
化合物 中含有的
中含有的 键的物质的量为
键的物质的量为②化合物Ⅱ中
 的配位数为
的配位数为
(3)一种由
 组成的晶体属四方晶系,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞棱边夹角均为 ,其晶胞结构如图。
,其晶胞结构如图。
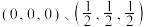 。则C点原子的分数坐标为
。则C点原子的分数坐标为②
 表示阿伏加德罗常数的值,该晶体的密度为
表示阿伏加德罗常数的值,该晶体的密度为 的代数式表示)
的代数式表示) 。
。
您最近一年使用:0次
解题方法
9 . 常温下,将 溶液滴加到乙二酸
溶液滴加到乙二酸 溶液中,混合溶液的
溶液中,混合溶液的 与
与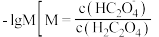 或
或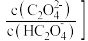 的关系如图所示。忽略滴定过程中温度的变化,下列叙述错误的是
的关系如图所示。忽略滴定过程中温度的变化,下列叙述错误的是
 溶液滴加到乙二酸
溶液滴加到乙二酸 溶液中,混合溶液的
溶液中,混合溶液的 与
与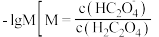 或
或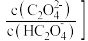 的关系如图所示。忽略滴定过程中温度的变化,下列叙述错误的是
的关系如图所示。忽略滴定过程中温度的变化,下列叙述错误的是
A.曲线Ⅱ表示 与 与 的变化关系 的变化关系 |
B.乙二酸的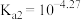 |
C. 溶液是碱性 溶液是碱性 |
D. 时, 时,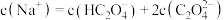 |
您最近一年使用:0次
2024-04-17更新
|
647次组卷
|
4卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学2024届陕西省商洛市高三上学期第二次模拟考试理综试题-高中化学(已下线)通关练10 盘点溶液中的“四大”平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)
10 . 常温下,往 溶液中滴入
溶液中滴入 溶液,溶液中由水电离出的
溶液,溶液中由水电离出的 的负对数
的负对数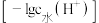 与所加
与所加 溶液体积的关系如图所示,下列说法错误的是
溶液体积的关系如图所示,下列说法错误的是 。
。
 溶液中滴入
溶液中滴入 溶液,溶液中由水电离出的
溶液,溶液中由水电离出的 的负对数
的负对数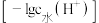 与所加
与所加 溶液体积的关系如图所示,下列说法错误的是
溶液体积的关系如图所示,下列说法错误的是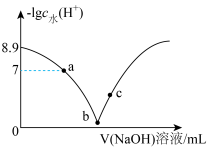
 。
。A.a点溶液中, |
B.b点溶液中, |
C.c点溶液中,由水电离出的 和由水电离出的 和由水电离出的 的乘积为 的乘积为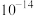 |
D.往碳酸钠溶液中加入足量的 溶液,一定无气泡产生 溶液,一定无气泡产生 |
您最近一年使用:0次



