名校
1 . 下列反应中,原子利用率为100%的是
A.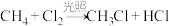 |
B.2CH2=CH2+O2 2 2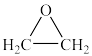 |
C. |
D.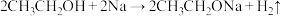 |
您最近一年使用:0次
2024-05-22更新
|
441次组卷
|
2卷引用:2023-2024学年广东省汕头市汕头金南实验学校三模化学试题
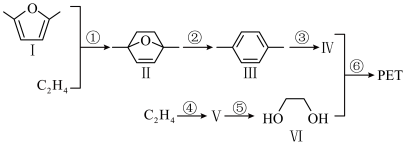
2 . PET是一种用途广泛的高分子材料,其合成的方法如图所示(反应所需的部分试剂与条件省略)。___________ 。化合物Ⅲ与酸性KMnO4溶液反应可得到化合物Ⅳ,则化合物Ⅳ的名称为___________ 。
(2)化合物Ⅴ是环状分子,与H2O加成可得到化合物Ⅵ,则化合物Ⅴ的结构简式为___________ 。
(3)化合物Ⅶ是化合物Ⅱ与足量H2加成后所得产物的一种同分异构体,其核磁共振氢谱中峰面积比为3:1:3,请写出一种符合条件的化合物Ⅶ的结构简式:___________ 。
(4)根据化合物Ⅲ的结构特征,分析预测其可能具有的化学性质,并完成下表:
(5)下列关于反应①②的说法中正确的有___________(填标号)。
(6)请以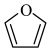 与丙烯为含碳原料,利用所学知识与上述合成路线的信息,合成化合物
与丙烯为含碳原料,利用所学知识与上述合成路线的信息,合成化合物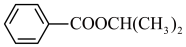 ,并基于你的合成路线,回答下列问题:
,并基于你的合成路线,回答下列问题:___________ (注明反应条件)。
(2)化合物Ⅴ是环状分子,与H2O加成可得到化合物Ⅵ,则化合物Ⅴ的结构简式为
(3)化合物Ⅶ是化合物Ⅱ与足量H2加成后所得产物的一种同分异构体,其核磁共振氢谱中峰面积比为3:1:3,请写出一种符合条件的化合物Ⅶ的结构简式:
(4)根据化合物Ⅲ的结构特征,分析预测其可能具有的化学性质,并完成下表:
| 序号 | 反应试剂、条件 | 反应生成的新结构 | 反应类型 |
| 1 |
| ||
| 2 | 取代反应 |
(5)下列关于反应①②的说法中正确的有___________(填标号)。
| A.反应①为加成反应 |
| B.化合物Ⅲ中所有原子共平面 |
| C.反应②过程中,有C-O键和C-H键的断裂 |
| D.化合物Ⅱ中,氧原子采取sp3杂化,且不含手性碳原子 |
(6)请以
 与丙烯为含碳原料,利用所学知识与上述合成路线的信息,合成化合物
与丙烯为含碳原料,利用所学知识与上述合成路线的信息,合成化合物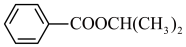 ,并基于你的合成路线,回答下列问题:
,并基于你的合成路线,回答下列问题:(a)从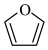 出发,第一步反应的产物为
出发,第一步反应的产物为
您最近一年使用:0次
3 . SO2-空气电池是一种新型环保电池,可在发电的同时制得硫酸,电池内部以稀硫酸为电解液。电池工作时,下列说法正确的是
| A.SO2发生还原反应 |
| B.H2SO4在电池的负极生成 |
| C.电子从负极通过电解液移向正极 |
| D.通入空气发生的电极反应为O2+4e-+2H2O=4OH- |
您最近一年使用:0次
4 . 实验探究是化学学习的方法之一、下列实验设计、现象和实验结论均正确的是
| 选项 | 实验设计 | 现象 | 实验结论 |
| A | 向鸡蛋清溶液中滴入几滴硫酸铜溶液 | 产生白色沉淀,加水后沉淀不溶解 | 蛋白质发生了变性 |
| B | 室温下用pH计测定同浓度的NaClO溶液和CH3COONa溶液的pH | NaClO溶液的pH较大 | 酸性: HClO>CH3COOH |
| C | 向溶液中先滴加新制氯水,再加KSCN溶液 | 溶液变红 | 该溶液一定含有Fe2+ |
| D | 取少量 | 紫红色褪去 | 该有机物中含有醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列事实中,不能用化学平衡移动原理解释的是
A.棕色的 体系加压后,颜色先变深后逐渐变浅 体系加压后,颜色先变深后逐渐变浅 |
| B.在配制硫酸亚铁溶液时往往要加入少量铁粉 |
| C.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
您最近一年使用:0次
解题方法
6 . 二氧化硫是重要的化工原料。某实验小组欲制备SO2并探究其相关反应。
Ⅰ.SO2的制备
(1)实验小组以亚硫酸钠(Na2SO3)粉末和70%的硫酸为原料制取SO2,并要求能够控制反应速率,下列可选用的仪器是___________ (填标号)。
实验事实:小组同学向1mL0.5mol/LFeCl3溶液中通入SO2至饱和,溶液先变成红色,静置5min后溶液红色变浅,慢慢变为黄色,静置9h后溶液变为绿色。
提出问题:溶液变为红色与什么微粒有关?
查阅资料:①Fe3+易与阴离子形成配合物,且Fe(Ⅲ)配合物常呈现特殊颜色。
②SO2溶液中,存在的含有硫元素的微粒有SO2、H2SO3、 和
和 。
。
提出猜想:a.溶液变为红色与 有关;
有关;
b.溶液变为红色与 有关。
有关。
实验验证:为验证猜想,小组同学做了如下实验。
(2)完成表格:实验②中加入___________ 溶液。
上述两个实验中溶液都变为红色,因此无法得出实验结论。
进一步验证:为进一步验证猜想,小组同学配制系列溶液并测量其吸光度,绘制出右图曲线。
参比溶液:0.5mL1mol/LFeCl3溶液+0.5mL1mol/LNa2SO3溶液+7mL蒸馏水
图中A、B、C三点对应加入各试剂的体积如表所示。
说明:①已知吸光度大小与溶液中红色物质浓度成正比。②参比溶液的作用是空白对照,设定参比溶液的吸光度为0。
(3)补充上表中数值,其中a=___________ ,b=___________ 。
实验结论
(4)根据以上实验,可以推测:溶液变为红色与___________ (填离子符号)有关。
拓展探究
将静置9h后变为绿色的溶液分为两份,向其中一份溶液中滴加铁氰化钾溶液,有蓝色沉淀生成;向另一份溶液中滴加盐酸酸化的氯化钡溶液,有白色沉淀生成。
(5)①写出溶液变为绿色所发生氧化还原反应的离子方程式:___________ 。
②试从平衡移动的角度,分析溶液红色变浅直至消失的原因:___________ 。
(6)写出二氧化硫在生产生活中的一种应用:___________ 。
Ⅰ.SO2的制备
(1)实验小组以亚硫酸钠(Na2SO3)粉末和70%的硫酸为原料制取SO2,并要求能够控制反应速率,下列可选用的仪器是
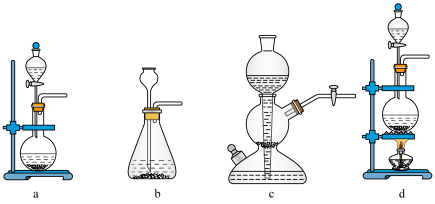
实验事实:小组同学向1mL0.5mol/LFeCl3溶液中通入SO2至饱和,溶液先变成红色,静置5min后溶液红色变浅,慢慢变为黄色,静置9h后溶液变为绿色。
提出问题:溶液变为红色与什么微粒有关?
查阅资料:①Fe3+易与阴离子形成配合物,且Fe(Ⅲ)配合物常呈现特殊颜色。
②SO2溶液中,存在的含有硫元素的微粒有SO2、H2SO3、
 和
和 。
。提出猜想:a.溶液变为红色与
 有关;
有关;b.溶液变为红色与
 有关。
有关。实验验证:为验证猜想,小组同学做了如下实验。
| 实验 | 实验操作 | 实验现象 |
| ① | 取1mL1mol/LFeCl3溶液于试管中,加入3mL1mol/LNa2SO3溶液,观察5min内的颜色变化 | 溶液变为红色 |
| ② | 取1mL1mol/LFeCl3溶液于试管中,加入___________溶液,观察5min内的颜色变化 | 溶液变为红色 |
(2)完成表格:实验②中加入
上述两个实验中溶液都变为红色,因此无法得出实验结论。
进一步验证:为进一步验证猜想,小组同学配制系列溶液并测量其吸光度,绘制出右图曲线。
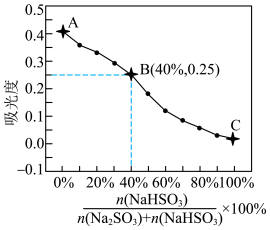
参比溶液:0.5mL1mol/LFeCl3溶液+0.5mL1mol/LNa2SO3溶液+7mL蒸馏水
图中A、B、C三点对应加入各试剂的体积如表所示。
| 点 | 1mol/LFeCl3/mL | 1mol/LNa2SO3/mL | 1mol/LNaHSO3/mL |
| A | 0.5 | 4.0 | 0.0 |
| B | a | b | |
| C | 0.0 | 4.0 |
(3)补充上表中数值,其中a=
实验结论
(4)根据以上实验,可以推测:溶液变为红色与
拓展探究
将静置9h后变为绿色的溶液分为两份,向其中一份溶液中滴加铁氰化钾溶液,有蓝色沉淀生成;向另一份溶液中滴加盐酸酸化的氯化钡溶液,有白色沉淀生成。
(5)①写出溶液变为绿色所发生氧化还原反应的离子方程式:
②试从平衡移动的角度,分析溶液红色变浅直至消失的原因:
(6)写出二氧化硫在生产生活中的一种应用:
您最近一年使用:0次
解题方法
7 . 化学与生产生活息息相关,下列生产生活实例与所述化学知识没有关联的是
| 选项 | 生产生活实例 | 化学知识 |
| A | 补铁剂与维生素C同时服用效果更佳 | 维生素C具有还原性 |
| B | 用小苏打作发泡剂烘焙面包 | NaHCO3可与酸反应产生气体 |
| C | 用Na2S标准液检测污水中Cu2+含量 | CuS属于难溶电解质 |
| D | 用聚乙烯塑料制作食品保鲜膜 | 聚乙烯燃烧能生成CO2和H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 下列有关化学用语表述正确的是
A.过氧化氢的电子式: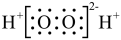 |
| B.HClO的结构式: H-Cl-O |
C.用电子式表示CO2的形成过程为 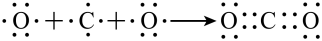 |
D.用电子式表示 的形成过程为 的形成过程为 |
您最近一年使用:0次
2024-04-24更新
|
284次组卷
|
2卷引用:2023-2024学年广东省汕头市汕头金南实验学校三模化学试题
9 . 下列陈述I和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | HCl的酸性强于CH3COOH | 盐酸的pH一定小于醋酸溶液 |
| B | 通过煤的干馏可获得苯、甲苯等化工原料 | 煤的干馏属于化学变化 |
| C | 将Cl2通入溴水中,溴水褪色 | Cl2具有漂白性 |
| D | 将金属Na加入CuSO4溶液中,析出红色固体 | 还原性:Na>Cu |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-23更新
|
854次组卷
|
2卷引用:2024届广东省肇庆市高三上学期二模化学试题
解题方法
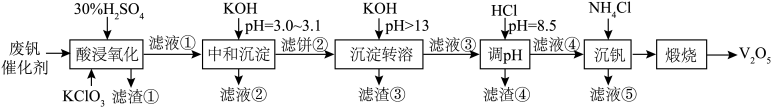
10 . 为回收利用废钒催化剂(含有V2O5、VOSO4、SiO2、Fe3O4以及钾和铝的硅酸盐),科研人员研制了一种回收V2O5的新工艺,主要流程如下图。
ii.VOSO4可溶、(VO2)2SO4易溶、V2O5和NH4VO3难溶; +2OH-=
+2OH-= +H2O
+H2O
(1)“酸浸氧化”时,VO2+转化成 反应的离子方程式为
反应的离子方程式为______ ,同时V2O5转化为 。滤渣①主要成分是
。滤渣①主要成分是______ 。
(2)“中和沉淀”中,钒水解并沉淀为V2O5·2H2O,随滤液②可除去金属离子K+以及部分的金属离子有______ 。
(3)“沉淀转溶”中,V2O5·2H2O转化为KVO3溶解,写出V2O5·2H2O与KOH反应的化学方程式______ 。
(4)“调pH”中滤渣④的主要成分是______ 。
(5)全钒液流储能电池可实现化学能和电能的相互转化,其原理如图所示。______ 。
②放电过程中,右槽溶液颜色变化的情况是______ 。
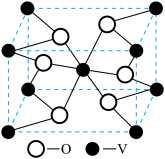
(6)钒的某种氧化物的立方晶胞结构如图所示,钒原子的配位数为______ 。若该晶胞的密度为ρg/cm3,且用NA表示阿伏加德罗常数,则该晶胞的边长为______ nm。
| 金属离子 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 |
 +2OH-=
+2OH-= +H2O
+H2O(1)“酸浸氧化”时,VO2+转化成
 反应的离子方程式为
反应的离子方程式为 。滤渣①主要成分是
。滤渣①主要成分是(2)“中和沉淀”中,钒水解并沉淀为V2O5·2H2O,随滤液②可除去金属离子K+以及部分的金属离子有
(3)“沉淀转溶”中,V2O5·2H2O转化为KVO3溶解,写出V2O5·2H2O与KOH反应的化学方程式
(4)“调pH”中滤渣④的主要成分是
(5)全钒液流储能电池可实现化学能和电能的相互转化,其原理如图所示。
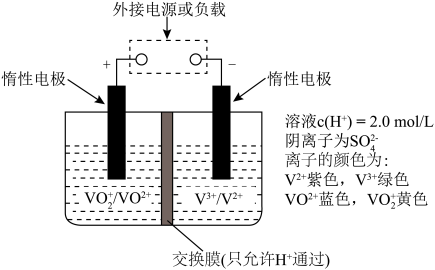
②放电过程中,右槽溶液颜色变化的情况是
(6)钒的某种氧化物的立方晶胞结构如图所示,钒原子的配位数为
您最近一年使用:0次

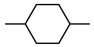
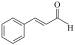 于试管中,滴加酸性KMnO4溶液
于试管中,滴加酸性KMnO4溶液

