1 . 苯是重要的化工原料,可用来合成A和有机物高分子材料N,一种制取A和N的流程如下图所示。
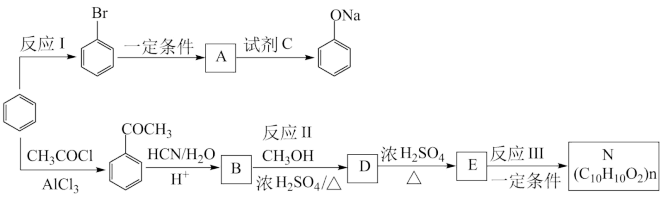
已知:
回答相关问题:
(1)①反应I的反应条件是___________ 。
②试剂C可以选用___________ (选填字母编号)。
a.CH3COONa溶液 b.NaOH溶液 c.NaHCO3溶液 d.Na2CO3溶液
(2)D生成E的过程中,浓硫酸的作用是___________ 。
(3)B中的含氧官能团的名称为___________ 。
(4)反应II、III的化学方程式为___________ 、___________ 。
(5)符合下列条件的B的同分异构体有___________ 种。
A.与Fe3+溶液显紫色;B.属于酯类;C.苯环上只有两个取代基
(6)参照上述合成路线和信息,设计以苯为原料制备另一种高分子化合物 的合成路线
的合成路线___________ 。

已知:

回答相关问题:
(1)①反应I的反应条件是
②试剂C可以选用
a.CH3COONa溶液 b.NaOH溶液 c.NaHCO3溶液 d.Na2CO3溶液
(2)D生成E的过程中,浓硫酸的作用是
(3)B中的含氧官能团的名称为
(4)反应II、III的化学方程式为
(5)符合下列条件的B的同分异构体有
A.与Fe3+溶液显紫色;B.属于酯类;C.苯环上只有两个取代基
(6)参照上述合成路线和信息,设计以苯为原料制备另一种高分子化合物
 的合成路线
的合成路线
您最近一年使用:0次
2022-01-14更新
|
516次组卷
|
3卷引用:陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题
陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题四川省北大成都附属实验学校2021-2022学年高三下学期第四次模拟考试理科综合化学试题(已下线)题型163 以高分子为基的有机推断
2 . 钛被称为继铁、铝之后的第三金属,钛及化合物在生活和生产中有重要应用,钙钛矿中典型代表CaTiO3晶体是工业获取钛的重要原料。回答下列问题:
(1)基态Ti的价电子排布图是___________ ,若Ca原子核外电子有11种空间运动状态,则该原子处于___________ (填“基态"或“激发态”)。
(2)纳米TiO2是一种应用广泛的催化剂,催化实例如图所示。化合物甲分子中采取sp2和sp3杂化的碳原子个数比为___________ ;化合物乙的组成元素第一电离能由大到小的顺序为___________ 。
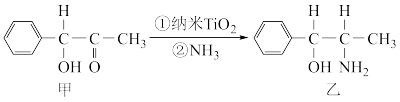
(3)TiC4可以与胺形成配合物,如[TiCl4(CH4NH2)2]、[TiCl4(H2NCH2CH2NH2)]等。
①lmolH2NCH2CH2NH2中含有的σ键数目为___________ 个
②[TiCl4(H2NCH2CH2NH2)]中Ti的配位数是___________ 。
③配合物[TiCl4(H2NCH2CH2NH2)]与游离的H2NCH2CH2NH2分子相比,其H—N—H键角______ (填“较大”,“较小”或“相同”),原因是___________ 。
(4)硫酸氧钛(TiOSO4)晶体中阳离子为链状聚合形式的离子,结构如图1所示,则该阳离子的化学式为_____ ;与其阴离子互为等电子体的微粒有____ 和_____ (写出一种分子和一种阴离子)。
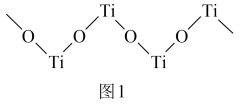
(5)CaTiO3,的晶胞为立方晶胞,结构如图2所示。
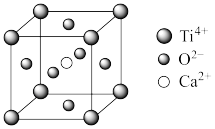
①在晶胞中与Ti距离最近且相等的O2-有______ 个。
②若最近的Ti4+和O2-之间的距离为apm,则晶胞的密度为_____ g·cm-3(用代数式表示,NA为阿伏加德罗常数)。
(1)基态Ti的价电子排布图是
(2)纳米TiO2是一种应用广泛的催化剂,催化实例如图所示。化合物甲分子中采取sp2和sp3杂化的碳原子个数比为

(3)TiC4可以与胺形成配合物,如[TiCl4(CH4NH2)2]、[TiCl4(H2NCH2CH2NH2)]等。
①lmolH2NCH2CH2NH2中含有的σ键数目为
②[TiCl4(H2NCH2CH2NH2)]中Ti的配位数是
③配合物[TiCl4(H2NCH2CH2NH2)]与游离的H2NCH2CH2NH2分子相比,其H—N—H键角
(4)硫酸氧钛(TiOSO4)晶体中阳离子为链状聚合形式的离子,结构如图1所示,则该阳离子的化学式为

(5)CaTiO3,的晶胞为立方晶胞,结构如图2所示。

①在晶胞中与Ti距离最近且相等的O2-有
②若最近的Ti4+和O2-之间的距离为apm,则晶胞的密度为
您最近一年使用:0次
3 . CO2是重要的工业原料,CO2的综合利用有利于碳达峰碳中和目标的最终实现。
(1)CO2和乙烷反应制备乙烯。298K时,相关物质的相对能量如图1所示,CO2与乙烷反应生成乙烯、CO和气态水的热化学方程式为___________ 。
已知:H2O(1)=H2O(g) ∆H=-242kJ·mol-1-(-286kJ·mol-1)=+44kJ·mol-1

(2)在Ru/TiO2催化下发生反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)。若无副反应发生,T℃时向1L恒容密闭容器中充入1molCO2和4molH2,初始总压强为5.0aMPa,反应进行到5min时,CO2与CH4的体积分数相等;10min后反应达到平衡时总压强为3.5aMPa。(已知:分压=总压×组分物质的量分数)
①该可逆反应达到平衡的标志为___________ (填标号)。
A.v(CO2)正和v(CH4)逆的比值为1:1
B.混合气体的平均相对分子质量不变
C.单位体积内分子总数不变
D.四种物质的分压之比等于计量系数之比
E.c(CO2)·c(H2)4=c(CH4)·c(H2O)2
②0~5min内,v(H2)=55mol·L-1min-l;平衡时CO2的分压为________ aMPa,此温度下该反应的平衡常数K=_________ 。
(3)工业上常用电解法和催化法将CO2合成为羧酸以实现资源化处理。
①电解法:以Pt为电极、质子惰性有机溶剂为电解液的装置,可将CO2转化为草酸(H2C2O4),其阴极的电极反应方程式为___________ 。
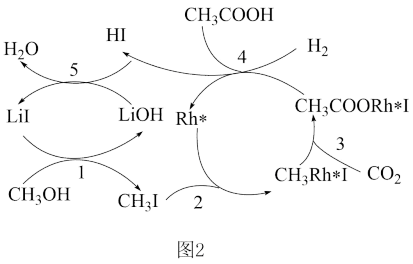
②催化法:图2是在催化剂作用下CO2合成乙酸的反应路径与机理图示,催化循环的总反应化学方程式为___________ (反应条件上注明催化剂的化学式);反应的中间产物共___________ 种。
HI、LiOH、CH3l、CH3Rh*I.
|CH3COORh*I为反应的中间产物
(1)CO2和乙烷反应制备乙烯。298K时,相关物质的相对能量如图1所示,CO2与乙烷反应生成乙烯、CO和气态水的热化学方程式为
已知:H2O(1)=H2O(g) ∆H=-242kJ·mol-1-(-286kJ·mol-1)=+44kJ·mol-1

(2)在Ru/TiO2催化下发生反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)。若无副反应发生,T℃时向1L恒容密闭容器中充入1molCO2和4molH2,初始总压强为5.0aMPa,反应进行到5min时,CO2与CH4的体积分数相等;10min后反应达到平衡时总压强为3.5aMPa。(已知:分压=总压×组分物质的量分数)
①该可逆反应达到平衡的标志为
A.v(CO2)正和v(CH4)逆的比值为1:1
B.混合气体的平均相对分子质量不变
C.单位体积内分子总数不变
D.四种物质的分压之比等于计量系数之比
E.c(CO2)·c(H2)4=c(CH4)·c(H2O)2
②0~5min内,v(H2)=55mol·L-1min-l;平衡时CO2的分压为
(3)工业上常用电解法和催化法将CO2合成为羧酸以实现资源化处理。
①电解法:以Pt为电极、质子惰性有机溶剂为电解液的装置,可将CO2转化为草酸(H2C2O4),其阴极的电极反应方程式为
②催化法:图2是在催化剂作用下CO2合成乙酸的反应路径与机理图示,催化循环的总反应化学方程式为
HI、LiOH、CH3l、CH3Rh*I.
|CH3COORh*I为反应的中间产物

您最近一年使用:0次
4 . 无水FeCl2是重要的污水处理剂,不溶于C6H5Cl、C6H4Cl2,易溶于乙醇,易吸水和易被氧化。某实验小组利用无水FeCl3和C6H5Cl(氯苯,无色液体,沸点132℃)制备少量无水FeCl2。实验原理:2FeCl3+C6H5Cl 2FeCl2+C6H4Cl2+HCl↑,回答以下问题:
2FeCl2+C6H4Cl2+HCl↑,回答以下问题:
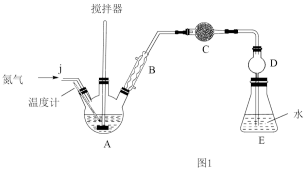
(1)先按图1所示组装好装置,再___________ 后,最后向三颈烧瓶A中加入一定量的无水FeCl3和氯苯(加热装置略去)。
(2)工业氮气中常含有H2O、O2、CO2,需用下图仪器和试剂提纯后才可通入三颈烧瓶A中进行相关反应。
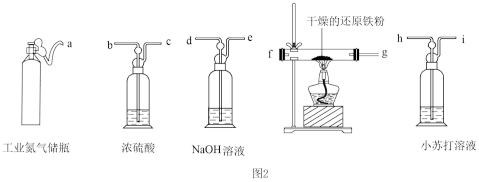
①请从图2中选择必要的装置,按气流方向其合理的连接顺序:a→___________ →j。
②在反应开始之前先通二段时间N2的目的是___________ 。
(3)装置C中的试剂是___________ (填试剂名称),其作用是___________ 。
(4)控制温度在128~139℃条件下对三颈烧瓶A加热2h,混合物颜色逐渐变浅,黏度降低。该步骤中加热温度已经接近或超过C6H5Cl沸点,但氯苯实际损失量却非常小,其原因是___________ 。
(5)下列装置中与D的作用相同的是___________ 。
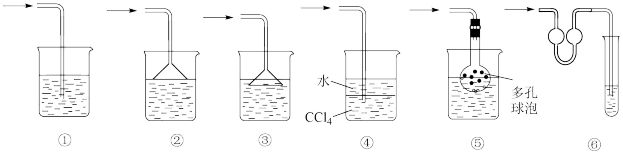
(6)冷却后,将三颈瓶内物质经过滤、洗涤干燥后,得到粗产品。简述回收滤液中C6H5Cl的实验方案___________ 。
 2FeCl2+C6H4Cl2+HCl↑,回答以下问题:
2FeCl2+C6H4Cl2+HCl↑,回答以下问题:
(1)先按图1所示组装好装置,再
(2)工业氮气中常含有H2O、O2、CO2,需用下图仪器和试剂提纯后才可通入三颈烧瓶A中进行相关反应。

①请从图2中选择必要的装置,按气流方向其合理的连接顺序:a→
②在反应开始之前先通二段时间N2的目的是
(3)装置C中的试剂是
(4)控制温度在128~139℃条件下对三颈烧瓶A加热2h,混合物颜色逐渐变浅,黏度降低。该步骤中加热温度已经接近或超过C6H5Cl沸点,但氯苯实际损失量却非常小,其原因是
(5)下列装置中与D的作用相同的是

(6)冷却后,将三颈瓶内物质经过滤、洗涤干燥后,得到粗产品。简述回收滤液中C6H5Cl的实验方案
您最近一年使用:0次
5 . 废旧电路板主要含有塑料。Fe、Cu、SnO2、PbO2等,研究人员一种从处理废旧电路板中回收金属锡(Sn)的流程如下。

已知:Sn和Pb位于周期表第IVA族;SnO2,PbO2可与强碱共热反应生成易溶盐和水。
(1)“焙烧”的主要目的是___________ 。
(2)“滤渣”中含有的金属元素有___________ (填元素符号)。
(3)SnO2与NaOH溶液反应的离子方程式为___________ 。
(4)加入Na2S可与"滤液a”中的Na2PbO3反应以达到除铅的目的,写出相关的化学方程式_____ ;可循环利用的物质的化学式为_______ 。
(5)理论上过量的焦炭与SnO2在高温下恰好反应时二者的质量比为___________ 。
(6)测定粗锡中Sn的纯度:在强酸性环境中将1.0g的粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe(SO4)2溶液,以二苯胺磺酸钠为指示剂,用0.1mol·L-1K2Cr2O7标准溶液滴定至终点。平行测定三次消耗的K2Cr2O7溶液的体积平均为25.00mL,计算Sn的纯度。
已知:由Sn2++2Fe3+=Sn4++2Fe2+、 +6Fe2++14H+=2Cr2++6Fe3++7H2O
+6Fe2++14H+=2Cr2++6Fe3++7H2O
①溶解粗锡时不宜选用浓盐酸,理由是___________ ;
②粗锡样品中Sn的纯度为___________ 。

已知:Sn和Pb位于周期表第IVA族;SnO2,PbO2可与强碱共热反应生成易溶盐和水。
(1)“焙烧”的主要目的是
(2)“滤渣”中含有的金属元素有
(3)SnO2与NaOH溶液反应的离子方程式为
(4)加入Na2S可与"滤液a”中的Na2PbO3反应以达到除铅的目的,写出相关的化学方程式
(5)理论上过量的焦炭与SnO2在高温下恰好反应时二者的质量比为
(6)测定粗锡中Sn的纯度:在强酸性环境中将1.0g的粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe(SO4)2溶液,以二苯胺磺酸钠为指示剂,用0.1mol·L-1K2Cr2O7标准溶液滴定至终点。平行测定三次消耗的K2Cr2O7溶液的体积平均为25.00mL,计算Sn的纯度。
已知:由Sn2++2Fe3+=Sn4++2Fe2+、
 +6Fe2++14H+=2Cr2++6Fe3++7H2O
+6Fe2++14H+=2Cr2++6Fe3++7H2O①溶解粗锡时不宜选用浓盐酸,理由是
②粗锡样品中Sn的纯度为
您最近一年使用:0次
2022-01-14更新
|
702次组卷
|
3卷引用:陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题
6 . 常温下,用NaOH溶液滴定二元弱酸H2R溶液,图中直线①表示溶液中 和
和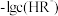 的关系,直线②表示
的关系,直线②表示 和-lgc(R2-)的关系。下列说法正确的是
和-lgc(R2-)的关系。下列说法正确的是

 和
和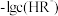 的关系,直线②表示
的关系,直线②表示 和-lgc(R2-)的关系。下列说法正确的是
和-lgc(R2-)的关系。下列说法正确的是
| A.Ka1(H2R)=10-2,Ka2(H2R)=10-4 |
| B.滴定过程中,当pH=6时,c(Na+)=3c(R2-) |
| C.NaHR的溶液中:c(Na+)>c(HR-)>c(R2-)>c(H2R) |
D.溶液中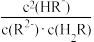 的值为10-3 的值为10-3 |
您最近一年使用:0次
7 . 光电池在光照条件下可产生电压,如图所示装置可实现光能的充分利用。双极膜复合层间的H2O能解离为H+和OH-,且双极膜能实现H+和OH-的定向通过。下列说法的不合理的是


| A.该装置工作时涉及光能、化学能及电能的转化 |
| B.光照过程中阳极区溶液中的n(OH-)基本不变 |
C.再生池中的反应为2V2++2H+ 2V3++H2↑ 2V3++H2↑ |
| D.阳极生成1molO2时,理论上双极膜共解离出离子数4NA个 |
您最近一年使用:0次
2022-01-14更新
|
839次组卷
|
4卷引用:陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题
陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题安徽省“皖南八校”2022届高三下学期第三次联考理综化学试题(已下线)专项11 电化学基础-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)(已下线)题型22 四室膜和双极膜电解装置及其应用
名校
解题方法
8 . m、n、p、q是有机合成中常用的原料,下列说法正确的是


| A.n、p、q互为同系物 |
| B.n的同分异构体中属于羧酸的有5种(不考虑立体异构) |
| C.鉴别p和q可用金属钠或溴水 |
| D.m与q互为同分异构体 |
您最近一年使用:0次
2022-01-14更新
|
881次组卷
|
4卷引用:陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题
陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题(已下线)押江苏卷第10题 有机化合物的结构与性质 -备战2022年高考化学临考题号押题(江苏卷)(已下线)题型156 官能团的性质与有机物的检验云南省昆明市第一中学西山学校2022-2023学年高二下学期4月月考(三)化学试题
9 . 短周期元素Q、X、Y、Z、W原子序数依次增大,Z与W同主族,五种元素组成的一种分子结构如图。下列说法正确的是
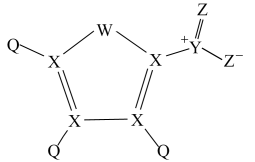

| A.原子半径:W>X>Y>Q |
| B.元素的最高正化合价:Z>Y>X |
| C.Q、X、Y、Z四种元素只能形成共价化合物 |
| D.气态氢化物的沸点:W>Z>X |
您最近一年使用:0次
2022-01-14更新
|
733次组卷
|
3卷引用:陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题
陕西省宝鸡市2021-2022年上学期高考模拟检测(一)理科综合化学试题(已下线)【直击双一流】08-备战2022年高考化学名校进阶模拟卷(通用版)山东省济南大学城实验高中2021-2022学年高三3月阶段性调研化学试题
10 . 实验室制备下列气体所选试剂、制备装置及收集方法均正确的是


| 选项 | 气体 | 试剂 | 制备装置 | 收集装置 |
| A | NH3 | NH4Cl+Ca(OH)2 | a | e |
| B | SO2 | Na2SO3+浓H2SO4 | b | c |
| C | Cl2 | KMnO4溶液+浓HCl | b | d |
| D | CO2 | CaCO3+稀H2SO4 | b | c |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



