1 . 工业上,从铜镍矿(主要成分为铜氧化物、镍氧化物,含有 、
、 、
、 等杂质)中提取镍和铜的一种工艺流程如下:
等杂质)中提取镍和铜的一种工艺流程如下:
②当溶液中某离子浓度c≤10-5mol/L时,可认为该离子沉淀完全。
③
(1)基态 原子的价电子排布图为
原子的价电子排布图为___________ 。
(2)浸出过程中通入 的目的是
的目的是___________ 。
(3)萃取时发生反应: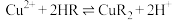 (HR、CuR2在有机层,
(HR、CuR2在有机层, 在水层)。
在水层)。___________ 。
(4)写出用惰性电极电解 溶液发生反应的化学方程式:
溶液发生反应的化学方程式:___________ 。
(5)黄钠铁矾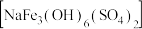 比
比 更易形成沉淀,则生成黄钠铁矾的离子方程式是
更易形成沉淀,则生成黄钠铁矾的离子方程式是___________ 。
(6)第二次使用 调节溶液
调节溶液 ,使
,使 沉淀完全,应将
沉淀完全,应将 调节至
调节至___________ (保留2位小数)。
 、
、 、
、 等杂质)中提取镍和铜的一种工艺流程如下:
等杂质)中提取镍和铜的一种工艺流程如下: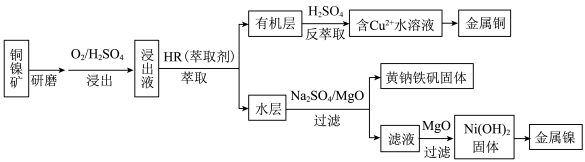
| 物质 |  |  |  |  |
 |  |  |  | 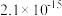 |
③

(1)基态
 原子的价电子排布图为
原子的价电子排布图为(2)浸出过程中通入
 的目的是
的目的是(3)萃取时发生反应:
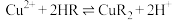 (HR、CuR2在有机层,
(HR、CuR2在有机层, 在水层)。
在水层)。①某种 的结构简式为
的结构简式为 ,该分子中可能与
,该分子中可能与 形成配位键的原子有
形成配位键的原子有
(4)写出用惰性电极电解
 溶液发生反应的化学方程式:
溶液发生反应的化学方程式:(5)黄钠铁矾
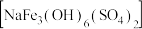 比
比 更易形成沉淀,则生成黄钠铁矾的离子方程式是
更易形成沉淀,则生成黄钠铁矾的离子方程式是(6)第二次使用
 调节溶液
调节溶液 ,使
,使 沉淀完全,应将
沉淀完全,应将 调节至
调节至
您最近一年使用:0次
名校
解题方法
2 . 水杨酸异戊酯( ,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
②按照下图搭建反应装置,在145~155℃油浴下加热回流至不再有水生成。
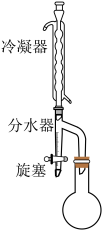
④干燥、减压蒸馏有机层,收集到31.2g产物。
⑤用红外光谱仪和核磁共振仪对产物进行表征。
已知:
①环己烯(沸点83℃)可与水形成沸点为70℃的共沸物。
②沸点:水杨酸211℃、异戊醇131℃、环己烯83℃、水杨酸异戊酯282℃。
回答以下问题:
(1)反应中浓硫酸的作用是吸水剂和
(2)写出制备水杨酸异戊酯的化学方程式
(3)步骤②中表明反应中不再有水生成的现象是
(4)洗涤反应液时需要使用的主要仪器是
(5)步骤③中NaHCO3溶液的作用是
(6)本次实验的产率为
(7)红外光谱图中可获得产物信息包括
a.产物中碳氧双键键长 b.产物相对分子质量
c.产物中含有酯基结构 d.产物中氧元素质量分数
您最近一年使用:0次
名校
3 . 二氧化碳一甲烷重整反应制备合成气(H2+CO)是一种生产高附加值化学品的低碳过程。该过程存在如下化学反应:
①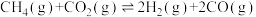

②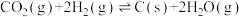
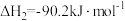
③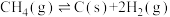
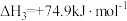
④
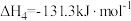
回答下列问题:
(1)
_______ ,该反应在___________ (填“高温”或“低温”或“任意温度”)下可自发进行。
(2)反应体系总压强分别为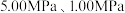 和
和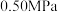 时,
时, 平衡转化率随反应温度变化如图所示,则代表反应体系总压强为
平衡转化率随反应温度变化如图所示,则代表反应体系总压强为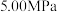 的曲线是
的曲线是_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”),判断依据是_______ 。 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高,
时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高, 的物质的量先增加后减少,主要原因是
的物质的量先增加后减少,主要原因是_______ 。 和
和 反应可制取乙烯,反应的化学方程式为
反应可制取乙烯,反应的化学方程式为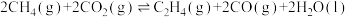 。一定温度下,向某恒容密闭容器中充入
。一定温度下,向某恒容密闭容器中充入 和
和 ,体系的初始压强为
,体系的初始压强为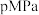 ,若平衡时
,若平衡时 的转化率为
的转化率为 ,不考虑副反应的发生,
,不考虑副反应的发生,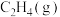 的平衡分压为
的平衡分压为____ Mpa(用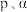 表示,下同),该反应的压强平衡常数
表示,下同),该反应的压强平衡常数
_____ 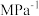 。
。
(5)CH4过光电化学转化可制得乙二醇,以乙二醇为燃料的燃料电池工作时,若以 溶液为电解液,则该电极的电极反应式为
溶液为电解液,则该电极的电极反应式为___________ 。
①
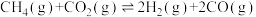

②
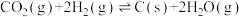
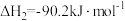
③
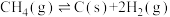
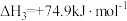
④

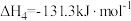
回答下列问题:
(1)

(2)反应体系总压强分别为
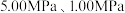 和
和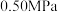 时,
时, 平衡转化率随反应温度变化如图所示,则代表反应体系总压强为
平衡转化率随反应温度变化如图所示,则代表反应体系总压强为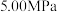 的曲线是
的曲线是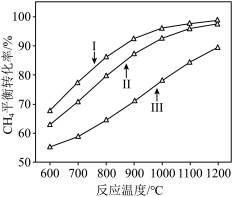
 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高,
时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升高, 的物质的量先增加后减少,主要原因是
的物质的量先增加后减少,主要原因是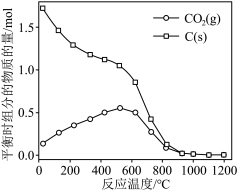
 和
和 反应可制取乙烯,反应的化学方程式为
反应可制取乙烯,反应的化学方程式为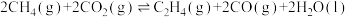 。一定温度下,向某恒容密闭容器中充入
。一定温度下,向某恒容密闭容器中充入 和
和 ,体系的初始压强为
,体系的初始压强为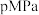 ,若平衡时
,若平衡时 的转化率为
的转化率为 ,不考虑副反应的发生,
,不考虑副反应的发生,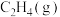 的平衡分压为
的平衡分压为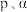 表示,下同),该反应的压强平衡常数
表示,下同),该反应的压强平衡常数
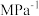 。
。(5)CH4过光电化学转化可制得乙二醇,以乙二醇为燃料的燃料电池工作时,若以
 溶液为电解液,则该电极的电极反应式为
溶液为电解液,则该电极的电极反应式为
您最近一年使用:0次
名校
解题方法
4 . 铁与镁组成的储氢合金的立方晶胞结构如图所示。铁原子位于顶点和面心的位置,镁原子位于将晶胞平分为8个立方单位的体心位置,NA为阿伏加德罗常数的值。下列说法正确的是
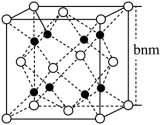
| A.该晶体中存在金属阳离子,所以该合金属于离子晶体 |
B.该晶体密度为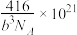 g·cm-3 g·cm-3 |
| C.距离Fe原子最近的Mg原子数为4 |
| D.晶体储氢时,H2在晶胞的体心和棱的中心位置,则储氢后化学式为FeMg2H |
您最近一年使用:0次
5 . 氧钒(Ⅳ)碱式碳酸铵晶体{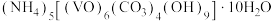 }的制备及纯度分析步骤如下。
}的制备及纯度分析步骤如下。
Ⅰ.制备氧钒(Ⅳ)碱式碳酸铵晶体的流程如下:
 碱式碳酸铵晶体
碱式碳酸铵晶体
其中,步骤ⅱ可通过如图装置完成。
实验步骤: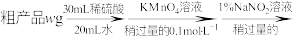
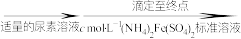 再重复实验两次。
再重复实验两次。
已知:①氧钒(Ⅳ)碱式碳酸铵晶体难溶于水,
②+4价钒在弱酸性条件下具有还原性。
③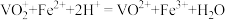 。
。
④在该实验条件下, 与尿素不反应。
与尿素不反应。
回答下列问题:
(1)从原子结构角度解释+5价钒较稳定的原因:_______ 。
(2)步骤ⅰ中 和
和 反应得到的产物之一是一种无毒无害的气体,该反应中氧化剂与还原剂的物质的量之比是
反应得到的产物之一是一种无毒无害的气体,该反应中氧化剂与还原剂的物质的量之比是_______ 。
(3)步骤ⅱ中盛装 溶液的仪器名称为
溶液的仪器名称为_______ 。
(4)步骤ⅱ中装置D的作用是_______ 。
(5)步骤ⅲ中依次用饱和 溶液无水乙醇、乙醚洗涤晶体,用饱和
溶液无水乙醇、乙醚洗涤晶体,用饱和 溶液洗涤的目的是
溶液洗涤的目的是_______ 。
(6)分析测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品纯度的流程:
①滴入 溶液的目的是除去
溶液的目的是除去 ,写出其反应的离子方程式:
,写出其反应的离子方程式:_______ 。
②若平均消耗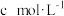
 标准溶液的体积为a mL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为
标准溶液的体积为a mL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为_______ %。
③若其他操作均正确,但 的加入量不足,会引起测定结果
的加入量不足,会引起测定结果_____ (填“偏大”“偏小”或“无影响”)。
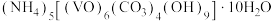 }的制备及纯度分析步骤如下。
}的制备及纯度分析步骤如下。Ⅰ.制备氧钒(Ⅳ)碱式碳酸铵晶体的流程如下:
 碱式碳酸铵晶体
碱式碳酸铵晶体其中,步骤ⅱ可通过如图装置完成。

实验步骤:
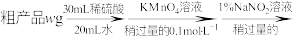
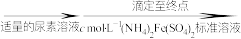 再重复实验两次。
再重复实验两次。已知:①氧钒(Ⅳ)碱式碳酸铵晶体难溶于水,

②+4价钒在弱酸性条件下具有还原性。
③
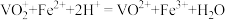 。
。④在该实验条件下,
 与尿素不反应。
与尿素不反应。回答下列问题:
(1)从原子结构角度解释+5价钒较稳定的原因:
(2)步骤ⅰ中
 和
和 反应得到的产物之一是一种无毒无害的气体,该反应中氧化剂与还原剂的物质的量之比是
反应得到的产物之一是一种无毒无害的气体,该反应中氧化剂与还原剂的物质的量之比是(3)步骤ⅱ中盛装
 溶液的仪器名称为
溶液的仪器名称为(4)步骤ⅱ中装置D的作用是
(5)步骤ⅲ中依次用饱和
 溶液无水乙醇、乙醚洗涤晶体,用饱和
溶液无水乙醇、乙醚洗涤晶体,用饱和 溶液洗涤的目的是
溶液洗涤的目的是(6)分析测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品纯度的流程:
①滴入
 溶液的目的是除去
溶液的目的是除去 ,写出其反应的离子方程式:
,写出其反应的离子方程式:②若平均消耗
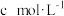
 标准溶液的体积为a mL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为
标准溶液的体积为a mL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为③若其他操作均正确,但
 的加入量不足,会引起测定结果
的加入量不足,会引起测定结果
您最近一年使用:0次
解题方法
6 . 研究 的资源综合利用,对实现“碳达峰”和“碳中和”有重要意义。
的资源综合利用,对实现“碳达峰”和“碳中和”有重要意义。
(1)在 加氢合成
加氢合成 的体系中,同时发生以下反应:
的体系中,同时发生以下反应:
反应 .
.

反应 .
.

反应 .
.
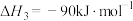
反应 的
的
___________  ,该反应在
,该反应在___________ (填“高温”、“低温”或“任意温度”)下能自发。
(2)向体积为1L的密闭容器中,投入 和
和 ,平衡时CO或
,平衡时CO或 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 转化率随温度的变化如图:
转化率随温度的变化如图: 的反应速率
的反应速率 ,
,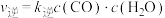 ,
, 、
、 为速率常数,c为物质的量浓度。
为速率常数,c为物质的量浓度。
①图中m代表的物质是___________ 。
②150~400℃范围内,随着温度升高, 的平衡产量的变化趋势是
的平衡产量的变化趋势是___________ 。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ;若p点时体系总压强为
;若p点时体系总压强为 ,反应
,反应 的
的
___________ (保留2位有效数字)。
④由实验测得,随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回起始的状态,原因是___________ 。
(3)将 通入一定浓度的
通入一定浓度的 溶液至饱和,通电后在电极上反应生成
溶液至饱和,通电后在电极上反应生成 ,原理如图所示(阴、阳极区溶液均为
,原理如图所示(阴、阳极区溶液均为 溶液)。生成尿素的电极反应式为
溶液)。生成尿素的电极反应式为___________ 。
 的资源综合利用,对实现“碳达峰”和“碳中和”有重要意义。
的资源综合利用,对实现“碳达峰”和“碳中和”有重要意义。(1)在
 加氢合成
加氢合成 的体系中,同时发生以下反应:
的体系中,同时发生以下反应:反应
 .
.

反应
 .
.

反应
 .
.
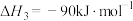
反应
 的
的
 ,该反应在
,该反应在(2)向体积为1L的密闭容器中,投入
 和
和 ,平衡时CO或
,平衡时CO或 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 转化率随温度的变化如图:
转化率随温度的变化如图: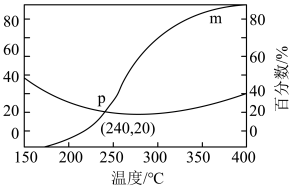
 的反应速率
的反应速率 ,
,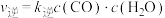 ,
, 、
、 为速率常数,c为物质的量浓度。
为速率常数,c为物质的量浓度。①图中m代表的物质是
②150~400℃范围内,随着温度升高,
 的平衡产量的变化趋势是
的平衡产量的变化趋势是③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ;若p点时体系总压强为
;若p点时体系总压强为 ,反应
,反应 的
的
④由实验测得,随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回起始的状态,原因是
(3)将
 通入一定浓度的
通入一定浓度的 溶液至饱和,通电后在电极上反应生成
溶液至饱和,通电后在电极上反应生成 ,原理如图所示(阴、阳极区溶液均为
,原理如图所示(阴、阳极区溶液均为 溶液)。生成尿素的电极反应式为
溶液)。生成尿素的电极反应式为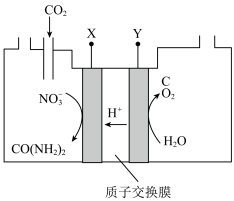
您最近一年使用:0次
解题方法
7 . 二氧化氯( )常用作饮用水的消毒杀菌剂,沸点为11.0℃,某实验小组在实验室用如下装置制备
)常用作饮用水的消毒杀菌剂,沸点为11.0℃,某实验小组在实验室用如下装置制备 并研究其相关性质。
并研究其相关性质。 气体浓度过高时易爆炸分解;②稳定剂可吸收
气体浓度过高时易爆炸分解;②稳定剂可吸收 ,生成
,生成 ,使用时加酸只释放
,使用时加酸只释放 一种气体。
一种气体。
回答下列问题:
Ⅰ.制备 :
:
(1)打开 、
、 ,关闭
,关闭 ,将浓HCl滴入装置A的圆底烧瓶中。
,将浓HCl滴入装置A的圆底烧瓶中。
①盛装浓HCl的仪器名称为___________ 。
②装置A中发生反应的离子方程式为___________ 。
(2)装置B中盛放的试剂是___________ 。
(3)向装置D中通入 的目的是
的目的是___________ ;装置D中发生反应的化学方程式为___________ 。
Ⅱ.验证 的氧化性:
的氧化性:
(4)停止滴加装置A中的浓HCl,待装置D中反应完全时,使___________ (用 、
、 、
、 填空,下同)开启,
填空,下同)开启,___________ 关闭,再将稀盐酸滴入稳定剂中。
(5)观察到装置G中出现的现象是___________ 。
Ⅲ.测定某 溶液的浓度:
溶液的浓度:
(6)为测定某 溶液的浓度,进行如下实验:准确量取10.00mL
溶液的浓度,进行如下实验:准确量取10.00mL 溶液,酸化后加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
溶液,酸化后加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
 标准溶液滴定至终点;重复上述操作2~3次,平均消耗
标准溶液滴定至终点;重复上述操作2~3次,平均消耗 标准溶液30.00mL。已知:
标准溶液30.00mL。已知: ,
, 。则该
。则该 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
 )常用作饮用水的消毒杀菌剂,沸点为11.0℃,某实验小组在实验室用如下装置制备
)常用作饮用水的消毒杀菌剂,沸点为11.0℃,某实验小组在实验室用如下装置制备 并研究其相关性质。
并研究其相关性质。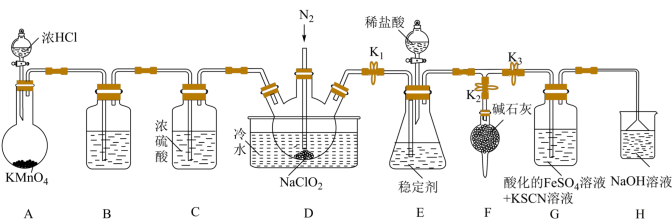
 气体浓度过高时易爆炸分解;②稳定剂可吸收
气体浓度过高时易爆炸分解;②稳定剂可吸收 ,生成
,生成 ,使用时加酸只释放
,使用时加酸只释放 一种气体。
一种气体。回答下列问题:
Ⅰ.制备
 :
:(1)打开
 、
、 ,关闭
,关闭 ,将浓HCl滴入装置A的圆底烧瓶中。
,将浓HCl滴入装置A的圆底烧瓶中。①盛装浓HCl的仪器名称为
②装置A中发生反应的离子方程式为
(2)装置B中盛放的试剂是
(3)向装置D中通入
 的目的是
的目的是Ⅱ.验证
 的氧化性:
的氧化性:(4)停止滴加装置A中的浓HCl,待装置D中反应完全时,使
 、
、 、
、 填空,下同)开启,
填空,下同)开启,(5)观察到装置G中出现的现象是
Ⅲ.测定某
 溶液的浓度:
溶液的浓度:(6)为测定某
 溶液的浓度,进行如下实验:准确量取10.00mL
溶液的浓度,进行如下实验:准确量取10.00mL 溶液,酸化后加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
溶液,酸化后加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
 标准溶液滴定至终点;重复上述操作2~3次,平均消耗
标准溶液滴定至终点;重复上述操作2~3次,平均消耗 标准溶液30.00mL。已知:
标准溶液30.00mL。已知: ,
, 。则该
。则该 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
8 .  (硫酸四氨合铜晶体)的制备和晶体中氨含量的测定如下。已知:硫酸铜在水中的溶解度随温度的升高而增大;硫酸四氨合铜晶体受热易分解。回答下列问题:
(硫酸四氨合铜晶体)的制备和晶体中氨含量的测定如下。已知:硫酸铜在水中的溶解度随温度的升高而增大;硫酸四氨合铜晶体受热易分解。回答下列问题:
Ⅰ.硫酸铜溶液的制备
①称取4g铜粉,在仪器A中灼烧10分钟并不断搅拌,然后放置冷却。
②在蒸发皿中加入30mL3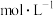
 溶液,将仪器A中的固体慢慢放入其中,加热并不断搅拌。
溶液,将仪器A中的固体慢慢放入其中,加热并不断搅拌。
③趁热过滤,得到蓝色溶液,然后将蓝色溶液冷却到室温。
(1)仪器A的名称为_______ 。
(2)第③步中,趁热过滤的目的是_______ 。
Ⅱ.硫酸四氨合铜晶体的制备
将上述制得的硫酸铜溶液按下图所示进行操作: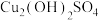 ,则反应生成该沉淀的离子方程式为
,则反应生成该沉淀的离子方程式为______________ 。
(4)析出硫酸四氨合铜晶体时采用加入95%乙醇溶液的方法,原因是______________ 。析出硫酸四氨合铜晶体时不能采用浓缩结晶的方法,原因是_______ 。
Ⅲ.氨含量的测定
精确称取m g晶体,加适量水溶解,注入如图所示的三颈烧瓶中,然后逐滴加入10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用 mL 0.500
mL 0.500 HCl标准溶液完全吸收。取下接收瓶,用0.500
HCl标准溶液完全吸收。取下接收瓶,用0.500 NaOH标准溶液滴定过剩的盐酸,到终点时消耗
NaOH标准溶液滴定过剩的盐酸,到终点时消耗 mL NaOH标准溶液。
mL NaOH标准溶液。_______ (填“酚酞”或“甲基橙”)溶液作指示剂。
(6)样品中氨的质量分数的表达式为_______ (用含m、 、
、 的代数式表示)。
的代数式表示)。
(7)下列实验操作会使氨含量的测定结果偏高的是_______(填标号)。
 (硫酸四氨合铜晶体)的制备和晶体中氨含量的测定如下。已知:硫酸铜在水中的溶解度随温度的升高而增大;硫酸四氨合铜晶体受热易分解。回答下列问题:
(硫酸四氨合铜晶体)的制备和晶体中氨含量的测定如下。已知:硫酸铜在水中的溶解度随温度的升高而增大;硫酸四氨合铜晶体受热易分解。回答下列问题:Ⅰ.硫酸铜溶液的制备
①称取4g铜粉,在仪器A中灼烧10分钟并不断搅拌,然后放置冷却。
②在蒸发皿中加入30mL3
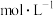
 溶液,将仪器A中的固体慢慢放入其中,加热并不断搅拌。
溶液,将仪器A中的固体慢慢放入其中,加热并不断搅拌。③趁热过滤,得到蓝色溶液,然后将蓝色溶液冷却到室温。
(1)仪器A的名称为
(2)第③步中,趁热过滤的目的是
Ⅱ.硫酸四氨合铜晶体的制备
将上述制得的硫酸铜溶液按下图所示进行操作:
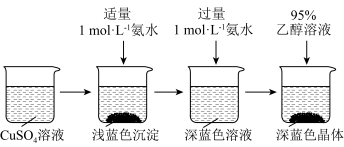
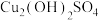 ,则反应生成该沉淀的离子方程式为
,则反应生成该沉淀的离子方程式为(4)析出硫酸四氨合铜晶体时采用加入95%乙醇溶液的方法,原因是
Ⅲ.氨含量的测定
精确称取m g晶体,加适量水溶解,注入如图所示的三颈烧瓶中,然后逐滴加入10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用
 mL 0.500
mL 0.500 HCl标准溶液完全吸收。取下接收瓶,用0.500
HCl标准溶液完全吸收。取下接收瓶,用0.500 NaOH标准溶液滴定过剩的盐酸,到终点时消耗
NaOH标准溶液滴定过剩的盐酸,到终点时消耗 mL NaOH标准溶液。
mL NaOH标准溶液。
(6)样品中氨的质量分数的表达式为
 、
、 的代数式表示)。
的代数式表示)。(7)下列实验操作会使氨含量的测定结果偏高的是_______(填标号)。
| A.读数时,滴定前平视,滴定后俯视 |
| B.碱式滴定管用蒸馏水洗净后未用NaOH标准溶液润洗就直接注入NaOH标准溶液进行滴定 |
| C.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁 |
| D.将样品液中的氨全部蒸出后,未用蒸馏水冲洗导管内壁 |
您最近一年使用:0次
9 . 利用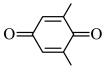 (Q)与
(Q)与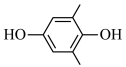 (
(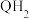 )电解转化法可从烟气中分离出
)电解转化法可从烟气中分离出 ,反就原理如图所示。已知:气体可选择性通过膜电极,溶液不能通过。下列说法错误的是
,反就原理如图所示。已知:气体可选择性通过膜电极,溶液不能通过。下列说法错误的是
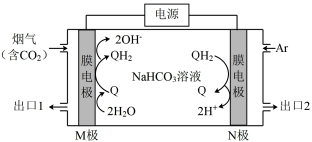
A. 向M极移动 向M极移动 |
B. 在M极被还原 在M极被还原 |
| C.溶液中有机物Q的质量始终保持不变 |
D.N极的电极反应式为 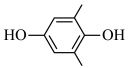  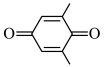 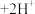 |
您最近一年使用:0次
10 . 一种绿色甲醇的生产方法是:通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制取甲醇。
主反应:
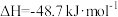
副反应:
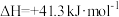
将 和
和 按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知:
按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知: 的产率=
的产率=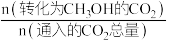 。下列说法错误的是
。下列说法错误的是
主反应:

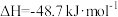
副反应:

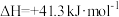
将
 和
和 按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知:
按物质的量之比1∶3混合,以固定流速通过盛放Cu/Zn/Al/Zr(锆)催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。已知: 的产率=
的产率=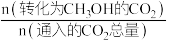 。下列说法错误的是
。下列说法错误的是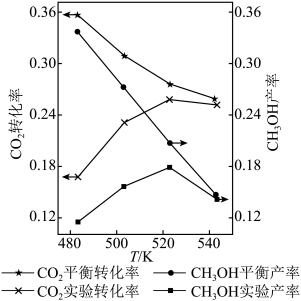
| A.由图可知,催化剂活性最好的温度大约在523K |
| B.483K升温到523K,主反应的反应速率受温度影响更大 |
C.温度由523K升到543K, 的实验产率快速降低的主要原因可能是:温度升高,催化剂的活性降低,导致主反应速率迅速减小 的实验产率快速降低的主要原因可能是:温度升高,催化剂的活性降低,导致主反应速率迅速减小 |
D.为了提高 的平衡转化率和 的平衡转化率和 的平衡产率,可以选择低温、低压条件 的平衡产率,可以选择低温、低压条件 |
您最近一年使用:0次



