名校
1 . X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成 分子;Y与M形成的气态化合物在标准状态下的密度为
分子;Y与M形成的气态化合物在标准状态下的密度为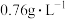 ;W的质子数是X、Y、Z、M四种元素质子数之和的
;W的质子数是X、Y、Z、M四种元素质子数之和的 。下列说法正确的是
。下列说法正确的是
 分子;Y与M形成的气态化合物在标准状态下的密度为
分子;Y与M形成的气态化合物在标准状态下的密度为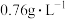 ;W的质子数是X、Y、Z、M四种元素质子数之和的
;W的质子数是X、Y、Z、M四种元素质子数之和的 。下列说法正确的是
。下列说法正确的是| A.原子半径:W>Z>Y>X>M |
B. 、 、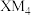 、 、 均为共价化合物 均为共价化合物 |
C.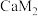 和 和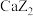 两种化合物中,阳离子与阴离子个数比均为1:2 两种化合物中,阳离子与阴离子个数比均为1:2 |
| D.由X、Y、Z、M四种元素共同形成的化合物中一定有共价键,可能有离子键 |
您最近一年使用:0次
名校
2 . 下列反应的离子方程式正确的是
A.少量 通入 通入 中: 中: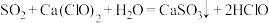 |
B.向二元弱酸 溶液中滴入足量烧碱溶液: 溶液中滴入足量烧碱溶液: |
C. 溶于HI溶液: 溶于HI溶液: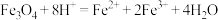 |
D.向含 的溶液通入标准状况下 的溶液通入标准状况下 : : |
您最近一年使用:0次
3 . 某化学小组同学对FeCl3溶液与Na2SO3溶液的反应进行探究
(1)请用离子方程式表示Na2SO3溶液显碱性的原因___________ 。
(2)甲同学认为实验①发生了氧化还原,其反应的离子方程式为___________ ,取反应后的溶液中加入K3[Fe(CN)6]溶液,观察到___________ (填现象),证实了此结论。
(3)乙同学检验红褐色沉淀为Fe(OH)3,请用平衡移动原理解释生成沉淀的原因___________ 。
(4)丙组同学检验实验②中无Fe2+,为探究此浓度下是否能发生氧化还原反应,做了如下实验:向U形管的左侧加入___________ ,观察到___________ (填实验现象),证实此浓度下的FeCl3溶液与Na2SO3溶液可以发生氧化还原反应。 可形成难电离的红色配合物:
可形成难电离的红色配合物: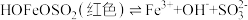 。请解释实验②中无Fe2+生成的原因
。请解释实验②中无Fe2+生成的原因___________ 。
(6)通过以上探究,FeCl3溶液与Na2SO3溶液的反应受___________ 因素影响(至少写出两项)。
| 实验操作 | 现象 | |
| ① |
| 溶液由棕黄色变为红色,无沉淀生成。 放置6小时后,溶液变为淡黄色,始终无沉淀生成。 |
② |
| 溶液由棕黄色变为红色,无沉淀生成。 放置6小时后,生成红褐色沉淀,上层清液为无色。 |
(1)请用离子方程式表示Na2SO3溶液显碱性的原因
(2)甲同学认为实验①发生了氧化还原,其反应的离子方程式为
(3)乙同学检验红褐色沉淀为Fe(OH)3,请用平衡移动原理解释生成沉淀的原因
(4)丙组同学检验实验②中无Fe2+,为探究此浓度下是否能发生氧化还原反应,做了如下实验:向U形管的左侧加入
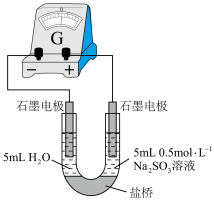
 可形成难电离的红色配合物:
可形成难电离的红色配合物: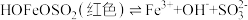 。请解释实验②中无Fe2+生成的原因
。请解释实验②中无Fe2+生成的原因(6)通过以上探究,FeCl3溶液与Na2SO3溶液的反应受
您最近一年使用:0次
4 . 难溶盐  可溶于盐酸。常温下,用
可溶于盐酸。常温下,用  调节
调节  浊液的
浊液的  ,测得体系中−lgc(F−)或−lgc(Ca2+)与
,测得体系中−lgc(F−)或−lgc(Ca2+)与 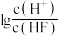 的关系如图所示,下列说法
的关系如图所示,下列说法错误 的是
 可溶于盐酸。常温下,用
可溶于盐酸。常温下,用  调节
调节  浊液的
浊液的  ,测得体系中−lgc(F−)或−lgc(Ca2+)与
,测得体系中−lgc(F−)或−lgc(Ca2+)与 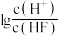 的关系如图所示,下列说法
的关系如图所示,下列说法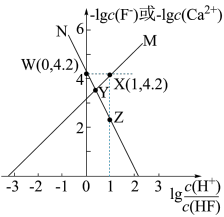
A.随着盐酸的加入, 不断溶解 不断溶解 |
B. 代表−lgc(F−)与 代表−lgc(F−)与 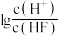 的变化曲线 的变化曲线 |
C.难溶盐  的溶度积常数Ksp(CaF2)=1.0×10−7.4 的溶度积常数Ksp(CaF2)=1.0×10−7.4 |
D. 点溶液中存在lgc(Ca2+)—2 点溶液中存在lgc(Ca2+)—2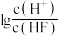 =—4.2 =—4.2 |
您最近一年使用:0次
名校
5 . 结晶玫瑰和高分子树脂M的合成路线如下图所示:
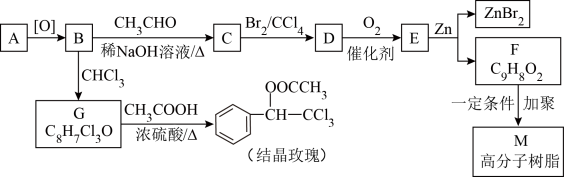
已知:①A是苯的同系物,在相同条件下,其蒸气相对于氢气的密度为46
② (-R表示烃基)
(-R表示烃基)
③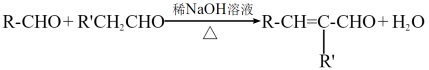 (R、R′表示烃基或氢)
(R、R′表示烃基或氢)
④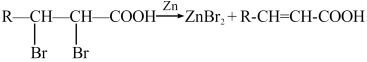
(1)C中官能团的名称为_______ ,E的结构简式为_______ 。
(2)写出由G生成结晶玫瑰的化学方程式:_______ 。
(3)上述流程中“C→D”在M的合成过程中的作用是_______ 。
(4)已知G在一定条件下水解生成H(C8H8O3),与H有相同官能团且与氯化铁溶液发生显色反应的同分异构体的数目有_______ 种。
(5)E的同分异构体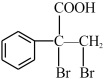 是一种重要的药物中间体,其合成路线与E相似,请以
是一种重要的药物中间体,其合成路线与E相似,请以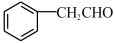 为原料设计它的合成路线
为原料设计它的合成路线_______ (其他所需原料自选)。

已知:①A是苯的同系物,在相同条件下,其蒸气相对于氢气的密度为46
②
 (-R表示烃基)
(-R表示烃基)③
 (R、R′表示烃基或氢)
(R、R′表示烃基或氢)④
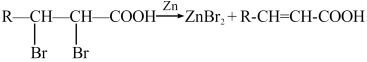
(1)C中官能团的名称为
(2)写出由G生成结晶玫瑰的化学方程式:
(3)上述流程中“C→D”在M的合成过程中的作用是
(4)已知G在一定条件下水解生成H(C8H8O3),与H有相同官能团且与氯化铁溶液发生显色反应的同分异构体的数目有
(5)E的同分异构体
 是一种重要的药物中间体,其合成路线与E相似,请以
是一种重要的药物中间体,其合成路线与E相似,请以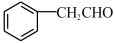 为原料设计它的合成路线
为原料设计它的合成路线
您最近一年使用:0次
名校
6 . 某同学用 与浓盐酸反应制备纯净的
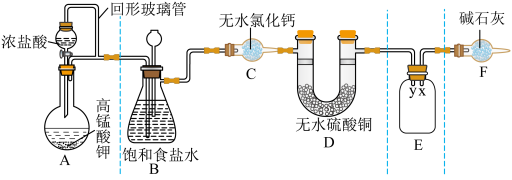
与浓盐酸反应制备纯净的 的装置如图所示。回答下列问题:
的装置如图所示。回答下列问题:
已知: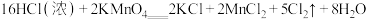
(1)装置A中盛放浓盐酸的仪器名称是
(2)E装置中导管(填“x”或“y”)
(3)装置F的作用有两个:一是
请写出氯气与碱石灰反应的化学方程式
(4)
 、HClO和
、HClO和 三种微粒的物质的量分数随pH(即
三种微粒的物质的量分数随pH(即 )变化的关系如图所示。
)变化的关系如图所示。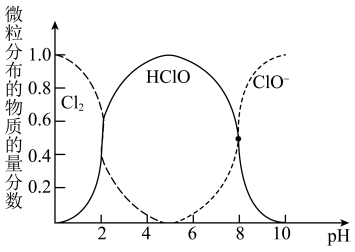
回答问题:①使用84消毒液时为增强消毒效果常调节4<pH<6,原因是
②通常购买的84消毒液pH在12左右,为增强消毒效果可向其中滴加
A.可口可乐 B.稀 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸
(5)实验室将
 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为 ,计算此时所得溶液中NaClO的质量分数为
,计算此时所得溶液中NaClO的质量分数为
您最近一年使用:0次
名校
解题方法
7 . 有机物X完全燃烧的产物只有二氧化碳和水,元素组成分析发现,该物质中碳元素的质量分数为64.86%,氢元素的质量分数为13.51%,它的核磁共振氢谱有5组明显的吸收峰,且只含有两个甲基。下列关于有机物X的说法正确的是
A.分子式为 | B.X只可能催化氧化成醛 |
| C.与X互为官能团异构的同分异构体有3种 | D.X可能消去生成两种结构的烯烃 |
您最近一年使用:0次
8 . 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼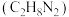 ,
, 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有 、
、 、
、 ,并放出大量热。
,并放出大量热。
已知:①

②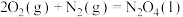

③

请写出上述反应的热化学方程式:______ 。
(2)碘蒸气存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程 (k为速率常数)。
(k为速率常数)。
下列表述正确的是______。
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中 和
和 发生反应
发生反应

 。实验测得:
。实验测得: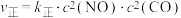 ,
, (
( 、
、 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。
①达到平衡后,仅升高温度, 增大的倍数
增大的倍数______ (填“大于”“小于”或“等于”) 增大的倍数
增大的倍数
②若在 的密闭容器中充入
的密闭容器中充入 和
和 ,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则
,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则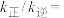
______ 。(保留小数点后两位)
(4)实验室用 溶液处理
溶液处理 ,已知
,已知 ,某吸收液中溶质只含
,某吸收液中溶质只含 ,溶液中
,溶液中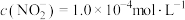 ,取该溶液
,取该溶液 ,加1滴
,加1滴 的
的 溶液混合均匀(20滴约为
溶液混合均匀(20滴约为 ),估算
),估算______ (填“能”或“不能”)产生 沉淀。
沉淀。
(5)一种以液态肼 为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达
为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:______ 。
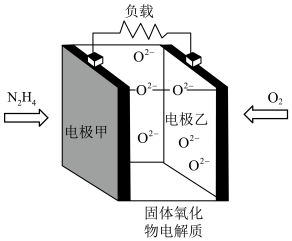
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼
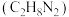 ,
, 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有 、
、 、
、 ,并放出大量热。
,并放出大量热。已知:①


②
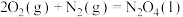

③


请写出上述反应的热化学方程式:
(2)碘蒸气存在能大幅度提高
 的分解速率,反应历程为:
的分解速率,反应历程为:第一步:
 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
 (快反应)
(快反应)实验表明,含碘时
 分解速率方程
分解速率方程 (k为速率常数)。
(k为速率常数)。下列表述正确的是______。
A. 分解反应中,k值与碘蒸气浓度大小有关 分解反应中,k值与碘蒸气浓度大小有关 |
| B.第二步对总反应速率起决定作用 |
| C.第二步活化能比第三步大 |
| D.IO为反应的催化剂 |
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中
 和
和 发生反应
发生反应

 。实验测得:
。实验测得: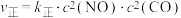 ,
, (
( 、
、 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。①达到平衡后,仅升高温度,
 增大的倍数
增大的倍数 增大的倍数
增大的倍数②若在
 的密闭容器中充入
的密闭容器中充入 和
和 ,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则
,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则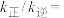
(4)实验室用
 溶液处理
溶液处理 ,已知
,已知 ,某吸收液中溶质只含
,某吸收液中溶质只含 ,溶液中
,溶液中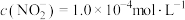 ,取该溶液
,取该溶液 ,加1滴
,加1滴 的
的 溶液混合均匀(20滴约为
溶液混合均匀(20滴约为 ),估算
),估算 沉淀。
沉淀。(5)一种以液态肼
 为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达
为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
您最近一年使用:0次
9 . 某实验小组在实验室制备氢氧化亚铁。
(一)制备氢氧化亚铁

(1)仪器g的名称是_______ ,选择上图中的装置制备氢氧化亚铁,连接顺序为_______ (按气流方向,用装置字母表示)。
(2)反应结束后继续通一段时间的N2,目的是_______ ,装置B中发生反应的离子方程式是_______ ,装置C的作用是_______ 。
(二)探究灰绿色沉淀的成因
反应后将装置B中固体过滤时白色沉淀会逐渐转变为灰绿色,实验小组为探究灰绿色沉淀的成因,查阅到以下资料:
i.Fe(OH)2沉淀具有较强的吸附性;
ii.若存在固体杂质,会导致Fe(OH)2沉淀不够紧密,沉淀与溶液的接触面积会更大。
甲同学猜测灰绿色可能是Fe(OH)2吸附Fe2+引起的,设计并完成了实验1~实验3。
(3)依据甲同学的猜测,实验1中沉淀无灰绿色的原因为_______ 。
(4)实验3中立即出现灰绿色浑浊的原因为_______ 。
(5)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件除了隔绝氧气外还有_______ 。
(一)制备氢氧化亚铁

(1)仪器g的名称是
(2)反应结束后继续通一段时间的N2,目的是
(二)探究灰绿色沉淀的成因
反应后将装置B中固体过滤时白色沉淀会逐渐转变为灰绿色,实验小组为探究灰绿色沉淀的成因,查阅到以下资料:
i.Fe(OH)2沉淀具有较强的吸附性;
ii.若存在固体杂质,会导致Fe(OH)2沉淀不够紧密,沉淀与溶液的接触面积会更大。
甲同学猜测灰绿色可能是Fe(OH)2吸附Fe2+引起的,设计并完成了实验1~实验3。
| 实验 | 操作 | 试剂(均为0.1mol/L) | 实验现象 |
| 1 |  向两片玻璃片中心分别滴加试剂,面对面快速夹紧 | i.1滴FeSO4溶液 ii.4滴NaOH溶液 | 玻璃片夹缝中有白色浑浊 |
| 2 | i.4滴FeSO4溶液 ii.1滴NaOH溶液 | 玻璃片夹缝中有白色浑浊,一段时间后变为灰绿色 | |
| 3 | i.2滴FeSO4溶液, 1滴Fe2(SO4)3溶液 ii.2滴NaOH溶液 | 玻璃片夹缝中立即有灰绿色浑浊 |
(3)依据甲同学的猜测,实验1中沉淀无灰绿色的原因为
(4)实验3中立即出现灰绿色浑浊的原因为
(5)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件除了隔绝氧气外还有
您最近一年使用:0次
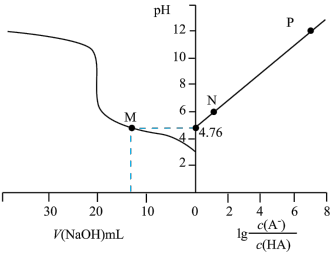
10 . 常温下,用0.1000mol/LNaOH溶液滴定一定浓度的HA溶液,溶液的pH与加入NaOH溶液的体积V(NaOH)、lg 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是
 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是
| A.可用酚酞作该滴定的指示剂 | B.Ka(HA)的数量级为10-5 |
| C.水的电离程度:M<N<P | D.pH=7时,c(Na+)>c(HA) |
您最近一年使用:0次





